Характеристика молекулярных механизмов развития опухолей является ключом не только к пониманию их патогенеза, но также к созданию эффективных диагностических и лечебных подходов. Нейроонкология в данном отношении занимает особое место в силу как уникальных особенностей возникновения и развития новообразований, так и следующей из этого сложности создания действенных лечебно-диагностических подходов. Наиболее полно данные характеристики соответствуют глиальным опухолям, занимающим ведущие позиции среди всех опухолей центральной нервной системы (ЦНС) [1].
В рамках более ранних работ мы провели комплексное изучение роли атипических изоформ протеинкиназы C в диффузных глиомах различной степени злокачественности. Для протеинов семейства атипических изоформ протеинкиназы C характерно, что они не требуют для своей активации ни Ca2+, ни диацилглицерола. Важнейшими членами данного семейства являются протеинкиназа С ζ, протеинкиназа Mζ (ПК Mζ), протеинкиназа С iota (ПК Ci) и протеинкиназа C λ [2]. Данные протеины характеризуются необычными свойствами, в том числе более высокой каталитической активностью [2]. Стоит подчеркнуть, что ПК Mζ является мозгоспецифичной, в отличие от других протеинкиназ она встречается только в клетках головного мозга, участвуя в реализации различных клеточных функций. Более того, для данной протеинкиназы типично свойство самоподдержания собственной активности, благодаря чему существует возможность ее автономного функционирования [3] и участия в важнейших молекулярно-биологических процессах.
В наших работах мы впервые показали, что ПК Ci и ПК Mζ выраженно экспрессируются в диффузных глиомах различной степени злокачественности; более того, ПК Mζ значимо влияет на общую и безрецидивную выживаемость пациентов с диффузными астроцитомами (ДА), анапластическими астроцитомами (АА) и глиобластомами (ГБ), в то же время активность экспрессии ПК Ci значимо влияет на общую и безрецидивную выживаемость пациентов с ГБ. При этом мы предположили, что данные протеинкиназы могут выступать в роли своеобразных маркеров для оценки активности клеток глиом [4]. Принцип дифференцированного подхода к изучению молекулярных свойств каждой опухолевой клетки в отдельности с последующим кластерированием и выделением клеточных популяций с различными свойствами становится все более популярным, поскольку позволяет с новой стороны, более глубоко рассмотреть свойства каждой опухоли. Путем применения технологий single-cell секвенирования было показано наличие нескольких клеточных популяций в составе глиом различной степени злокачественности, каждая из которых может вносить свой вклад в прогрессирование диффузной глиомы [5]. Существенное значение придается также фактору стволовых свойств клеток, который неравномерно распределяется в выделенных популяциях [5]. Попытка проникнуть в особенности внутриопухолевой гетерогенности диффузных глиом имеет как огромное практическое значение, позволяя создавать более прецизионные методы диагностики и таргетного лечения новообразований, так и фундаментальное значение, формируя принципиально новое представление о механизмах глиомогенеза.
Поэтому мы решили попытаться использовать ПК Ci и ПК Mζ в качестве маркеров для оценки активности опухолевых клеток с целью выделения на основе неравномерности их экспрессии клеточных кластеров в ткани диффузных глиом различной степени злокачественности. Также мы поставили задачу в настоящем исследовании охарактеризовать значимость для каждого выделенного кластера других наиболее важных для процессов канцерогенеза протеинкиназ, в частности протеинкиназы Cα, протеинкиназы PKCη, Akt1 протеинкиназы, STAT1 киназы [6, 7]. Наконец, учитывая значимость фактора глиомных стволовых клеток (ГСК) для патогенеза диффузных глиом, мы изучили их распределение с использованием маркера CD133 в полученных клеточных кластерах.
Материалы и методы исследования
Группа для исследования
В рамках проведенного исследования были взяты при хирургическом вмешательстве в НМИЦ нейрохирургии им. акад. Н.Н. Бурденко в 2014–2018 гг. по 30 образцов диффузной астроцитомы, IDH-мутантной (ДА), анапластической астроцитомы, IDH-мутантной (АА), глиобластомы, IDH-дикого типа (ГБ). Пациенты с ДА характеризовались средним возрастом на момент операции 38,24±4,82 года, с АА – 44,42±2,36 года, с ГБ – 62,42±4,28 года. Диагноз был подтвержден в лаборатории нейроморфологии при проведении патогистологического и молекулярно-генетического исследований при участии трех опытных патологов.
Проведение иммуногистохимии для всех маркеров
Для проведения исследования изготавливали срезы толщиной 3 мкм из парафиновых блоков с фиксированными в них образцами опухолей, далее образцы депарафинировали с использованием ксилола и повторно гидратировали с помощью различных концентраций этанола, после чего срезы высушивали в термостате при 45°C. После этого проводили инкубацию с кроличьими моноклональными антителами против антигена ПК Mζ (Abcam, Великобритания), ПК Сi человека (Abcam, Великобритания), протеинкиназы Cα (Abcam, Великобритания), протеинкиназы PKCη (Abcam, Великобритания), Akt1 протеинкиназы (Abcam, Великобритания), STAT1 киназы (Abcam, Великобритания), CD133 (Abcam, Великобритания) и конъюгировали с антикроличьим мышиным IgG антителом против пероксидазы хрена (Cell Marque, Sigma-Aldrich, США). Визуализацию сайтов связывания антител проводили с помощью тетрагидрохлорида 3,3'-диаминобензидина (Ventana Medical Systems, США), ядра клеток окрашивали гематоксилином.
Первичный анализ изображений
Все полученные препараты были оцифрованы с использованием сканера Aperio 3T (Leica Biosystems, GmbH). Все полученные сканированные изображения для маркеров ПК Mζ и ПК Ci подвергались медианной фильтрации для эффективного удаления шума при сохранении важных деталей для последующего распознавания с помощью программного обеспечения ImageJ (Национальный институт здравоохранения, США), Adobe Photoshop (Adobe Systems, США) и QuPath (Университет Эдинбурга, Великобритания). Затем проводилось нерезкое маскирование для всех изображений с использованием Aperio ImageScope (Leica Biosystems, GmbH), ImageJ и QuPath. Затем на полученных изображениях с использованием программного обеспечения, описанного выше, были выделены отдельные клетки и ядра клеток, а также положительные метки для обоих маркеров полуавтоматическим способом с применением программного алгоритма под контролем двух операторов.
Проведение кластеризации
После этого был выполнен кластерный анализ сложных изображений с использованием программного обеспечения Matlab (The MathWorks, США) и SPSS Statistics 23 (IBM, США). Для этих целей использовался метод k-средних. В качестве исходных данных для кластеризации для каждой клетки служили координаты клетки, наличие или отсутствие меток в клетке, значения показателя цветности меток в соответствии с эталонной моделью CIE XYZ (при отсутствии метки это значение принималось равным 0), кластеризация проводилась отдельно для ПК Mζ и ПК Ci. Для этого были определены значения цветности каждого пикселя внутри метки для красной кривой (Y), зеленой кривой (Z) и синей кривой (X), а затем был рассчитан средний индекс цветности для всей метки. Клетки были сгруппированы с выделением групп клеток, образующих повторяющиеся скопления, которые мы назвали кластерами клеток.
Проведение вторичного анализа
Далее были получены сложные, комплексные изображения, которые включали в себя точно совмещенные по координатным данным препараты с маркером ПК Mζ и протеинкиназами Cα, PKCη, Akt1, STAT1 киназой, CD133, а также ПК Ci и теми же протеинкиназами и CD133, после чего размечались выявленные ранее клеточные кластеры. Затем был проведен вторичный анализ изображений, целью которого было рассчитать активность экспрессии протеинкиназы Cα, протеинкиназы PKCη, Akt1 протеинкиназы, STAT1 киназы, CD133 в каждом выявленном кластере во всех препаратах. Для каждого маркера проводилась оценка полуколичественным методом по типу histoscore активности экспрессии (АЭ) в каждом выявленном кластере. Далее подсчитывалось среднее значение АЭ для каждого маркера в каждом кластере по всем изученным препаратам.
Статистический анализ
При проведении статистического анализа сравнение средних двух выборок производилось с использованием U-теста Манна–Уитни. Для выявления корреляций показателей между собой применялся корреляционный анализ по методу Пирсона. Все статистические тесты были выполнены с использованием программного обеспечения SPSS Statistics 22 (IBM, США). Значения p<0,05 считались статистически значимыми.
Результаты исследования и их обсуждение
Результаты проведения кластерного анализа
В рамках проведения кластерного анализа было выявлено, что активность экспрессии ПК Mζ действительно распределяется достаточно неравномерно в ткани глиом различной степени злокачественности. Подобная выраженная гетерогенность распределения ПК Mζ в ткани опухолей позволила выделить с помощью метода k-средних отдельные клеточные кластеры, которые хорошо разделялись, в каждом виде опухолей. В ДА и АА выделялись три клеточных кластера. Первый кластер располагался непосредственно вокруг сосудов и включал в себя группу клеток, наиболее близко расположенную к сосудистой стенке, поэтому данный кластер был назван нами периваскулярным кластером (ПВК). Второй кластер находился непосредственно вокруг первого кластера, окружая его со всех сторон, и был назван транзиторным васкулярным кластером (ТВК). Наконец, третий кластер включал в себя все остальные зоны опухолевой ткани и был назван нами промежуточным кластером (ПК) (рис. 1).
Стоит заметить, что наибольшая АЭ ПК Mζ в ДА и АА выявлялась в ПВК, она составила 102,96±4,24% и 108,16±4,48% соответственно и была выше таковых в ТВК в ДА и АА, в которых АЭ ПК Mζ составила 68,42±4,46% и 70,28±6,22% соответственно. При этом различия как для ДА, так и для АА носили статистически значимый характер (p=0,000072 и p=0,000032 соответственно). В то же время АЭ ПК Mζ в ТВК была выше таковой в ПК как в ДА, так и АА, в ПК она составила 52,18±4,48% и 56,24±4,42% соответственно. Данные различия были статистически значимыми как для ДА, так и для АА (p=0,000068 и p=0,000452 соответственно).
При проведении кластеризации в ткани ГБ удалось выделить пять кластеров, в том числе три ранее выделенных – ПВК, ТВК и ПК. Расположение данных кластеров в ткани опухоли соответствовало таковому в ДА и АА, при этом выделились еще два кластера. Один из них располагался непосредственно вокруг зоны некрозов и был назван нами перинекротическим кластером (ПНК). Другой кластер располагался вокруг предыдущего и был назван по аналогии с ТВК транзиторным некротическим кластером (ТНК) (рис. 1). В рамках сравнения выделенных кластеров по уровню АЭ ПК Mζ в ГБ было показано, что наибольший уровень данного параметра выявлялся в ПВК и составил 109,28±6,42%. На втором месте АЭ ПК Mζ в ТНК, в котором она составила 82,44±2,38%, при этом разница с ПВК носила статистически значимый характер (p=0,000028). На третьем месте по АЭ ПК Mζ находился ТВК, в котором она составила 74,34±2,46%, кроме того, выявленные различия с ТНК были статистически достоверными (p=0,002136). Далее на четвертом месте по АЭ ПК Mζ располагался ПК, в котором она составила 50,38±2,28%, в то же время разница с ТВК была статистически значимой (p=0,000082). Самая низкая АЭ ПК Mζ наблюдалась в ПНК и составила 46,48±4,34%, при этом различия с ПК были статистически значимыми (p=0,004242) (рис. 1).
При рассмотрении возможности применения ПК Ci в качестве маркера для проведения кластерного анализа было показано, что данный маркер распределяется в ткани диффузных глиом с низкой степенью неравномерности. Выделение клеточных кластеров с помощью кластерного анализа показало низкую степень дифференциации между кластерами. В целом ПК Ci существенно менее применима в связи со всем вышеизложенным для выделения клеточных кластеров в новообразованиях.
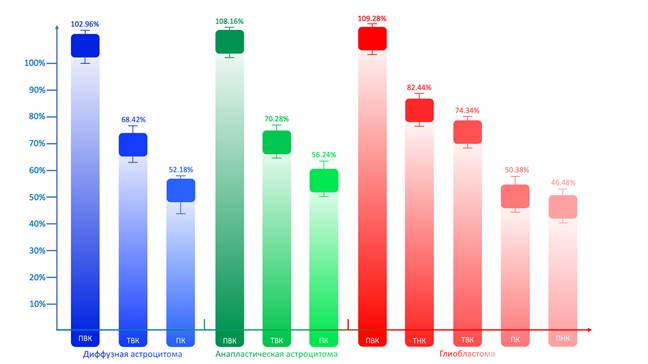
Рис. 1. Кластеры в ткани глиальных новообразований, выделенные по выраженности продукции протеинкиназы Mζ (ПК Mζ). По оси абсцисс приводятся гистологические виды глиом, а также соответствующие виды кластеров, в том числе периваскулярный кластер (ПВК), транзиторный васкулярный кластер (ТВК), промежуточный кластер (ПК), перинекротический кластер (ПНК) и транзиторный некротический кластер (ТНК). По оси ординат приведены средние значения активности ПК Mζ в каждом кластере
Протеинкиназы в кластерах в ДА
В рамках рассмотрения вопроса раздельного выявления АЭ протеинкиназы Cα, протеинкиназы PKCη, Akt1 протеинкиназы, STAT1 киназы в различных клеточных кластерах в ДА было выявлено, что только протеинкиназа Cα гетерогенно распределялась в ткани новообразования, остальные протеинкиназы распределялись в кластерах относительно равномерно. В то же время наибольшая АЭ протеинкиназы Cα выявлялась в ПВК, в котором она составила 68,32±6,26%. Данный показатель в ТВК составил 52,44±2,72%, в то время как в ПК он составил 52,34±2,64%, при том АЭ протеинкиназы Cα в ПВК была статистически значимо больше по сравнению с ТВК и ПК (p=0,007246 и p=0,006248 соответственно) (рис. 2).
Распределение АЭ протеинкиназ в кластерах в АА
При рассмотрении распределения в кластерах в АА экспрессии протеинкиназы Cα, протеинкиназы PKCη, Akt1 протеинкиназы, STAT1 киназы было выявлено, что также только протеинкиназа Cα распределяется в кластерах неравномерно. Было показано, что протеинкиназа Cα также наиболее выраженно экспрессируется в ПВК, АЭ в данном кластере рассматриваемого протеина составляет 74,22±4,52%. В то же время в ТВК АЭ протеинкиназы Cα составила 58,42±6,42%, в ПК данный показатель составил 56,18±6,12%, при этом уровни АЭ протеинкиназы Cα в ПВК были статистически значимо выше по сравнению с ТВК и ПК (p=0,006274 и p=0,005486 соответственно) (рис. 2).
Распределение АЭ протеинкиназ в кластерах в ГБ
При изучении АЭ протеинкиназы Cα, протеинкиназы PKCη, Akt1 протеинкиназы, STAT1 киназы в кластерах в ГБ было показано, что гетерогенное распределение в ткани демонстрирует только протеинкиназа Cα. Для данной протеинкиназы АЭ была наибольшей в ПВК, в котором она составила 78,62±4,38%. В то же время в ТНК данный параметр составил 62,28±4,42%, при этом в ПВК рассматриваемый показатель был статистически значимо выше (p=0,000058). Далее по рассматриваемому параметру расположились ТВК со значением 56,22±4,74%, ПК со значением 56,36±4,62% и ПНК со значением 56,42±4,18%, все три кластера статистически значимо различались по АЭ протеинкиназы Cα с ТНК (p=0,002486 для ТВК, p=0,004262 для ПК и p=0,004886 для ПНК) (рис. 2).
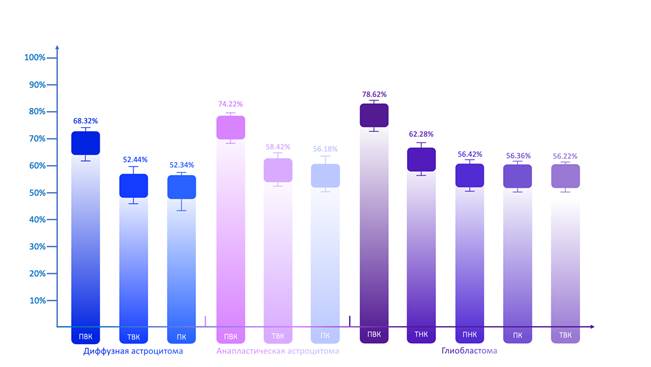
Рис. 2. Выраженность продукции протеинкиназы Cα в кластерах диффузных глиом. По оси абсцисс приводятся гистологические виды глиом, а также соответствующие виды кластеров, в том числе периваскулярный кластер (ПВК), транзиторный васкулярный кластер (ТВК), промежуточный кластер (ПК), перинекротический кластер (ПНК) и транзиторный некротический кластер (ТНК). По оси ординат приведены средние значения активности протеинкиназы Cα в каждом кластере
Распределение клеток со стволовыми свойствами
Клетки со стволовыми свойствами с наличием маркера CD133 выявлялись практически исключительно в ткани ГБ. Было показано, что данный тип клеток существенно превалировал в рамках ПВК, в котором процент позитивных клеток равнялся 36,44±4,38%. Далее по рассматриваемому параметру следовал ТВК, в котором данный показатель составил 28,16±4,22%. За ним расположился ПК с показателями процента CD133 позитивных клеток 16,12±2,82%. Наиболее низкие значения выявлялись в ПНК и ТНК, в них данный параметр составлял 4,88±2,12% и 4,14±2,26% соответственно. В целом различия между всеми кластерами в отношении процента клеток с позитивным CD133 были статистически значимыми.
Другой важной закономерностью при рассмотрении распределения клеток со стволовыми свойствами стала положительная корреляция между наличием стволового маркера в клетке и активностью экспрессии ПК Mζ высокой степени (коэффициент корреляции составил 0,82).
В рамках нашего исследования мы получили очень интересные результаты. В частности, было выявлено, что экспрессия ПК Mζ распределяется в ткани неравномерно. На основе неравномерности распределения можно выделить клеточные кластеры с различными молекулярными свойствами. Кластеры имеют четкие топографические особенности и определенное взаимоотношение с важнейшими гистологическими структурами в ткани опухоли. Более того, важно также заметить, что настоящие данные хорошо согласуются с полученными нами ранее результатами по изучению внутриопухолевой гетерогенности ГБ, в рамках которого выделение клеточных кластеров проводилось на основе пролиферативной и антиапоптозной активности всех клеток [8]. Кластерирование на основе АЭ ПК Mζ позволило выявить идентичные предшествующему исследованию кластеры, таким образом, ПК Mζ распределяется в ткани диффузных глиом в соответствии с градиентом изменения таких ключевых функциональных параметров новообразования, как пролиферативная и антиапоптозная активности. По сути, это указывает на ключевую роль ПК Mζ в реализации пролиферативного потенциала опухолевых клеток, а также на возможность применения методов оценки АЭ ПК Mζ как важнейшего инструмента не только для характеристики внутриопухолевой гетерогенности, но и для разработки инновационных персонализированных методов диагностики и лечения глиом.
Нельзя не заметить также другой важный фактор, на этот раз клеточного свойства, который непосредственно влияет на свойства как отдельных кластеров, так и опухоли в целом, – ГСК. Мы продемонстрировали преимущественное скопление подобных клеток в наиболее активных клеточных кластерах. Более того, нам удалось показать наличие четкой корреляции стволовых свойств опухолевых клеток с АЭ в них ПК Mζ, что дополнительно подчеркивает роль данного протеина в раскрытии злокачественного потенциала глиомы.
Также мы выявили другую важную закономерность, связанную с изучением роли наиболее важных для патогенеза глиальных опухолей протеинкиназ в каждом клеточном кластере раздельно. Мы выявили, что потенциально ключевым молекулярным фактором, действующим под влиянием ПК Mζ или в связке с ней, является протеинкиназа Cα. Данный протеин может выполнять различные роли и не столь сильно при этом связан с процессом глиомогенеза, тем не менее может выступать в качестве важного вторичного посредника или младшего партнера при реализации функций ПК Mζ в клетках новообразования.
Заключение
В данной работе были получены крайне любопытные результаты, значимость которых лежит не только в фундаментальной, но также в практической плоскости. В частности, нам удалось доказать важнейшую роль в процессах глиомогенеза ПК Mζ, также данный фактор может выступать в качестве ценного инструмента для оценки активности опухолевой ткани глиом, непосредственно учитывающего особенности внутриопухолевой гетерогенности. Дополнительно была охарактеризована взаимосвязь ГСК с ПК Mζ, при этом была выявлена важная роль данного протеина в поддержании стволового состояния. Более того, полученные функциональные кластеры были дополнительно изучены нами на предмет активности в них наиболее важных для патогенеза глиом протеинкиназ, при этом было показано, что протеинкиназа Cα может выступать в роли дополнительного молекулярного фактора, наряду с ПК Mζ формирующего профиль функциональной активности различных клеточных кластеров. В целом наши результаты могут стать основой для разработки новых персонализированных подходов к диагностике и лечению глиом головного мозга.
Исследование выполнено при финансовой поддержке РФФИ в рамках научного проекта № 18-29-01034 мк.



