Ишемическая болезнь сердца (ИБС) является одной из ведущих медико-социальных проблем мирового и национального здравоохранения, имея под собой не только высокий уровень развития сердечно-сосудистых осложнений, инвалидизации и смертности, но и прогрессивно растущие социально-экономические последствия. Последние десятилетия ознаменовались успехом в профилактике и лечении данного заболевания, немалая роль которого принадлежит широкому использованию интервенционных интракоронарных вмешательств – коронарной ангиопластики и стентирования [1]. Эндоваскулярные методы лечения в большинстве случаев обеспечивают положительные клинико-ангиографические результаты у больных острыми и хроническими формами ИБС. В то же время все большую долю в пуле коронарных пациентов стали занимать сопутствующий сахарный диабет (СД) 2 типа и метаболический синдром. Ассоциация ИБС и СД 2 типа характеризуется быстро прогрессирующим диффузным многососудистым атеросклеротическим поражением коронарного русла, с большей частотой развития хронических окклюзий, фатального и нефатального инфаркта миокарда и смерти [5]. Указанные особенности явились первоначальным основанием преимущественного использования коронарного шунтирования (КШ) в качестве реваскуляризационной терапии у данной группы пациентов, что подтверждено данными мета-анализа 10 рандомизированных контролируемых исследований, в ходе которого сравнивались КШ и баллонная ангиопластика с имплантацией голометаллических стентов (ГМС) [2]. Меньшая эффективность ГМС была обусловлена развитием внутристентовых стенозов, лежавших в основе рецидива ИБС [2]. Внедрение в практику стентов с лекарственным покрытием (СЛП), цитостатическое покрытие которых подавляет клеточную пролиферацию в месте имплантации, обеспечило достоверное снижение частоты указанных осложнений и необходимости повторных вмешательств в отдаленном периоде в случае сочетания ИБС с СД 2 типа при отсутствии влияния, как казалось, на смертность и инфаркт миокарда (ИМ) [3]. Ряд мета-анализов последних лет показал сопоставимые результаты при применении ангиопластики с использованием СЛП в сравнении с КШ [4,7,8]. В то же время замедление нормальной эндотелизации эндопротеза вследствие цитостатических свойств лекарственного покрытия и возможные тромбогенные свойства полимера увеличивают риск развития поздних тромботических коронарных осложнений, несмотря на снижение частоты повторных реваскуляризаций. Анализ клинических и морфологических причин поздних коронарных осложнений показал, что факторами риска неблагоприятного прогноза могут быть прекращение приема пациентами двойной антиагрегантной терапии, а также различные клинические состояния, способствующие гиперкоагуляции (сахарный диабет, почечная недостаточность, низкая фракция выброса и др.) [6,9]. Тем не менее выявление таких факторов по-прежнему остается актуальной проблемой, а относительно продолжительности приема двойной антиагрегантной терапии при различных сопутствующих заболеваниях нет единого мнения. Помимо этого, накопление отдаленных наблюдений показало, что СЛП в некоторых клинических ситуациях не обеспечивают эффективное подавление гладкомышечной пролиферации и снижения частоты развития рестеноза. В связи с этим по-прежнему остается актуальным статистический анализ с целью выявления факторов, увеличивающих вероятность развития рестеноза и негативно влияющих на отдаленный прогноз после коронарного стентирования.
Цель исследования: изучить отдаленные результаты коронарного стентирования и их предикторы у больных ИБС в сочетании с СД 2 типа.
Материалы и методы: в исследование были включены 172 пациента после перенесенной чрескожной коронарной ангиопластики, в ходе которой было проведено стентирование коронарных артерий. Они были распределены на 2 группы. В основную группу включено 103 больных с ИБС в сочетании с СД 2 типа (мужчин – 72, женщин – 31, средний возраст – 69,25±0,97 года). Анамнез СД 2 типа составлял от 0 до 18 лет, имея среднюю продолжительность около 9 лет. 43 (42 %) пациента находились на инсулинотерапии, остальные получали терапию пероральными антидиабетическими препаратами в виде двух- и однокомпонентной терапии. Группу сравнения составили 69 пациентов с ИБС без нарушений углеводного обмена (мужчин – 55, женщин – 14, средний возраст – 62,70±1,40 года). Критериями исключения из исследования были непереносимость АСК и/или клопидогреля; эрозивно-язвенные поражения желудочно-кишечного тракта в анамнезе; КШ в анамнезе; геморрагический синдром в анамнезе; обширное оперативное вмешательство в течение последнего месяца перед коронарным стентированием; количество тромбоцитов менее 100·109 л-1; концентрация гемоглобина менее 100 г/л; наличие острой патологии или обострения/высокой активности хронической патологии, в том числе онкологической.
В структуре обследованных, вошедших в основную группу, наблюдались нестабильная и стабильная стенокардия у 31 (30,4 %) и 50 человек (49,0 %) соответственно, не Q и Q-инфаркт миокарда у 15 (14,7 %) и 6 (5,9 %) соответственно, при этом у 13 (13 %) пациентов был отмечен рестеноз ранее имплантированного стента. В группе лиц с ИБС без нарушения углеводного обмена также преобладали пациенты с нестабильной и стабильной стенокардией – 26 (37,7 %) и 28 (40,6 %) соответственно, а не Q и Q-инфаркты миокарда наблюдались у 5 (7,2 %) и 10 (14,5 %) больных.
Всем пациентам в обеих группах выполнены исследования липидного спектра крови, мозгового натрийуретического пептида (BNP), рассчитана рСКФ по MDRD (таблица 1), а также проведена селективная коронарография (СКГ) перед интракоронарным интервенционным вмешательством, через 6 месяцев, на 1, 2, 3 и 4 годы. На основании данных исходной СКГ рассчитывался показатель шкалы SyntaxScore, который составил 13 [7;18] баллов в первой группе и 12 [7;16] баллов во второй (p=0,14).
Таблица 1
Исследуемые исходные показатели крови ( M ± m ), Me [25 %; 75 %]
|
Показатель |
1-я группа ( n = 103 ) |
2-я группа ( n = 69 ) |
p |
|
ОХС, ммоль/л |
5,26 [4,67;6,23] |
4,76[3,9;5,64] |
0,37 |
|
ХС ЛПВП, ммоль/л |
1,2±0,06 |
1,4±0,06 |
0,027 |
|
ХС ЛПНП, моль/л |
2,6±0,2 |
2,8±0,2 |
0,42 |
|
ТГ, ммоль/л |
1,65 [1,18;2,45] |
1,53[1,16;2,19] |
0,470 |
|
BNP, пг/мл |
164,4±22,05 |
121,1±19,9 |
0,010 |
|
рСКФ по MDRD (мл/мин/1,73 м2) |
55,8±2,9 |
84,8±4,6 |
0,001 |
Перед коронарной ангиопластикой и стентированием все пациенты получали нагрузочную дозу АСК (Aspisol®, Bayer Vital GmbH, ФРГ) 500 мг внутривенно и клопидогреля (Плавикс®, Sanofi Pharma Bristol-Mayers Squibb SNC, Франция) 600 мг внутрь. Интраоперационно использовался нефракционируемый гепарин 70 ЕД/кг внутривенно болюсно. 8 (7,8 %) пациентов основной группы и 6 (8,7 %) больных группы контроля в день проведения стенторования коронарных артерий получали абциксимаб (РеоПро®, Lilly, Швейцария; производитель Hospira Inc., США); упаковщик Cilag, Швейцария). Внутривенно 0,25 мг/кг болюсно (за 10–60 мин до коронарной ангиопластики), а затем инфузионно, со скоростью 10 мкг/мин в течение 12 часов. Всего пациентам в основной группе имплантировано 215 стентов (2,15±0,13), из них – 132 (61,4 %) стенты длиной менее 20 мм, которые были установлены 44 больным (42,7 %). Количество стентов длиной более 20 мм составило 83 (38,6 %), они были имплантированы 59 пациентам (57,3 %). В группе сравнения было имплантировано 166 стентов (2,41±0,2), из них 110 (66,3 %) – стенты длиной менее 20 мм, которые были имплантированы 30 больным (43,5 %). Количество стентов длиной более 20 мм составило 56 (33,7 %), они были имплантированы 39 пациентам (56,5 %). Не выявлено достоверных различий в среднем количестве установленных стентов между группами, при этом в группе сравнения достоверно чаще имплантировались стенты длиной менее 20 мм (χ2=3,65, p=0,05), в то время как у пациентов с ИБС в сочетании с СД 2 типа преобладали стенты длиной более 20 мм (χ2=27, p=0,0001). В обоих группах преобладали СЛП (79,6 % vs 75,4 %): сиролимус-покрытые (Cypher-Cordis (Johnson & Johnson, США) и Orsiro (Biotronik, ФРГ)), эверолимус-покрытые (Xience V и Xience Prime (Abbott Vascular, США), Promus и Taxus Element (Boston Scientific, США)); зотаролимус-покрытые (Resolute Integrity (Medtronic, США)). В качестве голометаллических стентов использовались PRO-Kinetic (Biotronik, ФРГ). Пациенты после коронарного стентирования в течение 12 месяцев (в случае СЛП) или 1 месяца (в случае ГМС) получали двойную дезагрегантную терапию АСК (Тромбо АСС®, Lannacher Heilmittel, Австрия) 100 мг/сутки и клопидогрель 75 мг/сутки (89 (86,4%) vs 54 (78,3 %) человек) или празугрел (Эффиент®, Eli Lilly, США) (11 (10,7%) vs 15 (21,7%) человек) 10 мг/сутки или тикагрелор (Брилинта®, AstraZeneca АВ, Швеция) 90 мг/сутки (4 (3,9 %) vs 0). Длительность наблюдения в среднем составила 4 года, в ходе которого фиксировались большие кардио- и цереброваскулярные (смерть, сердечно-сосудистая смерть, нефатальные инфаркт миокарда и инсульт, нестабильная стенокардия, нарастание класса тяжести стабильной стенокардии) и ангиографические (тромбоз и рестеноз ранее установленного стента, появление нового стеноза коронарных артерий) события. Полученные в ходе исследования результаты обрабатывались статистически общепринятыми методами статистики на компьютере IBM PC при помощи пакета прикладных программ для обработки медицинской и биологической информации «SТАTISTICA 10.0» (StatSoft Inc., США). При нормальном распределении переменных для определения различий между двумя независимыми группами использовался непарный t-критерий Стьюдента, а при непараметрическом – критерий Вилкоксона – Манна – Уитни. Различие между долями оценивали при помощи критерия χ2 в таблицах сопряженности 2×2. Для определения связи между демографическими, клиническими, лабораторными показателями использовались методы корреляционного анализа для параметрических и непараметрических критериев – критерии Пирсона и Спирмена соответственно. Достоверными считали различия и корреляции при p < 0,05. Анализ распределения промежутка времени до больших кардио- и цереброваскулярных событий в отдаленном периоде определяли при помощи кривых выживаемости по Каплану – Майеру. Анализ рисков (ожидаемой вероятности) развития отдаленных исходов эндоваскулярного лечения ИБС проводился при помощи вычисления абсолютного риска (частот развития событий в экспонированной и контрольной группах), атрибутивного и относительного риска).
Результаты и их обсуждение: наблюдаемые отдаленные исходы в сравниваемых группах пациентов отражены в таблице 2.
Таблица 2
Сравнительная оценка отдаленных исходов эндоваскулярного лечения ИБС у больных в группах сопутствующего СД 2 типа и без него
|
Показатель |
ИБС+СД 2 типа (n = 103) |
ИБС (n = 69) |
Относительный риск (OR) (95% ДИ) |
р |
|
Смерть, человек (%) |
5 (4,8%) |
2 (2,9%) |
1,71 (0,32; 9,07) |
<0,0001 |
|
Q-ИМ, человек (%) |
0 |
1 (1,4%) |
1,01 (0,99; 1,04) |
<0,0001 |
|
не-Q-ИМ, человек (%) |
3 (2,9%) |
4 (5,8%) |
0,49 (0,11; 2,25) |
<0,0001 |
|
Всего ИМ, человек (%) |
3 (2,9%) |
5 (7,2%) |
0,38 (0,09; 1,66) |
<0,0001 |
|
Нестабильная стенокардия, человек (%) |
30 (29,1%) |
9 (13,4%) |
2,33 (1,02; 5,33) |
0,0001 |
|
Нарастание функционального класса стабильной стенокардии напряжения, человек (%) |
17 (16,5%) |
8 (11,8%) |
1,48 (0,60; 3,65) |
<0,0001 |
|
Инсульт, человек (%) |
7 (6,8%) |
1 (1,5%) |
4,96 (0,60; 41,23) |
<0,0001 |
|
Тромбоз ранее установленного стента, человек (%) |
0 |
1 (1,5%) |
1,02 (0,99; 1,05) |
<0,0001 |
|
Рестеноз ранее установленного стента, человек (%) |
16 (15,5%) |
6 (8,7%) |
1,76 (0,65; 4,79) |
<0,0001 |
|
Возникновение нового стеноза, человек (%) |
30 (30,0%) |
12 (17,4%) |
1,94 (0,91; 4,14) |
0,0001 |
|
Хороший ангиографический результат, человек (%) |
54 (52,4%) |
23 (33,3%) |
2,2 (1,17; 4,15) |
0,2068 |
|
КШ, человек (%) |
1 (1%) |
2 (2,9%) |
0,32 (0,03; 3,69) |
<0,0001 |
|
Большие кровотечения, человек (%) |
1 (1%) |
0 |
0,99 (0,97; 1,01) |
<0,0001 |
В основной группе смерть наблюдалась к 4 году наблюдения у 5 (4,8 %) человек в основной группе (из них сердечно-сосудистая смерть – у 3 (2,9 %) пациентов), и 2 (2,9 %) больных в группе сравнения, из них у 1 (1,45 %) она была кардиоваскулярной природы (p<0,001). Риск развития смерти достоверно выше у больных с сопутствующим СД 2 типа, подвергнувшихся коронарной ангиопластике и стентированию (атрибутивный риск (АР) составил 1,9 %, а относительный риск (ОР) – 1,71). При этом сопутствующий СД 2 типа сопровождается увеличением АР и ОР появления новых стенозов (рисунок 1) и рестенозов ранее установленных коронарных стентов (12,6 % и 1,94, 6,8 % и 1,76 соответственно), что сопровождалось как нарастанием функционального класса стабильной стенокардии (АР – 4,7 %, ОР – 1,48), так и большей частотой развития нестабильной стенокардии (АР – 15,7 %, ОР – 2,33).
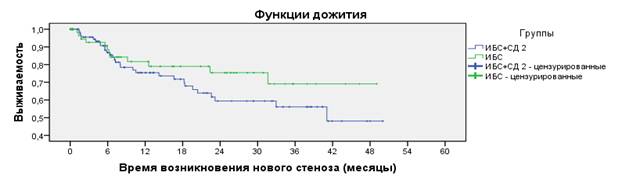
Рис.1. Сравнительная динамика развития de novo стенозов коронарного русла у больных с сопутствующим СД 2 типа и без него
В то же время у больных с ассоциацией ИБС и СД 2 типа, подвергнувшихся интракоронарному вмешательству, в 4-летнем отдаленном периоде значимо реже наблюдалось развитие нефатального ИМ (АР – -4,3 %, ОР – 0,38) и не встретился поздний тромбоз ранее установленного стента (таблица 2).
Корреляционный анализ показал зависимость развития стенозирующего процесса ранее неизмененых коронарных артерий у больных с сопутствующим СД 2 типа в течение ближайших 4 лет после ангиопластики и стентирования от исходного уровня триглицеридов крови (R=0,2, p<0,05) и уровня рСКФ (R=-0,25, p<0,05). Развитие рестеноза ранее установленных стентов положительно коррелирует с исходным количеством пораженных коронарных артерий и наличием кальциноза в них (R=0,69 и 0,26 соответственно, p<0,05), а также уровнем тропонина I через 24 часа после интракоронарного вмешательства (R=0,37, p<0,05). Несомненна роль рестеноза в развитии нестабильной стенокардии и ИМ в отдаленном периоде у данной группы пациентов (R=0,31 и 0,26 соответственно, p<0,05), в то время как вновь образованные ангиографически значимые стенозы лежат в основе нестабильной стенокардии и нарастания функционального класса стабильной стенокардии напряжения (R=0,35 и 0,24 соответственно, p<0,05). К предикторам развития нефатального ИМ в течение ближайших 4 лет относятся снижение фракции выброса левого желудочка (R= -0,42, p<0,05), развитие острого и подострого тромбоза стента при стентировании (R=0,43, p<0,05), хроническая окклюзия коронарных артерий (R=0,23, p<0,05), отсутствие использования β-адреноблокаторов в плановой терапии основного заболевания и его осложнений (R=-0,32, p<0,05).
К предикторам развития смерти в течение ближайших 4 лет следует отнести исходное повышение уровня BNP (R=0,48, p<0,05), жизнеопасные нарушения ритма в анамнезе, потребовавшие длительной терапии амиодароном (R=0,38, p<0,05), повышение параметров индуцированной арахидоновой кислотой и АДФ агрегации тромбоцитов (R=0,32 и 0,28 соответственно, p<0,05), наличие ИМ в анамнезе (R=0,28, p<0,05), исходных тахикардии в покое и выявлением тропонина I перед эндоваскулярным вмешательством (R=0,22 и 0,21 соответственно, p<0,05).
При анализе влияния адекватной сопутствующей антидиабетической терапии на отдаленные исходы эндоваскулярного лечения ИБС у больных с СД 2 типа установлено, что большинство классов используемых препаратов, включая инсулин, не оказывают какого-либо воздействия на них, за исключением более частого развития нестабильной стенокардии в случае применения ситаглиптина (R=0,37, p=0,036) (ОР, 4,09, 95% ДИ, 1.01-16.57).
Заключение
Наличие сопутствующего сахарного диабета 2 типа утяжеляет отдаленный прогноз у больных ИБС, подвергнувшихся эндоваскулярной терапии за счет прогрессирования многососудистого атеросклеротического поражения коронарных артерий, приводящее к развитию нестабильной стенокардии и нарастания функционального класса стабильной стенокардии напряжения. С учетом выявленных предикторов неблагоприятного прогноза значимое место во вторичной профилактике неблагоприятного клинико-ангиографического исхода и сердечно-сосудистых осложнений в данной группе пациентов должны занимать адекватные антитромбоцитарная и антиишемическая терапия с использованием высокоселективных β-адреноблокаторов в структуре последней, а также коррекция гипертриглицеридемии.
Рецензенты:
Варварина Г.Н., д.м.н., профессор, зав. кафедрой пропедевтики внутренних болезней, ГБОУ ВПО «Нижегородская государственная медицинская академия» Минздрава России, г. Нижний Новгород;
Королёва Л.Ю., д.м.н., профессор кафедры госпитальной терапии им. В.Г. Вогралика, ГБОУ ВПО «Нижегородская государственная медицинская академия» Минздрава России, г. Нижний Новгород.
Библиографическая ссылка
Калугина О.Ю., Носов В.П. ОТДАЛЕННЫЕ РЕЗУЛЬТАТЫ ЭНДОВАСКУЛЯРНОГО ЛЕЧЕНИЯ У ПАЦИЕНТОВ С ИШЕМИЧЕСКОЙ БОЛЕЗНЬЮ СЕРДЦА В СОЧЕТАНИИ С САХАРНЫМ ДИАБЕТОМ 2 ТИПА // Современные проблемы науки и образования. – 2014. – № 5. ;URL: https://science-education.ru/ru/article/view?id=14762 (дата обращения: 23.04.2024).



