Сахарный диабет (СД) является актуальной медико-социальной проблемой современного общества. По данным международной федерации СД за период 1985 года по 2015 количество больных СД во всем мире увеличилось с 30 до 285 миллионов. В России болеют примерно 6% населения, что составляет 9,6 миллионов человек [9]. Заболеваемость СД растет, что приводит к формированию множества осложнений, сокращению качества жизни, инвалидизации. Современная медикаментозная терапия СД, несмотря на достижения последних лет, не способна препятствовать прогрессированию клинических проявлений СД и развитию его осложнений. Поэтому поиск и разработка новых подходов к лечению СД остается актуальной проблемой современной диабетологии.
В последние годы, внимание исследователей привлекают аутологичные клетки костного мозга (ККМ), в частности мультипотентные мезенхимальные стромальные клетки (ММСК) костного мозга, обладающие набором уникальных свойств, которые могут использоваться для клеточной терапии СД [9]. ККМ обладают высокой пластичностью, способны дифференцироваться в клетки поврежденных органов и секретировать ростовые факторы и цитокины, тем самым способствовать регенерации поврежденных органов и тканей. Успешность терапевтического эффекта трансплантированных клеток при этом зависит не только от способности стволовых клеток восстанавливать поврежденные ткани, но и от миграции в очаг поражения [5]. Изучение миграции и распределения клеток после трансплантации является важным этапом при разработке клеточной терапии различных социально-значимых заболеваний, к числу которых относится СД. При этом результаты исследователей по оценке миграции клеток после их введения при СД немногочисленны и противоречивы.
Целью данного исследования является проведение сравнительного анализа миграционной активности популяций клеток костного мозга в лимфоидные и нелимфоидные органы в норме и на модели экспериментального сахарного диабета, а также возможности использования ККМ и ММСК для заместительной регенеративной терапии экспериментального сахарного диабета.
Материал и методы исследования
В работе использовались самки и самцы мышей линии С57ВL/6 и самцы мышей линии C57BL/6-Tg (UBC-GFP) 30Scha/J, в возрасте 8–12 недель. Линия мышей C57BL/6-Tg (UBC-GFP) 30Scha/J имеет ген, в котором находится молекула GFP – белка способная к видимой флуоресценции, что позволяет визуализировать клетки в органах реципиента. Животные содержались в индивидуальных клетках и находились на стандартной сбалансированной диете в виварии SPF-стандарта ИЦиГ СО РАН. Эксперименты проводили в соответствии с соблюдением принципов Хельсинкской декларации BMA (2000); с соблюдением принципов гуманности, изложенных в директивах Европейского сообщества (86/609/ЕЕС) и в соответствии с «Правилами проведения работ с использованием экспериментальных животных».
Экспериментальная модель сахарного диабета создавалась путем внутрибрюшинного введения раствора стрептозотоцина 100 мг/кг (Sigma, США) в 0,5 мл цитратного буфера однократно самкам-реципиентам мышей линии C57Bl6 8-12 недельного возраста [4]. О развитии сахарного диабета судили по уровню глюкозы в крови, который измеряли каждые 2-3 дня до момента достижения высоких значений на протяжении 3 последних измерений глюкозооксидазным методом венозной крови хвостовой вены. Для исследования брали животных, у которых уровень глюкозы в крови был выше 12 Ммоль/л. Выделение и культивирование популяций клеток проводили по стандартным методикам. ККМ выделяли из бедренных костей самцов С57ВL/6 и C57BL/6-Tg (UBC-GFP) 30 Scha/J, в стерильных условиях. Клетки костного мозга мышей-доноров суспендировали в среде RРМI-1640 (Биолот, СПб) при комнатной температуре. Для получения ММСК ядросодержащие ККМ мышей-самцов C57Bl/6 и C57BL/6-Tg (UBC-GFP) 30Scha/J культивировали в пластиковых флаконах (TPP, Швейцария) в среде DMEM (Биолот, СПб), дополненной 100 мкг/мл гентамицина сульфата (Дальхимфарм, Россия), 2 мM L-глютамина (ICN, США) и 15 % FCS (фетальная телячья сыворотка; Hyclone, США) при 37°С в атмосфере 5% СО2. Через 48 часов неприкрепленные к пластику клетки удаляли, а прилипающую фракцию клеток культивировали до получения конфлюэнтного монослоя. Снятие ММСК при пассировании осуществляли с использованием 0,25% раствора трипсина/0,02% раствора ЭДТА. В экспериментах использовали ММСК от 2-4 пассажа [9]. Клеточные популяции были трансплантированы интактным самкам – реципиентам мышей С57ВL/6 (ММСК; ККМ интактные) и самкам-реципиентам мышей С57ВL/6 с экспериментальным сахарным диабетом (ММСК; ККМ эксперимент) в хвостовую вену в концентрации 5х105 клеток/мл/мышь, через определенные временные интервалы (1 час, 1 сутки, 7 дней, 14 дней, 20 дней и 30 дней). Животных выводили из эксперимента и забирали органы для исследования миграции и распределения донорских Y-позитивных клеток в органах и тканях самок - реципиентов. Миграцию и распределение донорских Y-позитивных клеток исследовали методом полимеразной цепной реакции (ПЦР). Цельную ДНК выделяли из замороженных органов при помощи стандартной обработки додецилсульфатом натрия (SDS) с протеиназой К, методом высаливания. Полученную ДНК растворяли в воде и замораживали при температуре –20оС [1]. Амплификация образцов ДНК проводилась в реакционной смеси, содержащей мышиные праймеры, специфичные для Y-хромосомы [1]. Все образцы приводили к единой концентрации. Условия ПЦР: денатурация при 95 оС в течение 3 мин, затем 37 циклов по 50 с при 94 оС, 50 с при 52 оС и 50 с при 72 оС. Далее проводили ПЦР, используя вложенные праймеры [1]. В результате амплификации был получен фрагмент 320 пар оснований. В качестве позитивного и негативного контроля использовали ткань интактных самцов и самок соответственно. Полуколичественное определение маркера в органах проводили при помощи программного обеспечения Quantity One в денситометре Geldok (Bio-Rad, США) в единицах оптической плотности ампликонов электорофореграммы. Изменение структуры поджелудочной железы после трансплантации клеток ККМ и ММСК на модели сахарного диабета проводили с использованием световой микроскопии. Для гистологического исследования материал фиксировали в 10% нейтральном формалине. Срезы поджелудочной железы готовили из парафиновых блоков по стандартной методике, окрашивали гематоксилином и эозином. Анализ проводили на микроскопе (Axio) (Zeiss, Германия) с использованием программного обеспечения для анализа видеоизображения AxioVision (Zeiss, Германия).
Для визуализации миграции и распределения донорских GFP – клеток на срезах поджелудочной железы после их внутривенной трансплантации реципиентам C57BL/6 с экспериментальным сахарным диабетом, была использована флуоресцентная микроскопия. Срезы поджелудочной железы были сделаны на микротоме - криотоме (Zeiss, Германия), толщиной 5-7 мкм. Готовые срезы были фиксированы, с последующей обработкой судановым черным (Sudan B), для устранения аутофлюоресценции при исследовании GFP – клеток.
Статистическая обработка результатов проводилась при помощи программы Statistica 6,0 (StatSoft, США), достоверность различий оценивали по критериям Манна-Уитни (в независимых группах), при p <0,05, в сравнении между интактной и экспериментальной группами.
Результаты
На первом этапе была произведена оценка влияния введения общей популяции ККМ и ММСК на уровень глюкозы у мышей с индуцированным СД. Как видно на рисунке 1, введение как ККМ, так и ММСК после устойчивого формирования гипергликемии приводит к постепенному снижению уровня глюкозы в крови до нормы к 30 суткам после введения клеток (ККМ - 5,3 mmol/L; ММСК - 7,8 mmol/L). В группе контрольных животных без введения клеток в эти сроки гипергликемия оставалась высокой (более 41 mmol/L).
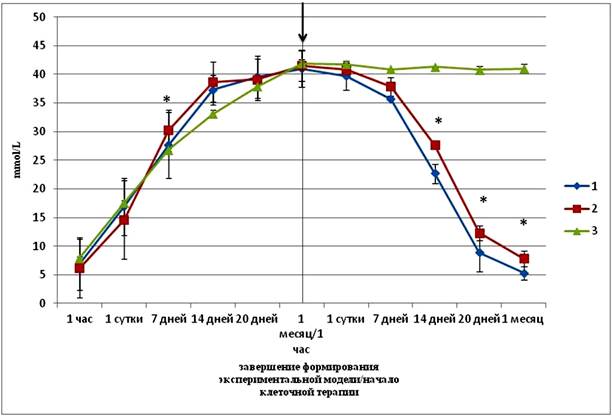
Рис. 1. Результаты исследования уровня глюкозы крови у самок – реципиентов мышей С57ВL/6 до и после проведения клеточной терапии
По оси ординат – уровень глюкозы крови у самок - реципиентов. По оси абсцисс представлены временные интервалы исследования уровня глюкозы в крови самок – реципиентов через 1 час, 1 сутки, 7 дней, 14 дней, 20 дней, 1 месяц до и после трансплантации клеток. 1 - ( ) - группа самок – реципиентов с экспериментальным сахарным диабетом, которым внутривенно трансплантировались ККМ. 2 - (
) - группа самок – реципиентов с экспериментальным сахарным диабетом, которым внутривенно трансплантировались ККМ. 2 - ( ) – группа самок – реципиентов с экспериментальным сахарным диабетом, которым внутривенно трансплантировались ММСК. 3 – (
) – группа самок – реципиентов с экспериментальным сахарным диабетом, которым внутривенно трансплантировались ММСК. 3 – (![]() ) - группа самок (контроль) – реципиентов с экспериментальным сахарным диабетом, которым не трансплантировались клетки.
) - группа самок (контроль) – реципиентов с экспериментальным сахарным диабетом, которым не трансплантировались клетки.
Примечание: Данные представлены как М±δ. * - значения достоверны по сравнению с контролем, при р <0,05.
Для того чтобы провести анализ миграции трансплантированных клеток, была исследована временная динамика распределения Y-позитивных клеток доноров в органах реципиентов. Мы сравнили распределение введенных ККМ и ММСК доноров мышей-самцов в организме самок - реципиентов мышей с экспериментальным СД и у интактных животных.
На рисунке 2 показано, что уже через 1 час после введения ККМ и ММСК доноров-самцов определяются в поджелудочной железе у самок – реципиентов, причем при СД клетки сильнее мигрировали в поджелудочную железу, чем у интактных животных.
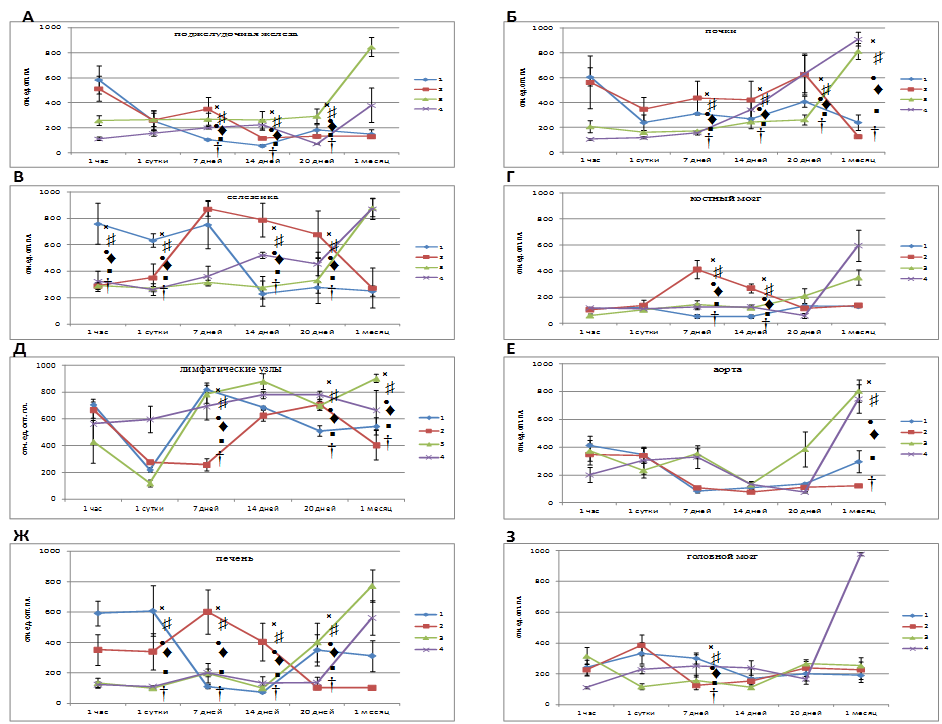
Рис. 2. Результаты сравнительного исследования динамики миграции и распределения ККМ и ММСК у интактных самок – реципиентов мышей С57ВL/6 и самок реципиентов мышей С57ВL/6 с экспериментальным сахарным диабетом
По оси ординат - относительные единицы оптической плотности, выражающие количественное содержание маркерного гена трансплантированных клеток в образцах. По оси абсцисс – представлены временные интервалы исследования миграции и распределения трансплантированных клеток 1 –ККМ ( ) трансплантированные самкам – реципиентам с экспериментальной моделью сахарного диабета; 2 - ММСК (
) трансплантированные самкам – реципиентам с экспериментальной моделью сахарного диабета; 2 - ММСК ( ) трансплантированные самкам – реципиентам с экспериментальной моделью сахарного диабета; 3 – ККМ (
) трансплантированные самкам – реципиентам с экспериментальной моделью сахарного диабета; 3 – ККМ ( ) – трансплантированные интактным самкам – реципиентам; 4 – ММСК ( ) - трансплантированные интактным самкам – реципиентам.
) – трансплантированные интактным самкам – реципиентам; 4 – ММСК ( ) - трансплантированные интактным самкам – реципиентам.
Примечания: Данные представлены как М±δ. Обозначены статистически значимые отличия от величин соответствующих показателей относительных единиц оптической плотности: интактных животных после трансплантации им ККМ ( ̽– при p < 0,05), от животных с экспериментальным сахарным диабетом после трансплантации им ККМ.
Интактных животных после трансплантации им ККМ ( ♯– при p < 0,05), от животных с экспериментальным сахарным диабетом после трансплантации им ММСК.
Интактных животных после трансплантации им ККМ ( •– при p < 0,05), от интактных животных после трансплантации им ММСК.
Животных с экспериментальным сахарным диабетом после трансплантации им ККМ ( ♦- при p < 0,05), от животных с экспериментальным сахарным диабетом после трансплантации им ММСК.
Животных с экспериментальным сахарным диабетом после трансплантации им ККМ ( ▪– при p < 0,05), от интактных животных после трансплантации им ММСК.
Животных с экспериментальным сахарным диабетом после трансплантации им ММСК ( † – при p < 0,05), от интактных животных после трансплантации им ММСК.
Через 1 сутки регистрируется снижение уровня меченных ККМ и ММСК у животных с СД, далее изменения носят волнообразный характер и к 20-30 дню введенные клетки определяются на невысоком уровне в поджелудочной железе. У интактных животных происходит постепенное накопление меченых клеток в поджелудочной железе, причем уровень ККМ является наиболее высоким, выше чем при трансплантации ММСК. В лимфатических узлах реципиентов через 7 дней и 1 месяц количество ККМ было статистически значимо выше, чем количество ММСК как в норме, так и при СД. В селезенке количество ККМ было статистически значимо выше, чем ММСК через 1 час и 1 сутки после их трансплантации. Две популяции введенных клеток костного мозга мигрировали и в костный мозг, печень, почки, головной мозг, определялись в аорте на разных сроках наблюдения с волнообразным изменением уровня регистрируемых клеток. Уровень миграции ККМ и ММСК у интактных животных практически во всех органах был выше, чем при СД. В печени количество ККМ было статистически значимо выше, чем ММСК через 1 сутки и 20 дней после их трансплантации как у интактных животных, так и при СД. В почках количество ККМ было достоверно выше, чем ММСК через 1 месяц после их трансплантации. В головном мозге количество ККМ было достоверно выше, чем ММСК через 7 дней после их трансплантации. В аорте количество клеток костного мозга было статистически значимо выше, чем мультипотентных мезенхимальных стромальных клеток через 1 месяц после их трансплантации. Таким образом, ККМ у реципиентов с экспериментальным СД циркулируют по кровотоку, попадая во все органы и ткани, и остаются там в течение 1 месяца после трансплантации. Трансплантированные ККМ и ММСК мигрируют и распределяются по всем органам в организме реципиента, как в норме, так и при экспериментальном СД.
Проведенное нами гистологическое исследование (рис. 3 и 4) подтверждает идею об изменении структуры поджелудочной железы у самок - реципиентов с экспериментальным сахарным диабетом после трансплантации им донорских клеток в результате миграции трансплантированных донорских клеток в область повреждений.
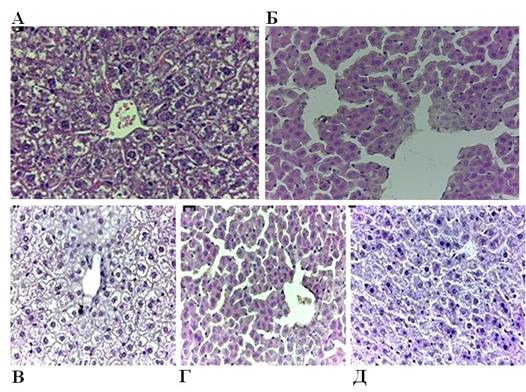
Рис. 3. Результаты гистологического исследования (световая микроскопия) временного изменения структуры поджелудочной железы у самок – реципиентов С57ВL/6 с экспериментальным сахарным диабетом после трансплантации им донорских клеток ККМ.
Ув.х400; окраска Гематоксилин- Эозин.
Примечания:
А – срез островка поджелудочной железы интактной самки – реципиента.
Б - срез островковой зоны поджелудочной железы самки – реципиента с экспериментальным сахарным диабетом без трансплантации донорских клеток.
В, Г, Д – срез островка поджелудочной железы самки – реципиента с экспериментальным сахарным диабетом после трансплантации донорских клеток через 1 час, 7 дней и 1 месяц.
Как видно на рисунке 3(Б), имеются отчетливые повреждения структуры поджелудочной железы после индуцирования СД введением стрептозотоцина. После трансплантации донорских клеток структурные изменения менее значительные, наблюдается восстановление структуры поврежденного органа. На рисунке 4 на срезах поджелудочной железы самок-реципиентов с СД видны яркие, светящиеся регионы — это множественные скопления GFP-меченных клеток мышей линии C57BL/6-Tg (UBC-GFP) 30Scha/J.
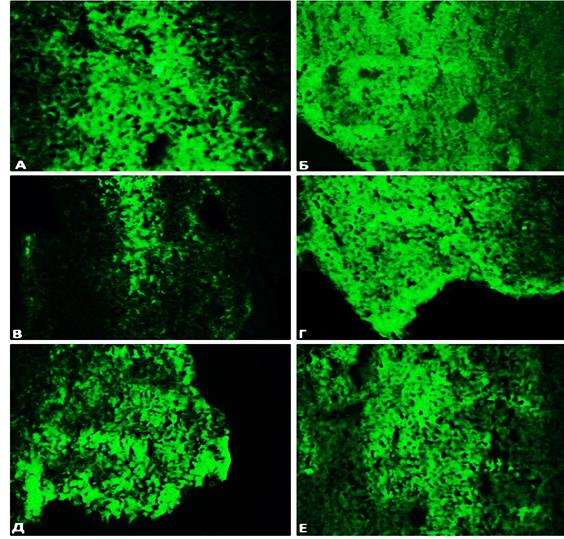
Рис. 4. Флуоресцентная микроскопия срезов поджелудочной железы у самок – реципиентов С57ВL/6 с экспериментальным сахарным диабетом после трансплантации им донорских клеток ККМ самцов линии C57BL/6-Tg (UBC-GFP) 30Scha/J.
Ув.х 200; окраска Судановым черным
Примечания: Яркие, светящиеся регионы - скопление трансплантированных клеток самцов-доноров линии C57BL/6-Tg (UBC-GFP) 30Scha/J.
А – срез поджелудочной железы на сроке 1 час после трансплантации донорских клеток.
Б – срез поджелудочной железы на сроке 1 сутки после трансплантации донорских клеток.
В - срез поджелудочной железы на сроке 7 дней после трансплантации донорских клеток.
Г - срез поджелудочной железы на сроке 14 дней после трансплантации донорских клеток.
Д - срез поджелудочной железы на сроке 20 дней после трансплантации донорских клеток.
Е - срез поджелудочной железы на сроке 1 месяц после трансплантации донорских клеток.
Таким образом, исследованные донорские клетки мигрируют во все сроки после их трансплантации, накапливаются и распространяются в поврежденной области, что подтверждено ранее полимеразной цепной реакцией. Очевидно, что донорские клетки мигрируют в патологический очаг, восстанавливая при этом структуру поврежденного органа.
Обсуждение
Наше исследование показало, что сингенная трансплантация как неразделенной популяции ККМ, так и ММСК приводила к значительному снижению уровня глюкозы крови мышей с индуцированным стрептозотоцином СД причем более значительное снижение уровня глюкозы в крови обнаружено после введения ККМ. При этом мнения разных авторов о механизмах заместительной клеточной терапии при сахарном диабете являются противоречивыми [3, 7, 10,]. Широко обсуждается вопрос о наиболее предпочтительном клеточном материале для трансплантации. Подавляющее большинство авторов рассматривают ММСК в качестве идеального кандидата среди других стволовых клеток для индуцированной дифференцировки в островковые клетки поджелудочной железы. Причиной является наличие у ММСК высокой пластичности и низкой иммуногенности, хотя другие источники стволовых клеток также не отвергаются. В качестве других источников стволовых клеток рассматриваются неразделенная популяция ККМ, а также резидентные стволовые клетки поджелудочной железы. Обсуждаются механизмы участия клеточного микроокружения поджелудочной железы в индукции дифференцировки трансплантированных стволовых клеток в β-клетки островков Лангерганса [4,10]. Разными авторами были получены противоречивые результаты о дифференцировке стволовых клеток костного мозга в β-клетки островков Лангерганса. Одни авторы в своих работах утверждают об эффективности заместительной клеточной терапии для лечения сахарного диабета и обсуждают возможные механизмы [4,7] другие авторы напротив высказывают сомнения в возможности трансдифференцировки клеток костного мозга в β-клетки островков Лангерганса [3]. Указанные работы поддерживают мнение о том, дифференцировочные способности стволовых клеток костного мозга ограничены, а доля панкреатических β-клеток полученных из костного мозга in vivo, не существенна [2,8]. Указанные различия возможно связаны с особенностями применяемых методов исследования и клеточным материалом, используемым в ходе клеточной терапии СД. Одним из обсуждаемых механизмов действия трансплантированных клеток является паракринный механизм секреции ростовых, трофических факторов и цитокинов, которые способствуют регенерации β-клеток поджелудочной железы, окружающих их тканей у реципиентов [11]. Поврежденные клетки поджелудочной железы также секретируют большое количество растворимых биологически активных молекул, которые также оказывают влияние на регенерацию поджелудочной железы [6]. Проведенные исследования подтверждают, что во время регенерации секретируется большое количество панкреатических цитокинов, индуцирующих продукцию транскрипционных белков [11], которые способствуют дифференцировке стволовых клеток в инсулин продуцирующие клетки.
Не смотря на расхождения в механизмах действия пересаженных клеток и их влияния на ткани поджелудочной железы, работы большинства исследователей показали, что трансплантация ММСК значительно снижает уровень глюкозы в крови животных с индуцированным стрептозотоцином СД, что было связано некоторыми исследователями с повышенным образованием островков Лангерганса [10]. Использование меченых GFP ККМ и ММСК для трансплантации и проведение флуоресцентной микроскопии подтверждает их локализацию в поджелудочной железе, а увеличение числа островковых клеток указывает на регенерацию поджелудочной железы. При этом общий результат был более значимым в группе при введении неразделенной популяции ККМ по сравнению с введением ММСК, что возможно связанно с различием факторов роста, продуцируемых не только ММСК, но и другими популяциями костного мозга - гемопоэтическими и эндотелиальными стволовыми клетками, которые стимулируют резидентные β-клетки островков. Можно предположить существование клеточных механизмов заместительной клеточной терапии для лечения СД, которые основаны на увеличении массы и/или функции β-клеток, включают в себя слияние ММСК с β-клетками островков Лангерганса или транс-дифференцировку ММСК в β-клетки [2]. В основе альтернативного потенциального механизма лежит развитие нового островка посредством гуморальной стимуляции дифференцировочного потенциала резидентных стволовых клеток островков поджелудочной железы [2]. Противоречивые результаты подтверждают, необходимость дальнейших исследований для того, чтобы установить окончательные ответы о возможности использования разных популяций стволовых клеток для лечения СД. Принимая во внимание все имеющиеся в настоящее время результаты, мы можем ожидать, что СД возможно успешно лечить с использованием трансплантации стволовых клеток. Однако, вопросы, касающиеся миграции и пролиферации трансплантированных клеток требуют дальнейших исследований. Данная работа указывает на преимущества трансплантации неразделенной популяции клеток костного мозга по сравнению с другими типами клеток.
Выводы:
1. Проведение клеточной терапии экспериментального сахарного диабета ККМ и ММСК приводит к положительному клиническому эффекту – снижению уровня глюкозы крови.
2. ККМ и ММСК мигрируют во все исследуемые органы и определяются в них во все сроки после трансплантации, Y-позитивные клетки определяются в поджелудочной железе, лимфатических узлах, селезенке, костном мозге и головном мозге, аорте, печени, почках.
3. Интенсивность миграции и распределения трансплантированных клеток меняется в зависимости от органа и срока после введения.
4. Миграция неразделенной популяции ККМ в органы и ткани реципиентов с экспериментальным сахарным диабетом выше, чем ММСК.
5. Миграция и распределение клеток ККМ и ММСК в исследуемых органах через 1 месяц после трансплантации у интактных реципиентов выше, чем на модели экспериментального сахарного диабета.
Библиографическая ссылка
Миллер Т.В., Повещенко А.Ф., Лыков А.П., Повещенко О.В., Бондаренко Н.А., Петровская И.Ф., Завьялов Е.Л., Дементьева Е.В., Захарова И.С., Грицык О.Б., Шурлыгина А.В., Коненков В.И. СРАВНИТЕЛЬНЫЙ АНАЛИЗ МИГРАЦИОННОЙ АКТИВНОСТИ ПОПУЛЯЦИЙ КЛЕТОК КОСТНОГО МОЗГА В ЛИМФОИДНЫЕ И НЕЛИМФОИДНЫЕ ОРГАНЫ В НОРМЕ И НА МОДЕЛИ ЭКСПЕРИМЕНТАЛЬНОГО САХАРНОГО ДИАБЕТА // Современные проблемы науки и образования. 2016. № 2. ;URL: https://science-education.ru/ru/article/view?id=24375 (дата обращения: 21.04.2026).



