Цель исследования – разработка адаптированного к клинической практике неинвазивного метода оценки периферической вегетативной (автономной) регуляции синоатриального узла сердца с помощью РКГ для анализа ВСР при различных формах ИБС. Актуальность темы обусловлена необходимостью оценки нарушений регуляции сократительной деятельности сердца для ранней диагностики ИБС, приоритетной по распространённости, смертности и инвалидизации населения, а также в ответ на результаты широкомасштабных кооперативных программ профилактики ИБС (HF-ACTION, GOSPEL, HPS, RESPONSE, CVD PREVENTION IN CLINICAL PRACTICE- European Guidelines, 2016) [4; 5; 7; 8].
Материалы и методы. Для этой цели был разработан по гранту Федерального фонда СРМП аппаратно-программный комплекс (АПК) КАП-РК-01- «Микор» (Рег. удостоверение Федеральной службы по надзору в сфере здравоохранения ФС022б2005/2447-06) для высокоточной регистрации и анализа ВСР в сопоставлении со стандартными методами исследования. Получены 9 патентов РФ по устройствам для регистрации ритмокардиограмм (Ркг) и методам клинического анализа ВСР. В 2001 г. была создана лаборатория нейрокардиологии для РКГ-исследований. Выполнено 27 диссертаций для доказательства практической полезности РКГ, в том числе для оценки дизрегуляций СУ при ИБС [4; 5]. Уровень доказательности – В-1 для контролируемых открытых рандомизированных исследований. По теме автономных дизрегуляций СУ при сердечно-сосудистой патологии опубликовано 5 монографий, более 500 научных публикаций в России и за рубежом. РКГ имеет дискретизацию межсистолических интервалов 1000±3 Гц, такое же хранение в оперативной памяти и анализ той же точности волновой структуры изменений межсистолических RR-интервалов, регулирующих сокращения сердца. При болезнях изменения ВСР проявляются многовариантными, патогенетически обусловленными изменениями волновой структуры ВСР. Основой для получения диагностически значимой информации является анализ пейсмекерной функции СУ сердца, являющегося суперинтегральным образованием, откликающимся на любые экзогенные и эндогенные воздействия [1; 3; 6-9]. Представляемый метод отличается от физиологических разработок, поскольку таковые нуждаются в клинической проверке. Здесь представляется часть результатов этой работы. Создан новый подход в диагностике сердечно-сосудистых болезней, ориентированный на выявление многовариантных нарушений регуляции СУ [4]. Большинство сердечно-сосудистых болезней, в том числе ИБС, начинается с дизрегуляции хронотропной функции сердца. С её облигатным участием формируется и хроническая ИБС в результате нарушения нормальной перфузии тканей сердца. Основным регулятором быстрого, адекватного в норме изменения функций всех внутренних органов является вегетативная система [5-8]. Без её нарушений не обходится ни один патологический процесс. Ближе всего к симптомообразованию при болезни находятся периферические отделы автономной системы. Их изучение с помощью анализа ВСР при кардиоваскулярных болезнях и явилось патофизиологической основой для создания клинической РКГ [4; 5].
Для РКГ в кардиохирургии создана модификация АПК с мониторным режимом регистрации ВСР [3; 4]. В течение 5-9 лет были обследованы более 3 тысяч пациентов с ИБС. Из их числа по специальным критериям отобраны 534 больных с СтСт без клинических проявлений СН и нормальной фракцией выброса, ОКС был у 115, СН у 518 пациентов, КА ишемического генеза у 971, сочетанные формы ИБС были у 1406. Дооперационное исследование было у 256 больных ИБС, из них 123 пациентам проведена интервенционная реваскуляризация миокарда методом коронарного шунтирования на открытом сердце [3; 4]. В статье представлен обзор 32-летних исследований. Более подробно они изложены в монографиях и статьях [1-5].
Помимо стандартных обследований (электрокардиография с нагрузкой, эхокардиография, мониторирование по Холтеру, мониторирование артериального давления, лабораторные анализы липидного спектра, высокочувствительного тропонина, креатинфосфокиназы, миоглобина и др.), многократно каждому больному проводилось РКГ-исследование с анализом ВСР. При сравнении результатов РКГ со стандартными клиническими и параклиническими данными выявлены определённые закономерности. Доказано, что дизрегуляции СУ патогенетически обусловлены, обязательно сопровождают не только клинические формы ИБС, но и кардиоваскулярные осложнения соматической патологии [1; 2]. РКГ-симптомы во многих случаях определяют направление диагностического поиска и терапии. Анализ ВСР нашёл применение в интранозологической диагностике болезней и их особенностей, что значимо для персонализированной терапии, прогноза, контроля эффективности фармакотерапии [1; 2; 5; 7; 8].
Неинвазивно тремя электродами в течение 20-25 минут регистрируется электрокардиосигнал с передней поверхности грудной клетки пациента с соблюдением специальных условий из-за высокой чувствительности РКГ (до приёма пищи и лечебных процедур, при отмене лекарственных средств (ЛС) и др.). Использовался временной статистический анализ изменений межсистолических RR-интервалов, для оценки соотношения регулирующих факторов в СУ-спектральный анализ с быстрым преобразованием Фурье, спектральными окнами Хамминга и Парсена. В отличие от зарубежных разработок (Task Force, 1996) в анализ ВСР включена оценка гуморально-метаболического влияния на ионные токи через мембрану пейсмекерных клеток СУ. Игнорирование этого фактора внеклеточной среды является ошибочным отступлением от классической физиологии медленных потенциалов действия в пейсмекерах СУ. Результат анализа ВСР в этом случае неверен и является одной из причин отставания в клиническом анализе ВСР. Средние величины ВСР-показателей статистического анализа: средняя продолжительность RR-интервалов на анализируемой Ркг –RR, стандартная девиация всех волн от среднего RR -SDNN, среднеквадратические отклонения каждого вида флуктуаций - волн гуморально-метаболического влияния -σl, симпатического- σm, парасимпатического –σs- отделов автономной системы, средняя амплитуда дыхательной аритмии -ARA. Для оценки соотношения 3 факторов регуляции в СУ проводился спектральный анализ [1; 5-7] 3 энергетических разночастотных вкладов в общий тотальный спектр ВСР (100%) после разложения на 3 частотные гармоники. В программе «Микор» соотношение представлено долями воздействия на пейсмекеры гуморально-метаболического влияния в очень низкочастотном (VLF%), симпатического в низкочастотном (LF%) и парасимпатического в высокочастотном (HF%) диапазонах (рис. 1). Запись ВСР осуществлялась в пробах по методу А.М. Вейна с соавт. (2003), направленных преимущественно на один из факторов регуляции в СУ: в исходном состоянии лёжа (Ph), в пробах парасимпатической Вальсальвы-Бюркера (Vm), гуморально-метаболической Ашнера (pA), симпатической активной ортостатической (Aop) и в нагрузочной пробе, дозированной по ЧСС120 (PWC) [5]. В каждой из 5 позиций регистрировалось 260-300 RR-интервалов, всего 1500-1800 интервалов при однократном РКГ-исследовании. Анализировались постстимульный результат стационарной Ркг, а также периоды стимуляции в пробах по максимальной реакции на стимул в процентах относительно исхода (ΔRR%), по времени достижения её (tAB), и восстановления ВСР после стимула (tr). Все показатели статистического анализа, tAB и tr представлены в секундах (с), спектрального соотношения регуляции и максимальной реакции в пробах – в %. Вычислялись также показатели, нормированные на исход по формуле Wielder (1957) -nu для учёта «Закона исходного уровня» - nuRR, nu SDNN и т.д. В статье приводятся ВСР-данные, совпадающие с нормированными. Для апробации РКГ при кардиохирургических вмешательствах в 2011 г. создан комплекс с мониторным режимом записи КАП-РК-02-«Микор». Успешное применение анализа ВСР в кардиохирургии было и у других авторов [6; 10-12]. Приводятся результаты апробации при 123 случаях реваскуляризации миокарда шунтированием [3].
Обработка материалов проводилась в программе Stat-6 с критериями Стьюдента, а также Z - аналог t для непараметрических выборок большого объёма. Для корреляционного анализа применялся непараметрический метод Спирмена с пакетом SPSS 12.0. Многолетний опыт работы с анализом ВСР позволяет утверждать, что для регистрации и корректного анализа ВСР, оценивающего синаптический уровень регуляции в СУ, необходимы дискретизация электрокардиосигнала в 1000 Гц, такое же хранение и корректное программное обеспечение. Полезна и синхронная с Ркг запись ЭКГ в реальном текущем времени. Возможно сохранение ЭКГ или её фрагментов для детального анализа, увеличение и уменьшение масштаба записи. Выборочно обследованы 278 больных мужчин с СтСт 1 и 2 ФК, 20 с СтСт 3-4 ФК по классификации Канадской ассоциации кардиологов, (1976), 115 с ОКС, 96 - в первые сутки ИМ, 254 с КА различных клинических форм, с СН - 426, из их числа 128 с СН 1 ФК, 233-СН 2 ФК, 43-с СН 3 ФК, 22-с СН 4 ФК по классификации NYHA (1964). Все пациенты с ИБС были без сопутствующих других соматических болезней, на период РКГ-наблюдения обследованы стандартными кардиологическими методами. 256 пациентов обследованы коронароангиографией перед хирургическим вмешательством, из них 123 до, во время и в первую неделю после реваскуляризации миокарда шунтированием. 133 пациента направлены на стентирование. В остальных случаях с ИБС, в том числе с сочетанными формами, также проводилось РКГ-исследование, их данные включены в оценку общих ВСР-симптомов при всех формах ИБС. Контролем служили данные анализа ВСР у 47 здоровых мужчин возраста, сопоставимого с основной группой (рис. 1) [4; 5].
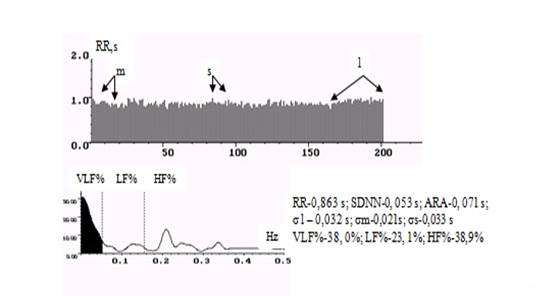
Рис. 1. Ритмокардиограмма, спектрограмма и цифровые значения показателей ВСР у здорового мужчины
Примечание. Показаны симпатические (m), парасимпатические (s) и гуморально-метаболические (l) волны ВСР. Автономные среднеквадратичные колебания (σm+σs) преобладают по амплитуде над среднеквадратичным отклонением гуморально-метаболических флуктуаций – σl. В спектральном соотношении регулирующих в СУ факторов LF%+ HF% (52%), установлено наименьшее гуморальное влияние (VLF%-38%) на пейсмекеры СУ, судя по спектрограмме.
Результаты исследования и их обсуждение
1. Хроническая ИБС и её клинические формы сопровождались общими для всей когорты больных РКГ-симптомами. При хроническом нарушении перфузии тканей сердца из-за атеросклеротической окклюзии венечных сосудов страдают и ткани СУ, миокарда и проводящей системы [1; 4; 5; 7-9]. Особо значимы нарушения с окклюзией в правой огибающей венечной ветви, от которой отходит артерия СУ [1; 4; 5; 7]. При хронической недостаточности кровоснабжения происходят дистрофические нарушения в самих пейсмекерных клетках СУ. Хуже всего, если в центральной зоне, в Р-клетках при формировании автономной кардионейропатии (АКН). На РКГ при АКН отсутствует волновая структура ВСР [3-5; 7]. RR-интервалы по продолжительности отличаются друг от друга в пределах единиц миллисекунд (3,55±1,02 миллисекунды) и на современных экранах мониторов выглядят сплошной ровной линией, лишённой флуктуаций [4; 5; 7]. В наших исследованиях АКН у больных ИБС была выявлена в 2003 г. при стенокардии 3 и 4 ФК, и СН 4 ФК. Данные запатентованы (Миронова Т.Ф., Миронов В.А., Миронов М.В. Патент № 2322942, 2008). Позднее АКН выявлена и в других исследованиях с применением РКГ [3; 5; 8; 9]. Поскольку снижалась амплитуда не только симпатических и парасимпатических флуктуаций, но и гуморально-метаболических, было предположение, что лишь автономной денервацией (Ewing D., 1978) АКН не объяснить. Поэтому в 2003, и затем в 2010 г. был получен аутопсийный материал СУ и проведены электронные гистологические исследования узловой ткани у пациентов с зарегистрированной при жизни АКН. C помощью электронной микроскопии в пейсмекерах СУ обнаружeны разрушения крист в митохондриях, скопления липофусцина, кальцинаты, вакуолизация клеток (Давыдова Е.В., Миронова Т.Ф., 2010), т.е. выявлены признаки дистрофии в СУ (рис. 2).

Рис. 2. Электронная микроскопия пейсмекерных клеток синоатриального узла сердца [2]
Примечания:
2.1. Гистологический препарат клеток переходного типа проводящей системы сердца в области синусового узла у мужчины из группы контроля, погибшего от внесердечной причины. Ультратонкий срез, контрастированный уранилацетатом свинца и цитратом свинца (увеличение в 1260 и в 1984 раза). Видны митохондрии (м) с сохранными кристами внутри клетки.
2.2. Гистологический препарат клетки переходного типа проводящей системы сердца в области синусного узла у погибшего больного ИБС с автономной кардионейропатией при жизни. Ультратонкий срез, контрастированный уранилацетатом свинца и цитратом свинца (увеличение в 1984 раза). Набухание множественных митохондрий и разрушение митохондриальных крист (кр), кальцинаты (к) в митохондриях, внутриклеточные включения липидных капель (л) и липофусцина (лф), что соответствует дистрофии пейсмекерных клеток синоатриального узла [2].
Пейсмекеры не в состоянии нормально реагировать на импульсы автономной системы. Клинико-инструментальным результатом формирования АКН было снижение амплитуды всех волн ВСР у больных ИБС (SDNN=0,019±0,004 с vs 0,052±0,006 с в норме; z-13,2 при n-278 и 47). Изменялось и соотношение быстрой симпато-парасимпатической регуляции в СУ в виде переключения руководства ритмом на филогенетически низкий гуморально-метаболический уровень, медленный и неэффективный. В норме парасимпатическое действие преобладает из-за физиологических особенностей автономной иннервации [1; 4; 5; 7; 8; 13]. У пациентов с ИБС это преимущество утрачивается. Снижаются значения σs, ARA, HF%, и соответственно снижается SDNN (σs=0,018±0,004; ARA= 0,033±0,003 с vs нормы- σs=0,032±0,004 с и ARA=0,072±0,001с; z=5,6 и 15,6; n-278 и 47). Также спектральная доля парасимпатического фактора регуляции становилась меньше (HF%=17,1±5,3% vs в норме HF%=41,5±4,52%; z-5,4 при n-278 и 47). Соответственно возрастало влияние гуморально-метаболической среды на пейсмекеры СУ (VLF%=56,12±12,4% vs нормы VLF%=36,8±4,9; z-4,12; n-278 и 47). РКГ по отрицательной динамике позволяет определить предвестников риска осложнений – ОКС, ИМ, жизнеопасных КА, а также высокого риска летального исхода.
2. Был найден Ркг-эквивалент ишемического эпизода при СтСт. При пароксизме на Ркг регистрировался участок предельно выраженной стабилизации ВСР, синхронный с депрессией S-T на ЭКГ и клиническими признаками СтСт (n-278). Разница между продолжительностью RR-интервалов в пределах ишемического эпизода 3,55±1,02 миллисекунды. При современной чувствительности экранов мониторов эти фрагменты Ркг не имеют волн ВСР. Поэтому такое выраженное снижение ВСР часто называют стабилизацией ритма (рис. 3).
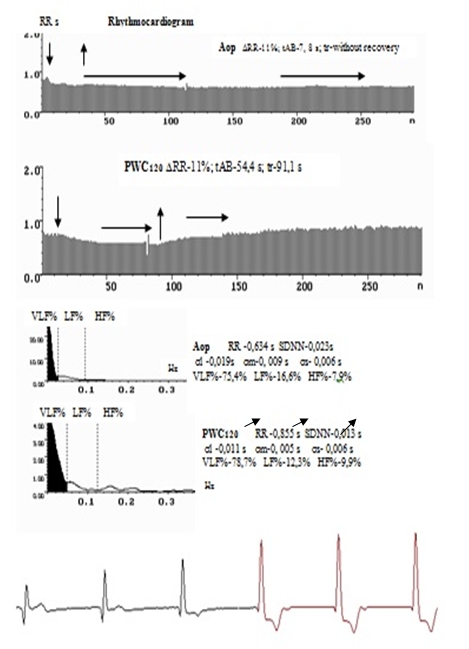
Рис. 3. Ритмокардиограммы, спектрограммы и средние значения показателей ВСР пациента со стабильной стенокардией 2 ФК в Аор и PWC
Примечание. Амплитуда волн ВСР снижена. На спектрограмме патологическое соотношение влияния регулирующих факторов с преобладанием очень низкочастотной гуморально-метаболической периодики – VLF%/ Горизонтальные стрелки обозначают фрагменты стабилизации на Ркг, синхронные с ишемическими эпизодами. На ЭКГ им соответствует депрессия ST.
Ркг-симптом СтСт со снижением амплитуды волн ВСР связан с нарушением перфузии СУ и гибернацией его пейсмекерных клеток из-за повышения вазоконстрикторного действия эндотелина-1 над атеросклеротической бляшкой, доводящего окклюзию венечных артерий до критических 70-80%. Степень снижения ВСР и реагирования в пробах соответствовала функциональным классам СтСт. При 1-2 ФК стабилизация ВСР во время пароксизма с разницей соседних интервалов в 3 тысячные доли секунды определяется лишь графическим курсором. Реакция на стимулы в пробах была также умеренно снижена. При СтСт 3-4 ФК дизрегуляция на Ркг представлена выраженным снижением амплитуды волн ВСР всей Ркг, то есть синдромом АКН [3-5; 7; 8]. Визуально при АКН разграничить эпизоды ишемии при современной чувствительности компьютерных медицинских мониторов трудно. Поэтому введён в программу модуль с точной оценкой тысячных долей секунды в определении продолжительности каждого интервала, а также с возможностью увеличения масштаба записи. Это измерение трудоёмко, но полезно при безболевой форме СтСт, в результате на Ркг она приобретает формализованный характер, что снижает её негативную диагностику (рис. 4).
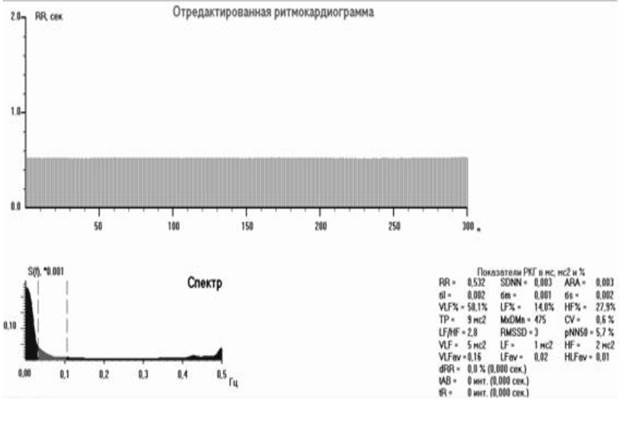
Рис. 4. Ритмокардиограмма, спектрограмма и средние значения ВСР-показателей у пациента с автономной кардионейропатией (АКН)
Примечание. РКГ не имеет волн, стабилизирована. Судя по спектрам, пейсмекерная активность СУ регулируется под влиянием гуморально-метаболической среды, недостаточно эффективной и медленной.
Проверка по методу И.И. Власова (1997) диагностической ценности этого Ркг- симптома СтСт составила: чувствительность - 87,3%, (более чем в 2 раза выше, чем при ЭКГ), специфичность- 83,54%, позитивный результат -69,3%, негативный - 45,4% (Миронов М.В., 2003).
3. Выявлены предвестники острого коронарного синдрома (ОКС), дифференцировано субэпикардиального и субэндокардиального (n-38 и 77) [4]. Общими предикторами ОКС являются увеличение продолжительности (с точностью до 1 мсек.) и частоты участков стабилизации ВСР, вариабельный порог ишемии. Субэндокардиальный вариант без элевации ST (ОКСБПST) чаще манифестировался очень низкоамплитудными симпатическими колебаниями ВСР (σm=0,010±0,004 с vs в норме σm=0,024±0,003 с; z=14,285, n -77 и 47), что, вероятно, обусловлено повышенной плотностью симпатических рецепторов в передней стенке левого желудочка. Субэпикардиальное (ОКСПST) поражение сочеталось с полной стабилизацией ВСР и отсутствием реакций на пробы, что соответствовало АКН (SDNN=0,014±0,005 c vs в норме SDNN= 0,052±0,006 c; n=38 и 47; z=3,18). При поражении задней стенки левого желудочка некрозом характерна предельно выраженная стабилизация ВСР - АКН. При АКН было выраженное снижение реакций на стимулы в пробах, замедленное их достижение и восстановление после пробы (SDNNAop=0,017±0,004 c; ΔRRАор =5,1±1,3%; tAB и trAop=18.4±3,2 и 21,5 с; n-20 vs нормы: SDNN=0,052±0,006 c; ΔRRАор =30±1,9%; tABАор=5,12±0,005%; trАор=7.015±0,003 с; n-19 и 47, z=2,8-14,2). Найдено, что АКН один из предикторов летальных исходов у больных ИМ задней стенки. Тюрин А.Ю. (2005), выполнив РКГ-исследование 96 пациентам с ИМ и пронаблюдав их в течение 1 года в динамике постинфарктного статуса, сообщил о смерти 8 из них. Из их числа у 7 был ИМ задней стенки левого желудочка. В процессе же наблюдения всей группы пациентов, перенёсших задний ИМ (n- 14), у умерших при жизни была наиболее тяжёлая клиника с акинезией задней и компенсаторной гиперкинезией передней стенки левого желудочка на ЭхоКГ. В случаях с передним ИМ (n -37) при благополучном течении на Ркг сохранялась очень низкоамплитудная симпатическая волновая структура ВСР, возможно, в связи с плотностью адренергических рецепторов. Определена дифференцированная волновая структура ВСР при ИМ, связанная с морфологическими особенностями миокарда [4; 5].
Найдены варианты преимущественного поражения миокарда и/или венечных артерий при хронической форме ИБС [4]. Преобладание преимущественных изменений в миокарде сопровождалось снижением максимальной реакции на стимулы в пробах (ΔRRАор =19,1±1,3% vs нормы ΔRRАор =29,4±1,8%; n=24 и 47, z=27,8), время максимального реагирования увеличилось недостоверно, восстановления после пробы достоверно (tABАор =12,35±5,08 c, tr Аор =12,4±7,4 c vs в норме tAB Аор =12,1± 0,005с и tr Аор =7,015±0,003 c; n-24 и 47; z=0,236 и 3,49).
Таким образом, общими для всех форм ИБС ВСР-симптомами являлись: снижение амплитуды всех волн ВСР (SDNN). В последовательности была сначала утрата нормального парасимпатического преобладания (σs, HF%), затем снижение всех 3 видов волн и снижение реакций в пробах (ΔRR), увеличение времени их достижения и восстановления после них (tAB, tr). Доказано, что в Аор снижению реакции соответствует снижение коронарного резерва (Жемайтите Д.И., 1989). При ИБС было нарушено и спектральное соотношение регулирующих факторов, оно изменялось в сторону увеличения гуморально-метаболического влияния в СУ (VLF%=56,39±14,9% vs нормы 36,8±4,9%; z=14,95; n=426 и 47) за счёт снижения спектральных долей cимпатического и парасимпатического воздействия (LF%, HF%). Филогенетически гуморальная регуляция наиболее древняя, медленная и недостаточная, иногда парадоксальная.
4. При аритмиях ишемического генеза при регистрации Ркг найдены полезные для аритмологии возможности метода, не повторяющиеся в других инструментальных исследованиях [1; 4; 5; 7]. База данных более чем в 971 записи по 5 позиций, сопоставление из них отобранных 254 Ркг без сопутствующей патологии с другими инструментальными данными свидетельствовали, что большинство клинических форм аритмий регистрируются на Ркг. Они часто легко и сразу распознаются визуально (рис. 5, 6), что имеет значимое клиническое преимущество. В аритмологии также привлекательна возможность определения гемодинамического значения нарушений ритма (чувствительность – 87,4%). Оно проявлялось изменением волновой структуры ВСР и/или уровня Ркг.
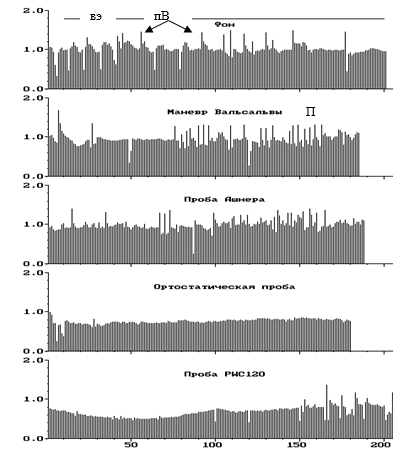
Рис. 5. На Ркг вставочные экстрасистолы (вэ) с удлинением 3-5 постэктопических интервалов, эпизоды парасистолии (П), периодика Венкебаха (пВ) - синоатриальная блокада 1-й степени 2-го типа с удлинением постэктопической паузы и последующих интервалов с уменьшающимся декрементом на фоне сниженной ВСР
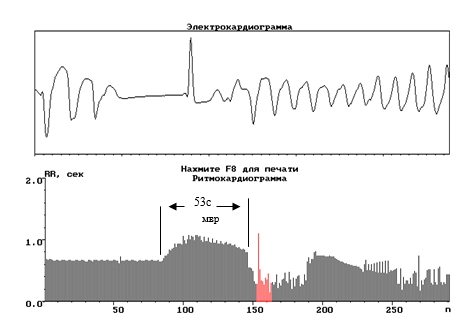
Рис. 6. Ркг и ЭКГ пациентки в отделении реанимации
Примечание. Во время записи Ркг начался спонтанно подъём уровня Ркг с признаками миграции водителя ритма (мвр), как предиктора желудочковой тахикардии за 53 минуты до жизнеопасного нарушения ритма. В условиях реанимации больную удалось спасти.
При коронарной патологии после эпизода аритмии в 42% возникала стабилизация ВСР, свидетельствующая о патогенетической связи нарушений ритма с ишемией (рис. 7).
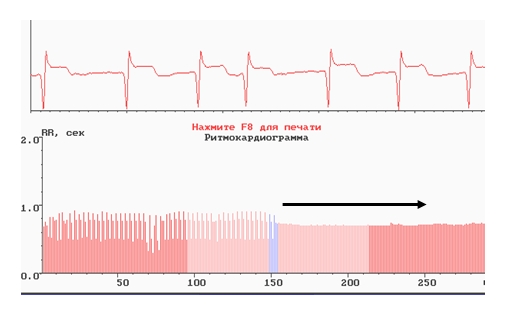
Рис. 7. Ркг и ЭКГ б-го с субэпикардиальным ИМ с суправентрикулярной экстрасистолией
Примечание. Стабилизация ВСР после экстрасистол свидетельствует об их гемодинамической значимости и спровоцированном аритмией ишемическом эпизоде (отмечен горизонтальной стрелкой). Значительное снижение ВСР характерно для автономной дизрегуляции и изменений в пейсмекерных клетках СУ при ИБС.
Безопасная РКГ предусматривает возможность выбора фармакотерапии, иногда при первой разовой дозе лекарства, что важно для рационального лечения. При сложных формах нарушений ритма РКГ-исследование способно определить фармакотерапию, фармакодинамику, дозу препарата, последовательность применения, а также нежелательные эффекты лекарств.
Соотношения пре- и постэктопических интервалов в силу точности Ркг-регистрации нуждаются в некоторых поправках. К примеру, удлинения постэктопических интервалов на величину недостающей до среднего значения преэктопического RR у суправентрикулярных экстрасистол отличаются на 15-25 миллисекунд. Колебания соотношения аналогичных показателей при желудочковых экстрасистолах также имеют отклонения от общепринятых суждений. Неповторима другими методами возможность Ркг-оценки автономного аритмогенного фона. АКН с выраженным снижением амплитуды и реакций ВСР свидетельствует о существенном ослаблении иерархической роли СУ, что сопровождается активацией эктопических очагов. Поэтому есть основания предполагать, что АКН с автономной денервацией и дистрофическими нарушениями в СУ является предиктором аритмий сердца, в том числе миграции водителя ритма по СУ и предсердиям, а также предвестником фибрилляции предсердий.
5. В кардиохирургии в 2011-2013 гг. проведено дооперационное РКГ-исследование 256 пациентов, назначенных на интервенционную реваскуляризацию миокарда. 123 стандартно отобранным пациентам проведено аорто- и маммаро-коронарное шунтирования на открытом сердце. Повторное РКГ-исследование проведено в раннем периоде после шунтирования. Волновая структура ВСР ухудшилась у всех пациентов, снизилась амплитуда волн ВСР, недостоверно увеличилась доля парасимпатической регуляции [3]. Судя по математическим значениям показателей Ркг, состояние больных с АКН (таких было 30) после операции оставалось тяжелым. Один пациент на 4-е сутки скончался, у 29 послеоперационный результат лечения положительный. У всех 30 названных наиболее тяжёлых пациентов при оценке ВСР-данных была установлена АКН до операции, что предполагало особо усиленную подготовку к вмешательству, профилактику осложнений во время и после шунтирования, персонализированное ведение анестезии во время операции. Такие же предвестники получены и у других авторов [6; 10-13]. Наиболее интересны РКГ-исследования с мониторной записью Ркг с помощью АПК КАП-РК-02-Микор во время проведения шунтирования. Оказалось, что каждому этапу проведения операции соответствует свой вариант нарушений структуры ВСР, патогенетически обусловленный изменениями, происходящими в кардиологическом актуальном статусе в результате анестезиологии, а также из-за хирургических манипуляций (рис. 8) [3]. Например, трепетание предсердий возникало при канюляции правого предсердия. По нашим данным, хирургические манипуляции связаны с аритмиями той локализации, где проводились эти вмешательства. Предсердные нарушения регистрировались на Ркг при канюляции правого предсердия, желудочковые – при канюляции аорты (рис. 8), при запуске сердца массажем после операции и отключении аппарата искусственного кровообращения возникали желудочковые аритмии.
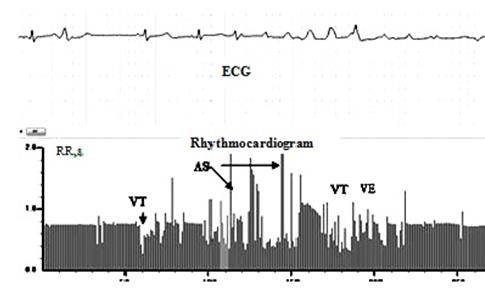
Рис. 8. ЭКГ и РКГ при установке зажима на аорте и введении кардиоплегической смеси перед подключением сердца к аппарату искусственного кровообращения
Примечание. Зарегистрированные нарушения ритма связаны с манипуляциями хирургов. Заметны эпизоды заместительных ритмов, тахикардии (VT) и асистолия (AS).
Ещё в предоперационном периоде выявляются предвестники осложнений во время вмешательства. Предиктором нарушений ритма была АКН уже при отборе больных для операции [3]. Реализована и апробирована online мониторная дистанционная передача Ркг-данных из операционного зала в лабораторию нейрокардиологии для неотложного анализа и консультирования. Выявленные подробности изменений в СУ сердца способны внести инновационное направление в отбор и подготовку пациентов к операции, ведение её с помощью мониторинга ВСР, а также корректировать формы послеоперационного менеджмента [3].
Выводы
1. Результаты исследований по разработке клинического метода ритмокардиографии позволяют считать компьютерную РКГ высокого разрешения адекватным методом интранозологической диагностики клинических форм ИБС от раннего выявления до интервенционного кардиохирургического вмешательства.
2. Основой РКГ является оценка мультивариантных нарушений регуляции пейсмекерной активности синусового узла сердца, патогенетически связанных с клиническими вариантами ишемического процесса с образованием Ркг-симптомов, опережающих диагностически значимые признаки заболевания и являющиеся для него фоном дизрегуляции.
3. Выделены РКГ-симптомы, общие для всех форм хронической ишемической болезни, в том числе для стабильной стенокардии, сердечной недостаточности в соответствии с их функциональными классами, вариантов острого коронарного синдрома и инфаркта миокарда субэндокардиальной и субэпиквардиальной форм, с элевацией ST и без неё.
4. Установлено, что при кардиоаритмиях ишемического генеза по Ркг возможно определение клинической формы нарушений ритма сердца, оценить аритмогенный автономный фон, а также гемодинамическое значение каждого эпизода аритмии, что важно для персонализированной терапии.
5. При интервенционном кардиохирургическом вмешательстве при реваскуляризации миокарда РКГ-исследование до операции позволяет определить предикторы жизнеопасных нарушений ритма во время операции, результаты операции и особенности ведения больных в послеоперационном периоде.
6. Каждому этапу шунтирования соответствуют патогенетически обусловленные изменения волновой структуры вариабельности сердечного ритма.
7. Найдено, судя по клинической форме аритмий, что кардиоаритмии во время шунтирования связаны с кардиохирургическими манипуляциями.
Библиографическая ссылка
Миронова Т.Ф., Миронов В.А., Николаенко О.В., Куватова Е.В. КЛИНИЧЕСКАЯ РИТМОКАРДИОГРАФИЯ ПРИ ИШЕМИЧЕСКОЙ БОЛЕЗНИ СЕРДЦА // Современные проблемы науки и образования. – 2017. – № 5. ;URL: https://science-education.ru/ru/article/view?id=26837 (дата обращения: 19.04.2024).



