Проблема некоронарогенных поражений сердца приобретает все большую социальную значимость, поскольку данная патология преимущественно встречается у лиц молодого и трудоспособного возраста. В течение последних десятилетий на порядки увеличилась частота их диагностики среди населения. Пересмотрены многие патогенетические концепции, усовершенствованы диагностические технологии, появился целый ряд новых методик, которые расширяют возможности оценки не только механизмов формирования, но и выбора наиболее эффективных методов лечения, способствующих улучшению прогноза [1]. Продолжают совершенствоваться методы профилактики и реабилитации больных. Несмотря на это, в современной медицине объединенная группа заболеваний сердца, условно относящихся к некоронарогенным, является малоизученной, поскольку по своей этиологии они весьма разнообразны [2; 3]. Более того, некоронарогенные заболевания миокарда (НЗМ) являются одной из ведущих причин сердечной недостаточности, которая, в свою очередь, приводит к ухудшению качества жизни пациентов, снижению или полной утрате трудоспособности и в итоге − к смерти больных [4].
По частоте встречаемости, тяжести течения миокардиты занимают одни из лидирующих позиций среди НЗМ. Следует помнить, что именно он является источником внезапно развившейся острой сердечной недостаточности примерно в 10% случаев. При этом у пациентов с фульминантным миокардитом чаще развивается кардиогенный шок с высоким процентом летальности. Эндомиокардиальная биопсия (ЭМБ) является «золотым стандартом» в диагностике данной патологии. Однако только 30% морфологически верифицированных миокардитов прогрессируют с развитием ДКМП, что связывают с плохим прогнозом [5; 6].
При дилатационной кардиомиопатии (ДКМП) отмечается расширение камер сердца, снижение фракции выброса левого желудочка (ФВ ЛЖ) <45%, увеличение конечно-диастолического размера ЛЖ > 117% или уменьшение фракции укорочения передне-заднего размера ЛЖ <25%. Описанные структурные изменения приводят к развитию застойной СН [7] с ежегодной летальностью от 10 до 50%. На 100 000 населения в год частота заболевания составляет 5–8 случаев [8; 9]. Практикующему врачу не следует забывать, что идиопатическая ДКМП всегда должна быть диагнозом исключения. Тщательное и полное обследование, включая инвазивные и генетические методы диагностики, позволяют наиболее точно распознать конкретную патологию у данного больного, что в свою очередь способствует подбору оптимальных методов терапии [10].
Патогистологическая верификация диагноза, особенно в группе миокардитов, очень важна, поскольку во многом может изменить тактику лечения. В настоящее время микроскопическая оценка патоморфологических изменений, оставаясь базовой, может быть дополнена системным количественным исследованием. Таким методом является морфометрия. В широком понимании морфометрия - учение о правилах получения числовых характеристик изменений форм любой природы. В медицине широко используют компьютерную морфометрию. На ее основе созданы морфометрические модели различных патологических состояний, изучены особенности миокарда левого желудочка при острой коронарной недостаточности. Таким образом, использование компьютерной обработки изображения микропрепаратов сердца в сочетании с морфометрией является перспективным научным направлением [11].
Цель исследования: определить морфологические изменения миокарда у пациентов с сердечной недостаточностью со сниженной фракцией выброса левого желудочка (ФВ ЛЖ) некоронарогенной этиологии с помощью компьютерной морфометрии.
Материалы и методы. Обследовано 68 человек, которым выполнена биопсия миокарда правого желудочка для морфологической верификации диагноза, явившегося причиной сердечной недостаточности разной степени выраженности.
Критерии включения в исследование: возраст > 18 лет; ФВ ЛЖ < 40%; отсутствие в анамнезе данных за ишемическую болезнь сердца; отсутствие гемодинамически значимых стенозов коронарных артерий по данным коронароангиографии; наличие у пациентов показаний для выполнения ЭМБ согласно современным рекомендациям Европейского общества кардиологов (2007); согласие больного на участие в исследовании.
Возраст пациентов составил от 19 до 66 лет. Среди них мужчин было 57, женщин − 9. Коронароангиография проведена у 63 человек с целью исключения ишемической болезни сердца. При направлении на ЭМБ у 51 больного клинико-анамнестически выставлен диагноз «дилатационная кардиомиопатия» (ДКМП), у 7 – «миокардит» (Мк), у 10 «постмиокардитический кардиосклероз» (ПМКС).
Биопсия миокарда правого желудочка проведена в условиях рентгеноперационной. Во время процедуры осуществляли мониторинг ЧСС, АД, ЭКГ и SpO2. После стандартной подготовки и местной анестезии 1%-ным раствором лидокаина была пунктирована общая бедренная вена (чаще правая) и через нее до правого предсердия доставлен проводниковый катетер 7 F длиной 85 см. Трехстворчатый клапан проходили с помощью проводника. Подтвердив правильное положение катетера в правом желудочке, с помощью гибкого биоптома брали от 4 до 6 образцов миокарда. После завершения процедуры венозный катетер удаляли и накладывали повязку. Биопсийный материал помещали в 15%-ный раствор нейтрального формалина. В условиях локальной лаборатории НИИ-ККБ № 1 гистологические препараты обрабатывались по общепринятой методике. При исследовании образцов первым этапом выполнена окраска гематоксилином-эозином парафиновых срезов с последующей световой микроскопией (микроскоп Olympus IX51). Изображения были получены цифровой камерой Nikon D3100. Проведена их обработка с помощью программы ImageJ (Rasband, W.S., ImageJ, U. S. National Institutes of Health, Bethesda, Maryland, USA): выполнен перевод в восьмибитный формат и бинаризация с выставлением порога чувствительности. Далее определяли поочередно площадь кровоизлияний, некроза, липоматоза и фиброза. Проведен расчет площади биоптата (фрагмент изображения, соответствующий биоптату, обводили встроенной в программу линейкой-курвиметром, далее определяли площадь данного фрагмента). Подсчитывали количество клеток воспаления (нейтрофилов, макрофагов, лимфоцитов) с последующим расчетом их содержания на 1 мм кв. площади биоптата (общее количество клеток / общая площадь биоптата) и процент площади, занимаемый патологическими изменениями (некроз, кровоизлияние, липоматоз, фиброз). У четырех больных с подозрением на миокардит исследование биоптата проводили методом полимеразно-цепной реакции (вирусологичекий спектр: вирус Эпштейна-Барр цитомегаловирус, t. gondii, varicella zoster, вирусы простого герпеса 1, 2, возбудители ОРВИ, парвовирус В19, полиовирусы, энтеровирусы группы С).
Статистическая обработка данных проводилась с помощью программы STATISTICA 10 for WINDOWS. При описании данных мерой центральной тенденции служила средняя арифметическая M, мерой рассеяния - стандартное отклонение. С целью выделения диагностически значимых критериев проводился многомерный дискриминантный анализ с оценкой λ – Уилкса, F-критериями значимости, уровнями толерантности, межгрупповыми и внутригрупповыми различиями, коэффициентами канонической корреляции. Показатели считались статистически значимыми при р <0.05.
Результаты. Все пациенты страдали сердечной недостаточностью разной степени выраженности. Фракция выброса левого желудочка, по данным эхокардиографии, составляла 21,7 + 3,62%. Дистанция 6-минутной ходьбы – 232 + 6,22 м. Отсутствие коронарной патологии подтверждено по результатам ангиографии. Вирусологическое исследование биоптатов показало вирус-негативность по представленному спектру у всех пациентов.
При исследовании биоптатов миокарда выявлены следующие изменения (табл. 1, 2).
Таблица 1
Гистологические изменения в миокарде
|
Параметры |
ДКМП |
ПМКС |
Mк |
Р (ДКМП/ПМКС) |
Р (ДКМП/Мк) |
Р (ПМКС/Мк) |
||
|
M± m |
||||||||
|
% некроза |
0,33±0,14 |
0,30±0,25 |
0,98±0,98 |
0,81 |
0,60 |
0,57 |
||
|
% кровоизлияния |
0,50±0,20 |
0,03±0,03 |
3,24±3,24 |
0,42 |
0,37 |
0,53 |
||
|
% липоматоза |
2,30±1,00 |
0,59±0,34 |
0,00±0,00 |
0,48 |
0,49 |
0,48 |
||
|
% фиброза |
4,90±2,02 |
3,73±1,56 |
1,38±0,97 |
0,86 |
0,85 |
0,42 |
||
Таблица 2
Клеточный состав инфильтрата миокарда
|
Параметры |
ДКМП |
ПМКС |
Mк |
Р (ДКМП/ ПМКС) |
Р (ДКМП/ Мк) |
Р (ПМКС/Мк) |
||
|
Число клеток в 1 мм2 (M± m) |
||||||||
|
Нейтрофилы |
1,89±0,72 |
0,82±0,68 |
9,47±5,98 |
1,00 |
0,71 |
0,47 |
||
|
Макрофаги |
4,04±1,28 |
2,90±1,01 |
9,50±3,85 |
0,74 |
0,63 |
0,50 |
||
|
Лимфоциты |
5,90±2,30 |
5,35±2,11 |
12,30±5,87 |
0,98 |
0,92 |
0,76 |
||
При анализе биоптатов миокарда определены следующие характеристики групп (рис.):
1. Для миокардитов характерна выраженная смешанно-клеточная инфильтрация нейтрофилами, макрофагами и лимфоцитами; обширные очаги некроза, множественные кровоизлияния, а также слабо и умеренно выраженный кардиосклероз.
. Для постмиокардитического кардиосклероза характерна скудная цитограмма лейкоцитарного инфильтрата, представленная в основном лимфоцитами и макрофагами, в то время как эффекторы острого воспаления (нейтрофилы) практически не встречаются; умеренно выраженный кардиосклероз, мелкие очаги некроза и единичные кровоизлияния.
3. При дилатационной кардиомиопатии цитограмма лейкоцитарного инфильтрата в миокарде умеренно выражена и представлена главным образом макрофагами и лимфоцитами, встречаются единичные нейтрофилы. Для данной группы характерна выраженная дистрофия кардиомиоцитов, сочетание очагов некроза и склероза. Имеются крупные очаги липоматоза.

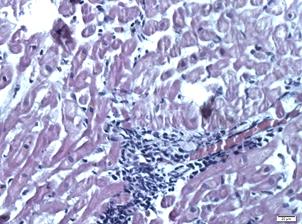
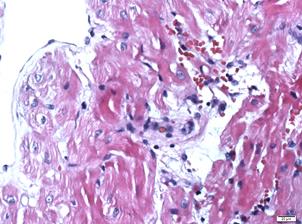

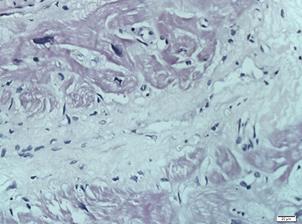
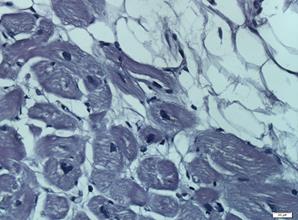

Морфологические изменения, выявленные по данным ЭМБ: а, б – «миокардит»* - обширные участки миоцитонекроза, резкий отек, густая лимфо-лейкоцитарная инфильтрация интерстиция (с преобладанием лимфоидных клеток), участки замещения фиброзной тканью. Сохранные кардиомиоциты неравномерно гипертрофированы; в – «постмиокардитический кардиосклероз» - среди пучков неравномерно гипертрофированных кардиомиоцитов в интерстиции имеются диффузные разрастания фиброзной ткани, единичные зрелые лимфоциты. Ядра окрашены неравномерно, отмечается слабый фокальный ядерный полиморфизм; г – «кардиомиопатия невоспалительного генеза» - гистоархитектоника миокарда нарушена за счет хаотичного расположения неравномерно гипертрофированных кардиомиоцитов. Ядра полиморфные, неравномерно окрашены. Цитоплазма со слабо выраженной зернистостью. Признаков текущего воспаления и миоцитонекроза не обнаружено. Окраска гематоксилином и эозином, об. 40 х ок. 10
* диагноз «миокардит» выставлен согласно Далласским критериям диагностики миокардитов.
Выводы. При изучении цитограммы лейкоцитарного инфильтрата в миокарде методом компьютерной морфометрии установлено, что при острых миокардитах на 1 мм2 преобладают нейтрофилы (эффекторы острого воспаления), в то время как макрофаги и лимфоциты превалируют в группах ПМКС и ДКМП. При анализе гистологических изменений в миокарде методом компьютерной морфометрии установлено, что в группе миокардитов преобладают некроз и кровоизлияния, в то время как при хронически текущем воспалении или кардиомиопатиях невоспалительного генеза (группы ПМКС и ДКМП) изменения представлены главным образом фиброзом и липоматозом.
Таким образом, компьютерная морфометрия может быть применена в дополнение к общепринятым методам цитологических и гистологических исследований миокарда с целью более точной морфологической верификации диагноза у пациентов, страдающих выраженной сердечной недостаточностью некоронарогенной этиологии.
Заключение. В настоящее время продолжается поиск новых и попытка усовершенствования уже известных диагностических алгоритмов КМП. С огромной скоростью развиваются иммуногистохимические и молекулярно-генетические методы верификации миокардитов [1; 13; 14]. Количественные гистологические и цитологические характеристики изменений в миокарде, полученные нами в ходе исследования, сопоставимы с результатами морфологической верификации миокардитов, постмиокардитического кардиосклероза и кардиомиопатий невоспалительного генеза, представленных в мировой литературе [5]. Однако использование компьютерной морфометрии позволяет взглянуть на особенности диагностики НЗМ под другим углом. В отличие от описательной анатомии, гистологии, патологической анатомии количественная морфология является интегративной дисциплиной, дополняющей и уточняющей данные исследований, проводимых обычными морфологическими методами с позиций новых обобщающих подходов. Использование для этих целей системного анализа расширяет возможности морфологического исследования качественных и количественных изменений, дает возможность глубже раскрыть и точнее выразить общие и частные закономерности [11].
Конфликт интересов не заявляется.
Библиографическая ссылка
Бахчоян М.Р., Космачева Е.Д., Славинский А.А., Веревкин А.А., Понкина О.Н., Чуприненко Л.М. СТРУКТУРНЫЕ ИЗМЕНЕНИЯ МИОКАРДА ПРИ ВЫРАЖЕННОЙ СЕРДЕЧНОЙ НЕДОСТАТОЧНОСТИ НЕКОРОНАРОГЕННОЙ ЭТИОЛОГИИ: КОМПЬЮТЕРНАЯ МОРФОМЕТРИЯ // Современные проблемы науки и образования. – 2017. – № 5. ;URL: https://science-education.ru/ru/article/view?id=26889 (дата обращения: 23.04.2024).



