В области консервативной терапии фибромиомы матки достигнуты определенные успехи, но, несмотря на это, основным методом лечения миомы матки на сегодняшний день остается хирургический, который используется в 50–70 % случаев [1-3]. Обращает на себя внимание наличие миомы матки у молодых женщин; средний возраст ее выявления составляет 32 года [4]. Сохранение репродуктивной функции у женщин с миомой матки, после операции по поводу ее удаления, приобретает все большую социальную значимость, что обусловлено увеличением среднего возраста женщин, планирующих первую беременность [5,6]. Одним из патологических процессов в организме женщины, который развивается у данной категории пациенток до и после оперативного лечения, является анемия (у 20–60 % больных), возникающая вследствие патологической кровопотери из пораженного болезнью органа [4].
Часто анемия является тем патологическим фоном, на котором возникают осложнения при оперативном лечении: возникает риск увеличения кровопотери во время операции и инфекционных осложнений в послеоперационном периоде, длительность послеоперационного периода и время заживления раны, что является одним из важных моментов, влияющих на положительный результат лечения [7,8]. При анемии возникает неполное кислородное обеспечение тканей, прогрессирующая гемическая гипоксия с последующим развитием вторичных метаболических расстройств [1,3]. Терапия анемии у больных с миомой матки на практике представляет трудно выполнимую задачу, так как на фоне рецидивирующих менометроррагий формируется порочный круг, когда из-за тяжести состояния больной – нет условий для консервативной миомэктомии, а лечение анемии, за короткий период до начала очередного кровотечения – неэффективно [9,10]. Многие годы терапия анемии решалась за счет донорской крови и ее компонентов. Недостатки трансфузии донорской крови широко известны: опасность заражения вирусными инфекциями, возможность тяжелых гемотрансфузионных осложнений [7,10].
Таким образом, большое значение в планировании периоперационного периода у данной группы пациенток должно уделяться современным методам коррекции анемического синдрома в совокупности с технологиями кровесбережения.
Цель исследования: оценить эффективность рационализации кровесберегающих технологий при выполнении консервативной миомэктомии на фоне применения карбоксимальтозата железа и транексамовой кислоты в периоперационном периоде.
Материалы и методы: в исследование включены 81 пациентка (возраст от 25 до 49 лет) с диагнозом симптомная множественная миома тела матки, которым выполнялась консервативная миомэктомия. Все пациентки оперированы в условиях сбалансированной общей анестезии и разделены на три группы в проспективном порядке. Группа стандартной терапии. В предоперационном периоде пациентки не получают терапию анемического синдрома. При необходимости возмещение кровопотери будет проводиться инфузионными растворами и, по показаниям, препаратами крови (протокол I). Группа терапии железодефицитной анемии в предоперационном периоде карбоксимальтозатом железа (протокол II). Кумулятивная доза препарата в мг элементарного железа, необходимая для восстановления уровня гемоглобина Нb и восполнения запасов железа, рассчитывается индивидуально в соответствии с общим дефицитом железа в организме по формуле:
Кумулятивный дефицит железа [мг] = Вес тела [кг] х (целевой Hb* – фактический Hb) [г/дл]** х 2.4*** + Запасное депо железа [мг]****
* Целевой Hb для веса тела меньше 35 кг = 13 г/дл, соответственно 8,1 ммоль/л. Целевой Hb для веса тела 35 кг и больше = 15 г/дл, соответственно 9,3 ммоль/л.
** Чтобы конвертировать Hb [мМ] в Hb [г/дл]: умножьте Hb [мМ] на коэффициент 1,61145.
*** Коэффициент 2,4 = 0,0034 х 0,07 х 10000; 0,0034: содержание железа гемоглобина = 0,34%; 0,07: объем крови = 7 % веса тела; 10000: коэффициент преобразования 1 г/дл =10000 мг/л.
**** железо депо для веса тела меньше 35 кг = 15 мг/кг веса тела. Железо депо для веса тела 35 кг и больше = 500 мг.
За 2 суток до предполагаемой операции вводится кумулятивная доза путем внутривенной инфузии. При необходимости, возмещение кровопотери согласно протоколу I. Группа терапии железодефицитной анемии в предоперационном периоде карбоксимальтозатом железа, с введением ингибиторов фибринолиза. Ведение пациентов согласно протоколу 2, с добавлением транексамовой кислоты, вводимой за 30 мин до операции в дозе 15 мг/кг (протокол 3).
Обследование пациенток в предоперационном периоде было выполнено по протоколу, который включал в себя: общеклинический анализ крови, исследование системы гемостаза, биохимическое исследование крови, рентгенографию органов грудной клетки, электрокардиографию. Перед операцией все пациентки получали премедикацию: H1-блокаторы (супрастин 25 мг), бензодиазепины (феназепам 1–2 мг), ингибитор Н+-К+-АТФ-азы (нексиум 20 мг). Перед операцией всем пациенткам проводилась преоксигенация 80 % 02, 3–5 мин. Индукция анестезии: пропофол (1,5–2,5 мг / кг массы тела), фентанил (2–3 мкг/кг). Миорелаксация, перед интубацией трахеи, выполнялась атракурия безилатом (0,5–0,6 мг/кг), и в дальнейшем поддерживалась его болюсным введением 0,1–0,2 мг/кг. Поддерживающая анестезия выполнялась севофлураном (2,2–1,8 %) в сочетании с фентанилом (2,0–4,0 мкг / кг / час). Уровень BIS мониторинга 40–50 % (система Bis Vista, Aspect Medical Systems, США). Всем пациенткам проводился стандартный периоперационный мониторинг (пульсоксиметрия, капнография, регистрация ЭКГ, ЧСС, артериального и венозного давления) и респираторная поддержка (Chirana Venar, Chirana, Словакия). Респираторная поддержка осуществлялась в режиме CMV, со следующими параметрами: дыхательный обьем 6–8 мл / кг, поток Minimаl-Flow анестезия – 1 л/мин, с ПДКВ 5 см вод. Ст, FiO2 40 %, при необходимости выше для достижения Sp02 95 % и выше. Частота дыхания корректировалась по поддержанию Et CO2 в пределах 30–35 мм рт. ст.
Оценка обьема интраоперационной кровопотери осуществлялась по методу Мура (Мооrе), V=ОЦКдх(Htд-Htф)/Htд, где V – объем кровопотери (мл.), ОЦК – должный ОЦК (мл.), Htд – должный Ht, Htф – фактический Ht. ОЦК вычисляется следующим образом: 60–65 мл на 1 кг массы тела у женщины.
Регистрировались показатели «красной» крови: гемоглобин, гематокритное число, количество эритроцитов в одном миллилитре крови. 1 – при поступлении пациентки в стационар (исходный уровень); 2 – непосредственно накануне операции; 3 – по окончании операции; 4 – через 12 часов после завершения операции. Иммунобиохимический контроль включает в себя:
1) оценка показателей лактата (повышенный уровень сывороточного лактата в раннем послеоперационном периоде может отражать наличие интраоперационной тканевой гипоперфузии);
2) оценку уровня гликемии (в ответ на хирургическую агрессию увеличивается продукция глюкозы за счет гликогенолиза в печени, индуцируемого симпатической адренергической стимуляцией. Повышение концентрации глюкозы в крови – пропорционально интенсивности хирургической травмы);
3) оценка исследования системы гемостаза.
Все исследования проводятся накануне, непосредственно перед операцией и по окончании оперативного вмешательства.
Все полученные в процессе исследования цифровые данные будут подвергнуты статистической обработке методами вариационной статистики с вычислением средней величины признака (М), среднего квадратичного отклонения (сигма) и ошибки средней арифметической величины (m). Достоверность различий будет определена при помощи критериев достоверности Стьюдента. Различия считали статистически значимыми при p<0.05.
Результаты
Величина интраоперационной кровопотери во всех группах не имеет достоверных различий (рисунок 1). Однако в целом в группе с инфузией транексамовой кислоты, кровопотеря была на 28,6 % меньше, чем в группе, следовавшей протоколу 1, и на 24 % меньше в группе, следовавшей протоколу 2.
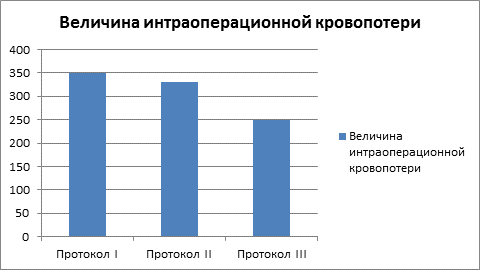
Рис. 1. Величина интраоперационной кровопотери
* Примечание: p<0,05, в сравнении с другими группами.
Для каждой группы были получены средние показателей крови в различные периоды времени: гемоглобин (таблица 1), эритроциты (таблица 2), гематокрит (таблица 3).
Таблица 1
Уровень гемоглобина у пациенток в различные периоды времени
|
Клиническая группа |
Время забора крови относительно операции |
||
|
48 часов до операции |
3 часа до операции |
Через час после операции |
|
|
Протокол 1 |
102,8±2,3 |
103,9±4,2 |
82,1±1,4* |
|
Протокол 2 |
98,0±2,7 |
119,2±1,8* |
90,2±1,8* |
|
Протокол 3 |
101,9±2,4 |
115,7±1,9* |
99,4±2,1* |
*Примечание: p<0,05, в сравнении с данными предыдущего этапа.
Таблица 2
Уровень эритроцитов у пациенток в различные периоды времени
|
Клиническая группа |
Время забора крови относительно операции |
||
|
48 часов до операции |
3 часа до операции |
Через час после операции |
|
|
Протокол 1 |
3,92±0,27 |
4,01±0,41 |
2,75±0,51 |
|
Протокол 2 |
4,11±0,61 |
4,21±0,15 |
2,99±0,67* |
|
Протокол 3 |
3,75±0,67 |
3,94±0,19 |
3,21±0,21 |
*Примечание: p<0,05, в сравнении с данными предыдущего этапа.
Таблица 3
Уровень гематокрита у пациенток в различные периоды времени
|
Клиническая группа |
Время забора крови относительно операции |
||
|
48 часов до операции |
3 часа до операции |
Через час после операции |
|
|
Протокол 1 |
32,2±2,1 |
31,1±1,4 |
25,5±1,5* |
|
Протокол 2 |
34,1±2,6 |
35,1±2,1 |
26,7±1,7* |
|
Протокол 3 |
31,3±1,9 |
33,9±1,8 |
28,3±3,1* |
* Примечание: p<0,05, в сравнении с данными предыдущего этапа.
Стоит отметить, что показатели крови в 1 группе за 48 часов до операции и накануне операции не имеют достоверной тенденции к изменению, в большую сторону, вследствие того, что пациентки этой группы не получали терапию анемического синдрома. В группах, идущих по протоколам 2 и 3, отмечалось достоверное повышение гемоглобина перед операцией в сравнении с исходным, показатели гематокрита и количества эритроцитов не имели статистически значимых различий, предположительно вследствие того, что у пациенток исходно была диагностирована железодефицитная анемия, как последствия рецидивирующих менометроррагий. Уровень гемоглобина в послеоперационном периоде был достоверно ниже во всех группах, что обусловлено интраоперационной кровопотерей и интроаоперационной гемодилюцией. Но в группе 2 и 3 показатели гемоглобина, гематокрита и количества эритроцитов не выходили за рамки критерия анемии легкой степени тяжести, что позволило избежать гемотрансфузий в интра- и постоперационном периоде. Тогда как в группе, следовавшей протоколу 1, в среднем у пациенток в послеоперационном периоде наблюдалась анемия средней степени тяжести. В I группе в трех случаях из 27 (11,1 %) возникла необходимость в интраоперационном переливании гомологичной крови. В группе, следовавшей протоколу 2, в 4 случаях из 27 возникла необходимость в интраоперационном переливании гомологичной крови (14,8 %). В группе 3 гемотрансфузий не выполнялось. Таким образом, терапия железодефицитной анемии в предоперационном периоде карбоксимальтозатом железа в сочетании с интраоперационным введением транексамовой кислоты позволила избежать трансфузий гомологичной крови в послеоперационном периоде в группе, следовавшей протоколу 3.
В ответ на хирургическую стимуляцию, гипоксию, обусловленную гипоперфузией тканей, активируется симпатическая адренергическая стимуляция и, как следствие, увеличивается продукция глюкозы за счет гликогенолиза в печени. В нашем исследовании достоверных различий по уровню глюкозы до и после операции не выявлено (рисунок 2).
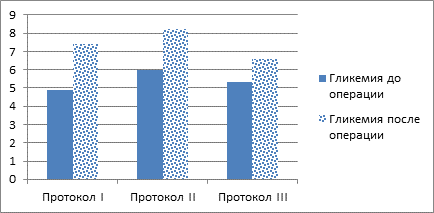
Рис. 2. Сравнение уровня гликемии в до- и послеоперационном периоде
*Примечание: p<0,05, в сравнении с периодом операции.
Также повышенный уровень сывороточного лактата в раннем послеоперационном периоде может отражать наличие интраоперационной тканевой гипоперфузии. Во всех трех группах достоверных различий по уровню сывороточного лактата, в раннем послеоперационном периоде, не было выявлено (рисунок 3). Полученные данные косвенно свидетельствуют об адекватной системной и тканевой перфузии во время проводимых операций, что говорит об адекватной анестезиологической защите пациентов, рациональном применении кровесберегающих технологий при выполнении консервативной миомэктомии.
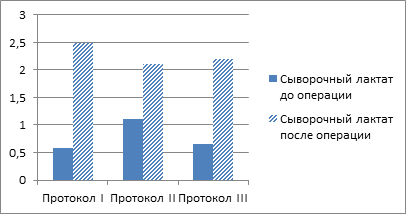
Рис. 3. Динамика оценки уровней лактата до и после операции
*Примечание: p<0,05, в сравнении с периодом операции.
Заключение
Терапия железодефицитной анемии в предоперационном периоде карбоксимальтозатом железа в сочетании с интраоперационным введением ингибиторов фибринолиза позволила избежать трансфузий гомологичной донорской крови.
Величина сывороточного лактата по средним данным сохранялась на нормальных значениях, во всех исследуемых группах, что достигалось адекватной концепцией ведения анестезии, достаточном уровне поддержания перфузии тканей. Частота гиперлактатемии не превышала 1 %.
Библиографическая ссылка
Кочеткова М.В., Сюткина И.П., Королева Е.Г., Смагин А.А., Хабаров Д.В., Демура А.Ю. ИСПОЛЬЗОВАНИЕ КАРБОКСИМАЛЬТОЗАТА ЖЕЛЕЗА И ТРАНЕКСАМОВОЙ КИСЛОТЫ ПРИ ОРГАНОСОХРАНЯЮЩИХ ОПЕРАЦИЯХ В ГИНЕКОЛОГИЧЕСКОЙ ПРАКТИКЕ // Современные проблемы науки и образования. – 2017. – № 5. ;URL: https://science-education.ru/ru/article/view?id=26924 (дата обращения: 20.04.2024).



