Транскраниальная электростимуляция (ТЭС-терапия) – лечебный метод, позволяющий при помощи неинвазивного воздействия током определенных характеристик селективно стимулировать синтез и секрецию β-эндорфина [1]. Активация опиоидэргической системы обладает нейропротекторным, противовоспалительным, антиоксидантным, нейротрофическим и антигипоксическим эффектами [2]. Благодаря этому ТЭС-терапия оказывает благоприятное стресс-лимитирующее влияние на нейроиммуноэндокринную регуляцию и используется для лечения широкого круга заболеваний. Одной из важнейших характеристик благоприятного эффекта ТЭС-терапии является гомеостатический характер действия метода [1-3]. Стресс-лимитирующий потенциал ТЭС-терапии был выявлен во многих экспериментальных и клинических работах, однако вопрос о влиянии ТЭС-терапии на стресс-индуцированую экспрессию гена c-fos мононуклеарными лейкоцитами крови остается недостаточно освещенным [1-5]. Последняя рассматривается в литературе в качестве маркера стресса и провоспалительного статуса и используется для оценки выраженности психических заболеваний [6-8].
Особого внимания заслуживает вопрос о влиянии индивидуальной стрессоустойчивости на характер стресс-индуцированной экспрессии c-fos мононуклеарными лейкоцитами. Ранжирование по стрессоустойчивости является ключевым методологическим приемом исследований, посвященных стрессу. Хорошо известны физиологические отличия низко- и высокоустойчивых животных, к числу которых, например, относится разное медиаторное обеспечение стресс-респонсивных центров мозга [9]. Для исследований, посвященных ТЭС-терапии, эта разделение тем более важно, так как позволяет детализировать представления о гомеостатическом характере действия данного лечебного метода.
Цель работы
Изучение влияния ТЭС-терапии на характер стресс-индуцированной экспрессии гена c-fos мононуклеарными лейкоцитами крыс различной стрессоустойчивости.
Материалы и методы исследования
Объектом исследования были 50 взрослых белых нелинейных самцов крыс массой 200-250 г. Содержание животных, постановка, описание экспериментов и представление полученных результатов проводились в соответствии с требованиями Приказа № 199н МЗ РФ от 01.04.2016 г., рекомендациями ARRIVE (Animal Research: Reporting of InVivo Experiments, 2010) и MIQE (Minimum Information or Publication of Quantitative Real-Time PCR Experiments, 2009) [10; 11].
Период адаптации перед экспериментом для всех крыс составлял 7 дней. Животные интактной группы не включались в эксперимент. Забор материала производился в первый день после адаптации. Оценка выносливости, работоспособности и стрессоустойчивости остальных крыс производилась в первый день после адаптации при помощи модифицированного НЦБМТ РАМН (Научный центр биомедицинских технологий) теста вынужденного плавания (плавательного теста) [12]. Для этого стеклянный аквариум, квадратный в сечении (длина стороны 30 см), заполнялся водой (высота водного столба 40 см, температура воды 28 °C). К хвосту животного прикреплялся груз (10% от массы тела). Животное погружалось в аквариум и после утомления извлекалось из воды. Критериями утомления являлись отказ от плавания, невозможность всплытия на поверхность и адинамия более 10 секунд [12]. Оценка стрессоустойчивости осуществлялась по времени плавания до утомления. Животные, время плавания которых было меньше среднего или превышало среднее более чем на 35%, оценивались как низкоустойчивые и высокоустойчивые соответственно. Далее животные случайным образом разделялись на две группы: основную (ТЭС-терапия по 1 сеансу в день со 2-го по 6-й день, n=20) и группу сравнения (без ТЭС-терапии, n=20). Таким образом, были сформированы три группы: интактная, группа сравнения и основная. Две последние группы включали в себя подгруппы низко- и высокоустойчивых животных. ТЭС-терапия проводилась с помощью модифицированного двухпрограммного электростимулятора «ТРАНСАИР-03» (ООО «Центр транскраниальной электростимуляции», Санкт-Петербург). Продолжительность первого сеанса составляла 15 мин, всех последующих - по 30 мин. [13]. Параметры ТЭС-терапии для крыс представлены в таблице. В качестве подкожных электродов использовались булавки с антикоррозийным покрытием. Электроды располагались фронто-мастоидально (сдвоенный катод – в области лба над глазницами, сдвоенный анод – позади ушных раковин). Предварительно перед установкой электродов место их установки и сами электроды обрабатывались 0,05%-ным водным раствором хлоргексидина [13]. За исключением ТЭС-терапии, все релевантные условия содержания, манипуляции и процедуры, производимые над животными основной группы и группы сравнения, были идентичны.
На 7-й и 8-й дни моделировался комбинированный стресс. Для этого использовались модифицированный тест вынужденного плавания, производимый на 7-й день, и ортостатический стресс на 8-й день. Ортостатический стресс включал в себя фиксацию крыс в специальных футлярах из оргстекла (объем 0,75×10-3 м3) вниз головой под прямым углом к горизонтальной поверхности. Ортостатический стресс сочетался, таким образом, с иммобилизацией. Время пребывания в антиортостатическом положении составляло 45 минут.
Параметры электрического тока, использующегося при проведении ТЭС-терапии в режиме анальгезии у крыс
|
Частота, Гц |
Длительность импульса, мс |
Величина суммарного тока, мА |
|
70±2 |
3,75±0,25 |
1–2,5 |
Забор крови в объеме 2 мл производился через 2 часа после ортостатического стресса в вакуэты с ЭДТА (концентрация 2,7%). Перед этим животное наркотизировалось золетилом 0,8 мг на 100 г веса крысы в/м (Virbac, Франция) и ксиланитом 0,8 мг на 100 г веса крысы в/м («НИТА-ФАРМ», Россия) [13]. Глубина наркоза верифицировалась по угнетению роговичного рефлекса и исчезновению реакции на болевые раздражители.
Мононуклеарные лейкоциты выделялись градиентным центрифугированием. Для этого кровь (1 мл) разбавлялась 1 мл физиологического раствора и наслаивалась на фиколл-верографиновый градиент плотности (ρ=1087 кг/м3) в соотношении 1:1, после чего производилось центрифугирование в течение 20 минут при 2000 об/мин. Отбиралось интерфазное кольцо мононуклеаров. Клетки осаждались центрифугированием в течение 5 минут при 2000 об/мин с последующим удалением надосадочной жидкости.
Экспрессия гена c-fos оценивалась методом полимеразной цепной реакции (ПЦР) в режиме реального времени. Выделение РНК из мононуклеарных лейкоцитов осуществлялось методом гуанидинтиоцианат-фенол-хлороформной экстракции с использованием коммерческого набора ExtractRNA («Евроген», Россия). Концентрацию РНК измеряли при помощи спектрофотометра Picodrop Pico200 (PicodropLtd, UK). Целостность выделенной РНК изучалась при помощи электрофореза в агарозном геле с бромистым этидием.
Для обратной транскрипции на матрице полученной РНК использовался коммерческий набор MMLV RT kit («Евроген», Россия) по инструкции производителя. Определение уровня мРНК гена интереса и референтного гена (actb) проводилось с использованием наборов TaqMan Gene Expression Assays (Applied Biosystems, USA) c-fos:Rn02396759_m1, beta-actin: Rn00667869_m1 (краситель – FAM, гаситель – BHQ).
Амплификационная смесь общим объемом 25 мкл, содержащая 1×TaqMan Gene Expression MasterMix (Applied Biosystems, USA), 1×TaqMan Gene Expression Assays и 5 мкл кДНК, помещалась в прибор для проведения ПЦР в режиме реального времени (Rotor-Gene Q-series, Qiagen, Germany). Режим ПЦР состоял из 2-минутного прогревания смеси при 50 ºC (для активации урацил-N-гликозилазы), 10-минутного прогрева при 95 ºС (активация полимеразы) с последующими 60 циклами: 12 сек денатурации при 95 ºС, 30 сек отжига праймеров при 56 ºС и 20 сек элонгации при 72 ºС. Описанный состав реакционной смеси и режим амплификации были подобраны в ходе предварительной оптимизации. Расчет относительной экспрессии гена c-fos осуществлялся по Livak [14].
Статистическая обработка полученных данных проводилась с помощью пакета программ Statistica (StatSoft, USA). Гипотеза о виде распределения проверялась посредством критерия Шапиро-Уилка. Поскольку закон распределения полученных значений отличался от нормального, данные представлялись как Me(Q1-Q3), где Me – медиана, Q1-Q3 – нижний (25%) и верхний (75%) квартили. Для выполнения задачи сравнения двух независимых групп использовался непараметрический U-критерий Манна-Уитни. Критический уровень значимости нулевой статистической гипотезы принимался равным 0,01 (с учетом проблемы множественных сравнений).
Результаты и обсуждение
Экспрессия гена c-fos в исследуемых клетках была ниже экспрессии гена β-актина во всех случаях. Эффективность амплификации кДНК гена интереса и референтного гена была равной (необходимое условие использования метода Livak). Относительная экспрессия гена c-fos в подгруппе низкоустойчивых животных группы сравнения составила 0,03(0,028–0,1)и была статистически значимо меньше (р=0,002), чем в высокоустойчивой подгруппе (1,3(1–2,9)). Применение ТЭС-терапии сопровождалось статистически значимым (p=0,008) увеличением медианы относительной экспрессии гена c-fos до уровня, сопоставимого с интактным (1(0,1–1,1)) в подгруппе низкоустойчивых животных (рисунок). Таким образом, одним из эффектов данного лечебного метода является благоприятное воздействие на процесс адаптации мононуклеарных лейкоцитов в условиях жесткого комбинированного стресса. В подгруппе высокоустойчивых животных применение ТЭС-терапии сопровождалось статистически значимым (p=0,002) снижением уровня относительной экспрессии гена c-fos (0,15(0,1–0,2). В данном случае имело место предупреждение и подавление мальадаптивной стресс-индуцированной гиперактивации гена c-fos в мононуклеарных лейкоцитах.
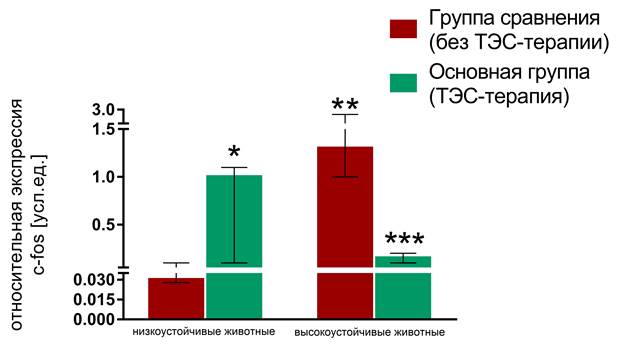
Уровень экспрессии гена c-fos в мононуклеарных лейкоцитах низко- и высокоустойчивых животных основной группы и группы сравнения относительно интактной группы
Примечание: * p=0,008 - по сравнению с низкоустойчивыми животными группы сравнения (без ТЭС-терапии); ** p=0,002 - по сравнению с низкоустойчивыми животными группы сравнения (без ТЭС-терапии); *** p=0,002 - по сравнению с высокоустойчивыми животными группы сравнения (без ТЭС-терапии).
Индивидуальная стрессоустойчивость является значимым фактором, влияющим на характер физиологических изменений при стрессе. У крыс с различной стрессоустойчивостью обнаруживаются значимые отличия в концентрации плазменного кортикостерона, электрической активности мозга, медиаторном обеспечении стресс-респонсивных центров [9]. К примеру, содержание моноаминов в гипоталамусе у высокоустойчивых животных выше, а содержание дофамина в стволовых структурах ниже, чем у низкоустойчивых [9]. В зависимости от стрессоустойчивости разнятся также паттерны активации нейронов стресс-реализующих систем. В паравентрикулярном ядре гипоталамуса после иммобилизации у высокоустойчивых животных наблюдается значительно больше Fos-позитивных клеток по сравнению с низкоустойчивой группой. Эти изменения, отражающие первый этап активации гипоталамо-гипофизарно-надпочечниковой оси, в свою очередь, связаны с разным содержанием моноаминов и глутамата в указанных структурах мозга [9]. Аналогичные паттерны активации – большее количество Fos-позитивных клеток в группе резистентных животных – имеют место также в лимбических структурах при стрессе [15]. Таким образом, многие значимые стресс-индуцируемые изменения в организмах низко- и высокоустойчивых животных имеют противоположную направленность [8]. При этом гипореактивность является характерным свойством низкоустоустойчивых организмов. Особое значение поэтому имеет детальное изучение стресс-лимитирующих лечебных методов, обладающих гомеостатическим характером действия.
Заключение
Уровень экспрессии генов стресса мононуклеарными лейкоцитами крови в значительной мере зависит от индивидуальной стрессоустойчивости организма. Так, низкоустойчивые животные в настоящем исследовании демонстрировали низкий уровень экспрессии гена c-fos, который является одним из проявлений характерной для подобных организмов гипореактивности. Напротив, в мононуклеарных лейкоцитах высокоустойчивых животных имела место стресс-индуцированная гиперактивация гена c-fos. В подгруппе низкоустойчивых животных использование ТЭС-терапии сопровождалось повышением экспрессии гена c-fos до уровня, сопоставимого с интактным. В подгруппе высокоустойчивых животных применение ТЭС-терапии предупреждало и подавляло мальадаптивную стресс-индуцированную гиперактивацию гена c-fos. Эти эффекты являются проявлением системного благоприятного стресс-лимитирующего влияния ТЭС-терапии на нейроиммуноэндокринную систему, имеющего выраженный гомеостатический характер.
Библиографическая ссылка
Каде А.Х., Поляков П.П., Агумава А.А., Гусарук Л.Р., Цымбалов О.В., Алиметов А.Я., Липатова А.С., Вчерашнюк С.П., Кравченко С.В., Шаркова А.В., Черных Н.Ю., Белякова И.С. ВЛИЯНИЕ ТЭС-ТЕРАПИИ НА ХАРАКТЕР СТРЕСС-ИНДУЦИРОВАННОЙ ЭКСПРЕССИИ ГЕНА C-FOS МОНОНУКЛЕАРНЫМИ ЛЕЙКОЦИТАМИ КРЫС РАЗЛИЧНОЙ СТРЕССОУСТОЙЧИВОСТИ // Современные проблемы науки и образования. – 2018. – № 1. ;URL: https://science-education.ru/ru/article/view?id=27389 (дата обращения: 16.04.2024).



