С каждым годом отмечается увеличение количества выполненных операций эндопротезирования крупных суставов. По данным экспертной группы ВОЗ (2012), ежегодно в мире выполняется до 1,5 миллионов тотальных замещений только тазобедренного сустава и, согласно прогнозам, в ближайшие два десятилетия это число может возрасти вдвое [1]. Однако интенсивное внедрение в медицинскую практику данного оперативного вмешательства влечёт за собой неуклонный рост послеоперационных инфекционных осложнений, достигающих при ревизионном протезировании 40% случаев [2].
В настоящее время одним из основных методов лечения поздней глубокой перипротезной инфекции (по классификации M.B. Coventry и D.T. Tsukayama) является двухэтапное ревизионное эндопротезирование [3; 4]. На первом этапе производится удаление инфицированного имплантата и радикальная некрэктомия. В результате проведенной хирургической санации очага нагноения очень часто формируются костные дефекты. Кроме того, повреждение костной ткани возникает и из-за септической нестабильности компонентов эндопротеза, их миграции [5; 6]. Обязательным этапом оперативного лечения образовавшихся костных дефектов является их замещение костным цементом с антибиотиком, что позволяет устранить «мертвое пространство» и предупредить его микробную колонизацию, которая возникает вследствие остаточного бактериального загрязнения [7; 8]. Кроме того, имплантаты, используемые в качестве антибактериальных спейсеров, должны обеспечивать сохранение артикуляции в суставе, что предупреждает развитие контрактур, атрофии мышц и создает благоприятные условия для выполнения второго этапа оперативного лечения поздней глубокой перипротезной инфекции - удаления спейсера и установки ревизионного эндопротеза [9]. Однако даже при прецизионном замещении костного дефекта артикулирующим спейсером частота его вывиха или поломки составляет от 21% до 27,2%, а риск рецидива инфицирования имплантата может достигать 32,3% [4-6]. Одним из инновационных методов решения данной проблемы является использование индивидуальных гибридных эндопротезов, состоящих из титанового и антибактериального костнозамещающего компонентов, изготовленных с помощью компьютерного моделирования и аддитивных технологий 3D-печати. Они позволяют не только заместить имеющиеся костные дефекты у пациента, сохранить функцию сустава до ревизионного эндопротезирования, но и в некоторых случаях могут быть окончательным вариантом лечения без необходимости выполнения повторного оперативного вмешательства.
Цель исследования – оценить клинико-рентгенологические результаты оперативного лечения пациентов с использованием индивидуальных гибридных эндопротезов, изготовленных с помощью аддитивных технологий 3D-печати.
Материалы и методы исследования. Работа основана на проведении клинического и рентгенологического обследования 15 пациентов с перипротезной инфекцией после первичного эндопротезирования тазобедренного, коленного или плечевого суставов, проходивших лечение в отделении гнойной хирургии (остеологии) института травматологии и ортопедии ФГБОУ ВО «ПИМУ» Минздрава России. Во всех случаях применялась методика двухэтапного ревизионного эндопротезирования с установкой на первом этапе индивидуального гибридного эндопротеза. Средний возраст пациентов составил 59,4 ± 9,3 года. Среди оперированных больных было 3 (25%) мужчин и 12 (75%) женщин. Все пациенты до операции ежедневно принимали пероральные анальгетики.
Больные были разделены на 3 группы в зависимости от локализации оперативного вмешательства: 1 группа - после эндопротезирования тазобедренного сустава (n=5), 2 группа - после эндопротезирования коленного сустава (n=5), 3 группа - после эндопротезирования плечевого сустава (n=5).
У всех пациентов имелись клинико-лабораторные признаки перипротезной инфекции, включающие наличие свищевой раны с гнойным отделяемым, рост патогенной микрофлоры после бактериального посева пунктата сустава. Микробиологические исследования проводились в бактериологической лаборатории ФГБОУ ВО «ПИМУ» Минздрава России.
На этапе предоперационной подготовки всем пациентам выполнялось рентгенологическое и компьютерно-томографическое (КТ) обследование сустава. КТ производилось как пораженного, так и патологически неизмененного контрлатерального сустава.
Создание индивидуального гибридного эндопротеза производилось по разработанной в ООО «ГИТО-ИННОВАЦИЯ» методике и включало на первом этапе получение информации для восстановления образа костных структур определенной плотности из массива томографических данных путем установки в компьютерной программе «3D Slicer» уровня отсечки, задавая коэффициент градиента интенсивности эмпирически. Также производилось отсеивание вокселей с информацией об имевшемся у пациента имплантате.
На втором этапе после построения компьютерной трехмерной модели сустава в программном обеспечении «Autodesk Meshmixer» производилось его гибридное параметрическое моделирование. Затем выполняли замещение костного дефекта, используя данные компьютерной томографии неповрежденного контрлатерального сустава. После этого осуществлялась топологическая оптимизация костнозамещающего имплантата в соответствии с реперными точками, которые отличались в зависимости от моделируемого сустава. Для тазобедренного сустава они соответствовали следующим анатомическим ориентирам: передняя нижняя подвздошная ость, ямка вертлужной впадины, вырезка вертлужной впадины, подвздошно-лобковое возвышение, надвертлужная борозда, головка бедренной кости, верхняя ветвь лобковой кости, седалищный бугор, ость седалищной кости, передний край вертлужной впадины, задний край вертлужной впадины, верхний край вертлужной впадины, нижний край вертлужной впадины. Реперными точками для моделирования коленного сустава являлись следующие анатомические образования: латеральный мыщелок бедренной кости, медиальный мыщелок бедренной кости, межмыщелковая ямка, латеральный надмыщелок бедренной кости, медиальный надмыщелок бедренной кости, приводящий бугорок, бугристость большеберцовой кости, латеральный мыщелок большеберцовой кости, медиальный мыщелок большеберцовой кости, межмыщелковое возвышение. Моделирование плечевого сустава производилось с применением следующих реперных точек: акромион, клювовидный отросток лопатки, подсуставной бугорок лопатки, надсуставной бугорок лопатки, вырезка лопатки, шейка лопатки, акромиально-ключичный сустав, передний край гленоидальной впадины, задний край гленоидальной впадины, верхний край гленоидальной впадины, нижний край гленоидальной впадины.
На третьем этапе после создания трехмерной модели костнозамещающего компонента гибридного эндопротеза производилось моделирование формы для его изготовления, внутренняя поверхность которой повторяла созданную модель, наружная часть для удобства имела форму куба с толщиной стенки 1 см. Затем на внутренней поверхности компьютерной трехмерной модели формы костнозамещающего компонента гибридного эндопротеза сустава создавались сферические возвышения высотой 1-5 мм. Они в последующем обеспечивали более лучшую адгезию костного цемента. После этого производилось разделение трехмерной модели формы на 3 части с последующей их 3D-печатью на FDM 3D-принтере и стерилизацией.
На четвертом этапе интраоперационно форма собиралась в единое целое, и в нее заливался костный цемент с антибиотиком. После его отвердения форму демонтировали, сформированный костнозамещающий компонент гибридного эндопротеза имплантировали в область костного дефекта на костный цемент с антибиотиком. После этого устанавливался титановый и при необходимости полиэтиленовый компоненты эндопротеза. При создании гибридного эндопротеза плечевого сустава перед импакцией костного цемента в форму, в нее устанавливался титановый стержень, который армировал плечевой компонент эндопротеза.
После выполнения операции всем пациентам проводилась антибактериальная терапия в соответствии с результатом антибиотикограммы. В зависимости от состояния параартикулярных тканей, наличия признаков воспаления на 4-7-е сутки производилась активизация больных, проводился курс лечебной физкультуры. На контрольных осмотрах через 1, 2 и 3 месяца после эндопротезирования больным выполнялась рентгенография оперированного сустава в двух проекциях, оценивался локальный статус, результаты лабораторных исследований. Также осуществлялся посев на стерильность пунктата оперированного сустава. При отсутствии данных за наличие рецидива перипротезной инфекции выполнялся второй этап оперативного лечения - ревизионное эндопротезирование.
Статистическая обработка цифрового материала результатов исследования выполнена с использованием программы Microsoft Offie Excel 2010, статистического пакета Statistica 10.0 (STATSOFT, США). Проверка нормальности распределения проводилась методом Шапиро-Уилка. Непараметрический метод - тест Манна-Уитни (U) для несвязанных групп использовали в тех случаях, когда значения анализируемых данных не соответствовали нормальному закону распределения или показатели носили дискретный характер. Для сравнения двух связанных (парных) выборок с целью оценки динамики лечения использовался Т-критерий Вилкоксона. Нулевые гипотезы отвергались при достигнутом уровне значимости соответствующего статистического критерия p<0,05.
Результаты исследования и их обсуждение. При оценке послеоперационных результатов лечения пациентов с использованием индивидуальных гибридных эндопротезов статистически достоверно (p<0,05) в каждой группе отсутствовали неинфекционные осложнения, включая вывихи, миграцию компонентов эндопротеза, переломы костнозамещающего компонента. Также не было выявлено ни одного случая рецидива периимплантной инфекции, что статистически достоверно (p<0,05) подтверждает положительную динамику в лечении пациентов и эффективность использования индивидуальных гибридных эндопротезов (таблица).
Результаты лечения пациентов с использованием индивидуальных гибридных эндопротезов
|
№ группы |
Количество пациентов с инфекционными осложнениями до операции |
Количество пациентов с инфекционными осложнениями через 3 месяца после операции |
Количество пациентов с неинфекционными осложнениями через 3 месяца после операции |
|
1 (n=5) |
5 |
0 |
0 |
|
2 (n=5) |
5 |
0 |
0 |
|
3 (n=5) |
5 |
0 |
0 |
Полностью отказались от приема обезболивающих препаратов 73% (n=11) пациентов. Пероральные НПВС 4-5 раз в неделю принимал только 1 пациент после эндопротезирования тазобедренного сустава, что, по нашему мнению, обусловлено длительным анамнезом заболевания (более 20 лет), обширным дефектом костей таза (III B по классификации W. Paprosky). Пероральные обезболивающие препараты 1-2 раза в неделю принимало трое пациентов (один - после эндопротезирования тазобедренного сустава, двое - после эндопротезирования коленного сустава).
Все пациенты после эндопротезирования коленного и тазобедренного суставов передвигались с помощью костылей с частичной опорой на оперированную конечность. У всех больных после эндопротезирования плечевого сустава сохранилась артикуляция в нем.
При сравнении полученных результатов с данными исследований различных авторов выявлено преимущество использования индивидуальных гибридных эндопротезов, создаваемых по разработанной методике, в лечении перипротезной инфекции по сравнению с применением спейсеров, изготовленных по традиционным технологиям. Например, в исследовании J. Jung с соавторами частота механических осложнений после имплантации спейсера тазобедренного сустава выявлена в 40,8% случаев (17% вывихов, 10,2% поломок спейсера, 13,6% переломов бедра) [10]. М. Faschingbauer с соавторами изучили результаты лечения 138 больных, которым устанавливались спейсеры. В результате исследования было выявлено 19,6% неинфекционных осложнений, включая 8,7% разрушений имплантатов, 8,7% вывихов, 0,7% переломов бедренной кости, 0,7% миграций компонентов эндопротеза в таз, 0,7% поломок и вывихов спейсера [11]. Однако необходимо проведение дополнительных сравнительных исследований на большем количестве пациентов.
Для демонстрации результатов применения индивидуальных гибридных эндопротезов в лечении перипротезной инфекции приводим следующий клинический пример.
Клинический пример. Больной М., 38 лет, диагноз: глубокое нагноение после тотального эндопротезирования левого тазобедренного сустава. На этапе предоперационной подготовки по результатам рентгенологического и КТ обследования диагностированы значительные дефекты дна и крыши вертлужной впадины (рис. 1).
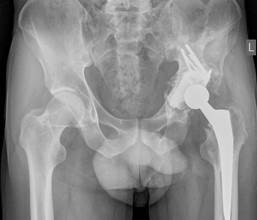
Рис. 1. Обзорная рентгенограмма таза
С использованием данных КТ выполнено создание трехмерной модели таза. Затем осуществлено компьютерное моделирование костнозамещающего ацетабулярного компонента гибридного эндопротеза тазобедренного сустава и формы для его создания с наличием на ее внутренней поверхности 10 сферических возвышений высотой 1 мм. После этого она была изготовлена на FDM 3D-принтере. Затем интраоперационно создан внутренний барьерный слой формы из асептической пленки, изготовлен костнозамещающий ацетабулярный компонент, выполнена его имплантация. В костнозамещающий вертлужный компонент эндопротеза установлена полиэтиленовая чашка диаметром 52 мм на костный цемент с антибиотиком. После этого произведена имплантация индивидуально подобранного бедренного компонента. Осуществлено его вправление. Тенденции к вывиху нет. Движения в суставе осуществляются в полном объеме (рис. 2).
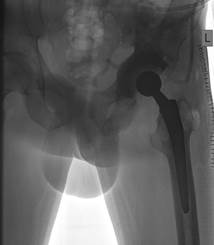
Рис. 2. Рентгенограмма левого тазобедренного сустава после операции
Пациент был выписан через 6 суток после операции. Рана зажила первичным натяжением. Рецидива воспалительного процесса не было. Через 3 месяца после операции пациенту выполнен 2-й этап оперативного лечения - ревизионное эндопротезирование левого тазобедренного сустава.
Выводы. Применение индивидуальных гибридных эндопротезов в ревизионном эндопротезировании тазобедренного, коленного и плечевого суставов позволяет прецизионно заместить дефекты костной ткани и сохранить движения в суставе.
Проведенная оценка клинико-рентгенологических послеоперационных результатов лечения больных с использованием персонифицированных гибридных эндопротезов, изготовленных с помощью аддитивных технологий 3D-печати, не выявила ни одного случая рецидива периимплантной инфекции, а также развития неинфекционных осложнений, включая вывихи, миграцию компонентов эндопротеза, переломы костнозамещающего компонента имплантата.
Исследование выполнено при финансовой поддержке гранта «Фонда содействия инновациям» (Договор (Соглашение) № 26ГС1НТИС5/43261 от 18.09.2018).
Библиографическая ссылка
Горбатов Р.О., Клеменова И.А., Новиков А.В., Зиновьев С.В., Казаков А.А. РЕВИЗИОННОЕ ЭНДОПРОТЕЗИРОВАНИЕ КРУПНЫХ СУСТАВОВ С ИСПОЛЬЗОВАНИЕМ ИНДИВИДУАЛЬНЫХ ГИБРИДНЫХ ЭНДОПРОТЕЗОВ // Современные проблемы науки и образования. – 2019. – № 4. ;URL: https://science-education.ru/ru/article/view?id=29095 (дата обращения: 20.04.2024).



