Астаксантин (АСТ), называемый красным морским витамином, является провитаминным каротиноидом, который содержится в красном пигменте креветок, крабов и лосося и обладает многими важными биологическими функциями, такими как антиоксидантная и противовоспалительная активность [1]. Биологическая активность AСT выше, чем у альфа-токоферола и бета-каротина [2], поэтому этот антиоксидант представляет большой интерес для исследований. Это наблюдение относится к нейродегенерации и защите когнитивной функции, поскольку эффективность этих ферментов уменьшается с возрастом [3]. АСТ может эффективно смягчать окислительный стресс, возникающий при различных патологических состояниях, и предотвращать вызванную окислительным стрессом митохондриальную дисфункцию [4].
Матупала и сотрудники показали, что в некоторых опухолевых клетках наблюдается высокий уровень экспрессии VDAC1, поэтому этот белок можно считать антираковой мишенью [5]. Транслокаторный белок (TSPO) тесно связан с VDAC1 и считается его партнером. Было доказано, что уровень TSPO повышался в раковых клетках, клетках мозга [6] и в других органах.
Серин-треониновая протеинкиназа В (Akt) является основной мишенью для регулирования роста клеток. Активированная Akt (фосфо-Akt) перемещается в цитоплазму и ядро, где фосфорилирует, активирует или ингибирует множество мишеней для регуляции различных клеточных функций [7]. Известно, что активированная Akt способствует клеточной пролиферации и ингибирует апоптоз [8].
Цель настоящей работы состояла в том, чтобы исследовать влияние АСТ на пролиферацию и индукцию дифференцировки клеток нейробластомы мыши N1E-115 (клон C-1300), а также оценить корреляцию изменения пролиферации с изменением уровней белков TSPO и VDAC1 под действием АСТ. Кроме того, мы изучили влияние АСТ на изменение активированной протеинкиназы В (Akt) в клеточных лизатах нейробластомы.
Материал и методы исследования. Клеточная культура нейробластомы мыши N1Е115 (клон С-1300) была взята из Российской коллекции клеточных культур ИНЦ РАН, Санкт-Петербург. Клетки выращивали по методике С.В. Мякишевой, описанной в [9]. Среду DМЕМ без сыворотки применяли в качестве контроля. АСТ добавляли в культуральную среду через 24 ч после посева клеток. После добавления АСТ (Sigma, США) к клеткам определяли общее число клеток, число пролиферирующих, дифференцирующих и погибших клеток через 24 и 72 ч. Оценку дифференцирующего действия проводили на основе морфологического изменения клеток [9]. Для этого осуществляли подсчет клеток, образующих отростки, длина которых более чем в 2 раза превышала диаметр клеточной сомы. Морфологический анализ клеток и микрофотографии проводили при помощи флуоресцентного микроскопа Ti-E (Nikon, Япония) [9].
Клеточные лизаты готовили, как описано в [9]. Супернатанты солюбилизировали в 4-кратном Лэммли буфере. Электрофорез в денатурирующих условиях проводили по методу Лэммли, описанному в [9]. Перенос белков с геля на мембрану (нитроцеллюлоза, Bio-Rad, США, 0,2 мкм) осуществляли методом Вестерн-блот. Определение изменения уровня исследуемых белков проводили при помощи коммерческих антител: Bcl-2 (Santa Cruz, США), BAX (Abcam, Великобритания), VDAC1 (Novus biologicals, США), TSPO (Abcam, Великобритания), p-Akt (Ser 437) (Cell Signalling, Нидерланды) и Akt (Cell Signalling, Нидерланды). Анти-β-тубулин (Cell Signaling, Нидерланды) использовали как контроль белковой нагрузки. Пероксидазную активность определяли хемилюминесцентными реагентами ECL (Bio-Rad, США) [9]. Количественный анализ интенсивности белковых полос проводили с помощью денситометрии (программа Image Lab, Bio Rad, США).
Результаты проведенных экспериментов представляли как среднее значение ± стандартное отклонение (±SD) после четырех повторов (n≥4). Значимость (*) – р<0,05 относительно контроля (без АСТ) считали по t‑критерию Стьюдента.
Результаты исследования и их обсуждение. В настоящем исследовании было изучено влияние АСТ на изменение пролиферации в клетках нейробластомы мыши N1E-115 (клон C-1300) и изменение уровня белков, таких как Bcl-2, ВАХ, VDAC1, TSPO р-Akt и Akt, в этих условиях. Сначала мы проанализировали действие различных концентраций АСТ на клетки нейробластомы. Для этого клетки обрабатывали АСТ в течение 96 ч в различных концентрациях (10-2, 10-3, 10-4, 10-5, 10-6, 10-7 М) (рис. 1). Нами была выбрана максимальная нетоксичная концентрация АСТ, равная 1 мМ.
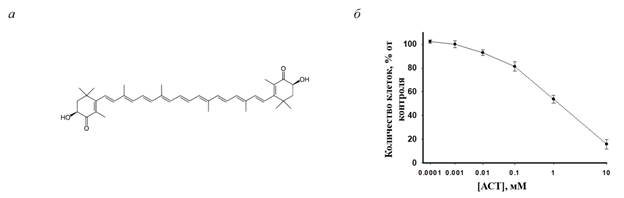
Рис. 1. а – Химическая структурная формула АСТ; б – Концентрационная зависимость цитотоксических эффектов АСТ
Такая высокая доза АСТ необходима для достижения субклеточных концентраций, достаточных для оказания фармакологических эффектов. Затем мы оценили пролиферативную активность клеток нейробластомы, обработанных АСТ в течение 72 ч (рис. 2). На рисунке 2а показана влияние АСТ на морфологические изменения клеток нейробластомы после 24 и 72 ч культивирования.
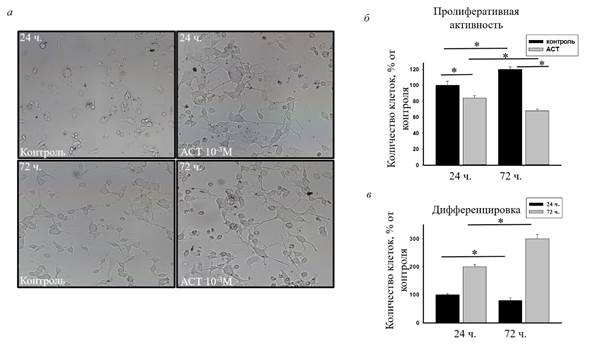
Рис. 2. а – Микрофотографии клеток после инкубации с АСТ в течение 24 (верх) и 72 ч (низ) по сравнению с контролем (без АСТ), б – диаграмма, показывающая изменение количества пролиферирующих клеток; в – изменение числа дифференцирующих клеток
Рисунок 2б отражает изменение пролиферативной активности клеток нейробластомы. Результаты изменения числа дифференцирующих клеток при добавлении в инкубационную среду АСТ показаны на рисунке 2в. Из рисунка 2в видно, что после 24 ч инкубации АСТ снижал количество пролиферирующих клеток на 20%, а через 72 ч культивирования – на 45%, тогда как количество клеток в среде, не содержащей АСТ, через 72 ч после культивирования увеличивалось на 20% по сравнению с контролем (100%, 24 ч культивирования, без АСТ). АСТ снижал пролиферативную активность клеток нейробластомы. В культурах контрольных клеток число погибших клеток не увеличивалось и составляло 1,5–2%. После 24 и 72 ч инкубации АСТ не усиливал гибель клеток, она составляла 2,5–3% (данные не показаны). Добавление АСТ усилило дифференцировку клеток в 2 раза через 24 ч культивирования по сравнению с контролем (100%, 24 ч культивирования, без АСТ), тогда как через 72 ч при добавлении АСТ число дифференцирующих клеток увеличивалось в 3 раза (рис. 2в).
Далее мы проверили изменение уровней белков семейства Bcl-2, таких как Bcl-2 и BAX, которые считаются анти- и проапоптотическими в наших экспериментальных условиях. На верхней части рисунка 3а показаны Вестерн-блоты Bcl-2 и BAX в лизированных клетках, обработанных и не обработанных АСТ в течение 24 и 72 ч культивирования.
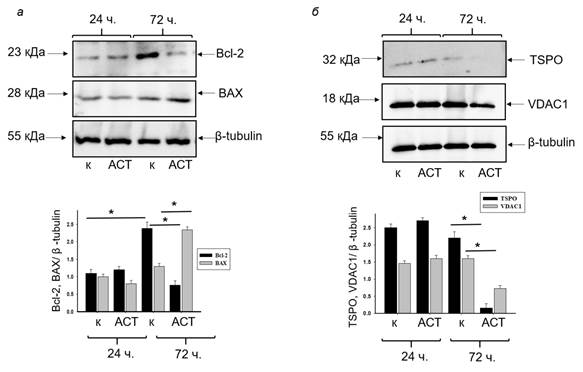
Рис. 3. Изменение уровня белков Bcl-2 и BAX, VDAC1 и TSPO в лизатах клеток нейробластомы после 24 и 72 ч культивирования в средах, содержащих АСТ, по сравнению с контролем: иммуноблоты, окрашенные соответствующими антителами (верх); диаграммы, отражающие соотношение Bcl-2 и BAX, VDAC1 и TSPO, нормированные на анти-β-тубулин (низ)
Количественное соотношение белковых полос оценивали по нормированию на анти-β-тубулин (рис. 3а нижняя панель). Через 72 ч культивирования мы наблюдали, что уровень Bcl-2 в клетках нейробластомы в контрольных условиях увеличивался в 2 раза. Содержание Bcl-2 в присутствии АСТ значимо не отличалось от контроля через 24 ч культивирования, однако через 72 ч культивирования АСТ способствовал снижению уровня Bcl-2 на ~40%. После 72 ч культивирования уровень BAX в контрольных условиях не изменялся (24 ч культивирования), однако под действием АСТ экспрессия ВАХ увеличивалась приблизительно в 2 раза. Полученные результаты подразумевают активацию каскада, приводящую к клеточной гибели [10].
Известно, что TSPO и его лиганды (РК11195, Ro 5-4864) считаются молекулярной мишенью при лечении онкологических заболеваний, лиганды TSPO способны проявлять антираковые свойства [9, 11] и участвуют в активации клеточной пролиферации [12]. Вероятно, изменение экспрессии TSPO влияет на туморогенность клеток. В настоящем исследовании мы наблюдали, что АСТ повышал уровень TSPO в клетках нейробластомы, что предполагает участие АСТ в развитии опухоли.
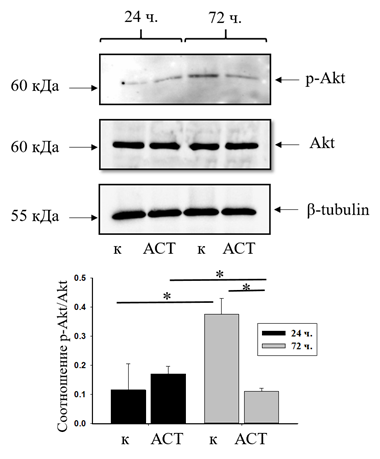
Рис. 4. Уровень фосфорилирования активированной протеинкиназы В (Akt). В верхней части показаны иммуноблоты, окрашенные антителами к p-Akt и Akt, в нижней части представлена диаграмма, отражающая изменение в соотношении p-Akt к Akt в абсолютных единицах. Анти-β-тубулин использовали как контроль белковой нагрузки
Это может привести к повышению пластических процессов, происходящих в опухолевых клетках, и к изменениям механизмов передачи сигнала через биологические мембраны [12]. Ранее мы исследовали совместное действие мелатонина с противоопухолевым препаратом, ретиноевой кислотой и наблюдали снижение уровней TSPO и VDAC1 в клетках HL-60 [12]. Молекулярные взаимодействия про- и антиапоптотических белков с VDAC являются разнообразными, более того, они могут как способствовать гибели клеток, так и предотвращать ее. Митохондриальный VDAC считается основным компонентом, который рассматривается как мишень для противоопухолевой терапии. Было показано, что VDAC способен инициировать сигнальные каскады, приводящие к апоптозу [13], а Матупала и соавторы заключили, что VDAC1 может рассматриваться как мишень противоопухолевого действия [5]. Поэтому в настоящем исследовании мы оценили изменение уровней TSPO и VDAC1 в выбранных нами условиях (рис. 3б). На рисунке 3б показано, что в присутствии АСТ уровни и TSPO, и VDAC1 снижались в 13 и 2 раза соответственно через 72 ч культивирования. Можно предположить, что АСТ способствует снижению экспрессии TSPO и VDAC1 и способен вызывать снижение онкогенности.
Известно, что Akt способна регулировать рост клеток. Кроме того, активированная Akt индуцирует клеточную пролиферацию и предотвращает развитие программируемой гибели клеток [9]. Регуляторное влияние АСТ на PI3K/Akt в настоящее время интенсивно исследуется. Ранее С.Х. Ким и Х. Ким наблюдали, что АСТ ингибировал клеточную пролиферацию и индуцировал апоптоз в клетках некоторых типов карцином, уменьшая соотношение p-Akt/Akt, тем самым подавляя нисходящие пути передачи сигналов Akt, такие как NF-κB, Wnt и STAT3 [14]. В настоящем исследовании мы проверили изменение активированной Akt в наших экспериментальных условиях. Мы заметили, что в контрольных клетках нейробластомы через 72 ч после культивирования соотношение р-Akt/Akt увеличивалось в 3 раза по сравнению с клетками нейробластомы, культивированными через 24 ч. АСТ не изменял соотношение р-Akt/Akt ни через 24, ни через 72 ч инкубации, и оно не отличалось от контрольного значения спустя сутки после культивирования. АСТ ингибировал активацию р-Akt, тем самым снижая пролиферативную активность клеток нейробластомы.
Заключение. Результаты исследований показывают, что АСТ подавляет пролиферацию клеток нейробластомы, в то же время усиливая их дифференцировку. Мы обнаружили, что АСТ способен регулировать уровни анти- и проапоптотических белков в митохондриях, что предполагает его участие в активации сигнального пути апоптоза. Также показана способность АСТ снижать экспрессию митохондриальных белков TSPO и VDAC1 в опухолевых клетках, что, вероятно, уменьшает онкогенность. АСТ ингибировал активацию р-Akt, тем самым снижая пролиферативную активность клеток нейробластомы. Таким образом, АСТ может считаться перспективным агентом при разработке новых терапевтических подходов для предотвращения онкозаболеваний.
В настоящей работе были использованы приборы ЦКП ИТЭБ РАН.
Работа поддержана грантами РФФИ №№ 20-04-00131, 20-015-00072.
Библиографическая ссылка
Мякишева С.Н., Бабурина Ю.Л., Крестинина О.В. АСТАКСАНТИН МОЖЕТ ВЛИЯТЬ НА РОСТ И РАЗВИТИЕ КЛЕТОК МЫШИНОЙ НЕЙРОБЛАСТОМЫ N1Е-115 (КЛОН С-1300) // Современные проблемы науки и образования. – 2020. – № 4. ;URL: https://science-education.ru/ru/article/view?id=29943 (дата обращения: 24.04.2024).



