Анализ опубликованных за последние годы работ по применению магнитных наночастиц показывает актуальность и практическую значимость этих объектов [6; 8; 9]. Адсорбционные процессы с использованием данного типа частиц привлекают внимание исследователей в связи с возможностью их использования в биомедицинских технологиях [8; 9] и в процессах водоочистки [5; 10].
Среди различных типов сорбентов все большее внимание привлекают углеродосодержащие сорбенты. Они отличаются высокими сорбционными свойствами, что позволяет использовать такие сорбенты для избирательного извлечения компонентов из растворов, а также как магнитоуправляемые носители лекарственных препаратов в медицине. Известно, что применение химиопрепаратов в терапии онкологических заболеваний приводит не только к лечебному эффекту, но и к возникновению тяжелых осложнений. В связи с этим в фармации возникает новое направление, связанное с созданием лекарственных форм на основе магнитных наночастиц.
Работы по созданию магнитных лекарственных форм проводятся в настоящее время по нескольким направлениям [1], одно из которых связано с «прямой посадкой», то есть с адсорбцией лекарственного вещества на поверхность магнитного носителя [1; 2]. Это направление обладает рядом преимуществ, связанных, прежде всего, с простотой и высокой скоростью получения магнитных лекарственных форм. Обзор [6; 8; 9] периодических изданий по сорбционным процессам на углеродосодержащих сорбентах показал, что данное направление довольно новое и требует более детального изучения механизма процесса.
В связи с этим целью настоящей работы является исследование кинетических и электрокинетических свойств процесса адсорбции органических молекул на железоуглеродном сорбенте, полученном методом электроискрового диспергирования железных гранул в гексане.
Материалы и методы исследования
Наноразмерный железоуглеродный сорбент (ЖУС) был получен в результате электроискрового диспергирования железных гранул в гексане. Методика импульсного диспергирования, схема установки, геометрия реактора подробно описаны нами в работах [7; 8]. Полученную суспензию, состоящую из ЖУС и среды диспергирования, разделяли на фракции с использованием центрифугирования. Крупную фракцию, выпадающую в осадок при числе оборотов до 5000 об/мин [5], использовали для процессов адсорбции неорганических ионов, оставшуюся часть ЖУС использовали для изучения процессов адсорбции органических адсорбатов для последующего использования в медицинских целях (размер наночастиц, используемых в медицинских целях, не должен превышать 1 мкм [1]).
Значение заряда поверхности (x-потенциал) определяли с использованием метода движущейся границы [7]. В качестве адсорбатов использовали следующие органические соединения:
C27H29NO11×HCl → [C27H29NO11]H+ + Cl- - гидрохлорид доксорубицина (ДР);
C9H11F2N3O4×HCl → [C9H11F2N3O4]H+ + Cl- - гидрохлорид гемцитабина (гемзар, ГЕМ);
NaC4H3FN2O2 → Na+ + [C4H3FN2O2]- - фторурацил (ФУ);
C7H15Cl2N2O2P - циклофосфан (ЦФ);
С16Н18ClN3S×HCl → [С16Н18ClN3S]H+ + Cl- - метиленовый голубой, катионный краситель;
Na2[С20Н6О5Br4] →2Na+ + [С20Н6О5Br4]2- - эозин, анионный краситель.
При изучении адсорбционных свойств использовали статический метод сорбции из растворов. Адсорбцию проводили при 20 °С в течение 48 ч. Исходную и равновесную концентрации адсорбатов определяли фотометрически с использованием спектрофотометра Apel PD-300UV. По результатам исследований были получены изотермы адсорбции, определена максимальная сорбционная емкость (А¥) образцов и константа сорбционного равновесия (К). Для оценки значения энергии активации адсорбции (Еак) на примере доксорубицина были измерены величины адсорбции А при различных температурах. Значение энергии активации оценивалось по уравнению Аррениуса в координатах lnVадс - 1/T (Vадс - скорость адсорбции).
Для определения характера взаимодействия препарата и носителя были записаны инфракрасные спектры диффузного отражения с использованием ИК-спектрометра Nicolet 5700 в диапазоне 400...4000 см-1.
Результаты исследования и их обсуждение
В данной работе была исследована адсорбция органических молекул на железоуглеродном сорбенте, изотермы адсорбции представлены на рис. 1. Из представленных изотерм видно, что для катионных адсорбатов характерны высокие значения сорбции. Электронейтральные и анионные формы адсорбатов не сорбируются (схемы диссоциаций приведены выше). Это может свидетельствовать об электростатическом взаимодействии адсорбата с поверхностью сорбента.



Рис. 1. Изотермы адсорбции:
а) доксорубицина; б) гемзара; в) метиленового голубого.
При адсорбции катионных форм адсорбатов для установления адсорбционного равновесия требуется не менее 48 ч, что может быть связано с наличием диффузионного и кулоновского барьеров, возникающих при прохождении органических катионов через одноименно заряженный диффузный слой Гуи-Чепмена и/или с химическим превращением при хемосорбции.
Для подтверждения электростатической природы механизма адсорбции были проведены эксперименты по изучению изменения потенциала поверхности с адсорбированными органическими ионами. При достижении максимального значения адсорбции для всех систем происходит изменение не только величины, но и знака x-потенциала (табл. 1).
Таблица 1 - Сорбционные характеристики и заряд поверхности железоуглеродных наночастиц (ЖУС)
|
Образец |
М адсорбата, г/моль |
Сорбционные характеристики |
x-потенциал, мВ |
||
|
А, мкмоль |
К, л/мкмоль |
Количество десорбир-го адсорбата, % |
|||
|
ЖУС+Н+ |
1 |
- |
- |
- |
-68±2 |
|
ЖУС+доксорубицин |
543 |
82,6 |
0,796 |
0 |
+22±2 |
|
ЖУС+гемзар |
282 |
416,6 |
0,0052 |
5,2 |
+34±2 |
|
ЖУС+метиленовый голубой |
319,5 |
115,0 |
0,11 |
0,45 |
+35±2 |
Предположительно причиной перезарядки может быть не только адсорбция ионов по электростатическому механизму, но и наличие специфической адсорбции. В то же время вся совокупность данных свидетельствует об определяющей роли заряда поверхности в адсорбции, так как на отрицательно заряженной поверхности адсорбируются только катионные формы органических молекул. Определение электро-кинетического потенциала, проведенное в изоионном состоянии, то есть в условиях, когда равновесие определяется только диссоциацией воды и твёрдой фазы, показало, что частицы образца заряжены отрицательно, причём абсолютное значение x-потенциала составляет -68±2мВ (табл. 1).
В связи с этим заряд поверхности и сорбционные свойства определяются процессами диссоциации или адсорбции поверхностных гидроксильных групп:
-Fe-C-СООН→-Fe-C-СОО-+Н+
Исходя из значения полученного ζ-потенциала, структуру мицеллы наночастицы в воде можно представить: {[m(Fe,FeC,Fe3C)]·nOH-·(n-x)H+}x-·хH+
При адсорбции доксорубицина наблюдается постепенное изменение значения дзета-потенциала, и при концентрации ДР более 16·10-6 моль/г происходит смена знака заряда поверхности. С учетом полученных данных по перезарядке поверхности ЖУС можно представить структуру мицеллы после адсорбции ДР следующим образом:
{[m(Fe,FeC,Fe3C)]·nOH- ·(n-x)DOX}х+·хOH-
Для подтверждения предположения о формировании прочного поверхностного соединения железоуглеродного сорбента и органических молекул были записаны ИК-спектры диффузного отражения как ЖУС, индивидуальных веществ, так и адсорбированных на ЖУС органических молекул (рис. 2).
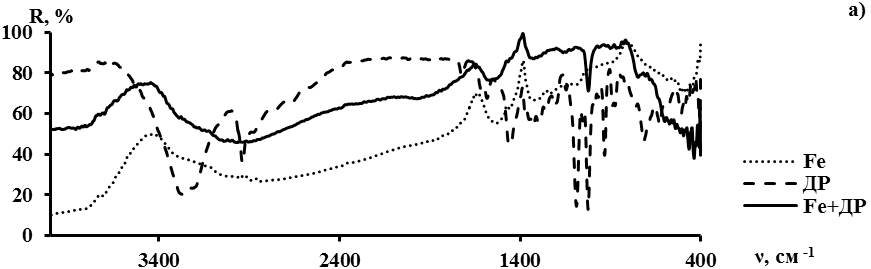
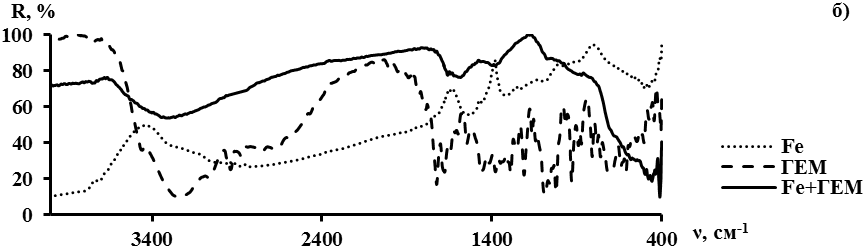
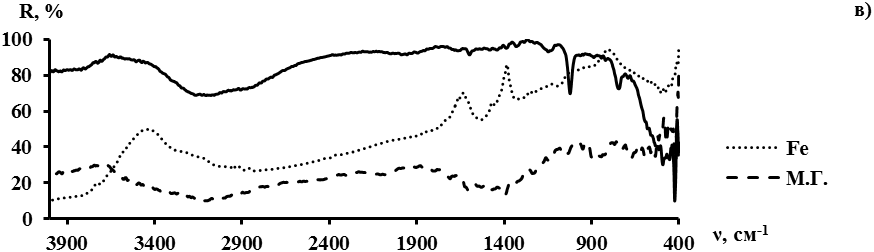
Рис. 2. ИК-спектры диффузного отражения: а) железоуглеродный сорбент, доксорубицин, доксорубицин, адсорбированный на железоуглеродном сорбенте; б) железоуглеродный сорбент, гемзар, гемзар, адсорбированный на железоуглеродном сорбенте; в) железоуглеродный сорбент, метиленовый голубой, метиленовый голубой, адсорбированный на железоуглеродном сорбенте.
Из рис. 2 видно, что в адсорбированном состоянии адсорбаты сохраняют только характеристические полосы поглощения деформационных колебаний связи С-Н (группа полос в области 950...550 см-1 и 1020...1030 см-1). Отсутствие характеристических полос валентных колебаний карбонильных и амидных и др. функциональных групп свидетельствует об их участии в образовании химического соединения на поверхности ЖУС. Очевидно, образование продуктов взаимодействия сорбента с доксорубицином, гемзаром и метиленовым голубым происходит не только по электростатическому, но и по обменному механизму ОН- групп поверхности ЖУС с функциональными группами, входящими в состав органических адсорбатов.
В настоящей работе для определения величины энергии активации были получены кинетические зависимости изменения концентрации ДР при адсорбции на ЖУС при различных температурах. Из полученных данных были рассчитаны значения констант скоростей адсорбции и десорбции, значение энергии активации, данные приведены в табл. 2.
Таблица 2 - Значения кинетических параметров процесса сорбции доксорубицина на железоуглеродном сорбенте
|
Температура сорбции, °C |
Kадс, мин-1 |
Кдес, мин-1 |
Ea, кДж/моль |
|
18 |
0,0013 |
0,00072 |
29 |
|
40 |
0,0032 |
0,00080 |
|
|
60 |
0,0052 |
0,00085 |
Экспериментальное значение энергии активации адсорбции составило 29 кДж/моль - значение, промежуточное между энергией активации диффузионно лимитированного процесса (около 5...10 кДж/моль) и активационного барьера хемосорбционных процессов (который может составлять до 40 кДж/моль - для адсорбции при комнатных температурах) [4]. Значение константы адсорбции много больше константы десорбции, что свидетельствует о том, что данный процесс практически не обратим.
Таким образом, в случае адсорбции крупных органических ионов на заряженной поверхности лимитирующей стадией является диффузия одноименно заряженных ионов в слое Гуи: А+ → А+г , где А+ - органический катион, А+г - органический катион, находящийся в слое Гельгольца.
Энергия активации этой стадии слагается из энергии активации диффузии адсорбата (ЕD) и энергии кулоновского отталкивания в диффузном слое Гуи-Чепмена. Так что Еа1 = ЕD + zFx ≈ 29 кДж/моль. Вторая стадия - хемосорбция адсорбата - протекает быстро и практически необратимо: А+г + Х- = АХ.
Выводы
- Установлены физико-химические закономерности адсорбции сложных органических ионов (доксорубицина, гемзара, метиленового голубого) на поверхности железоуглеродного сорбента, полученного в условиях импульсного электрического диспергирования в гексане.
- Показано, что адсорбция катионов происходит не только по электростатическому механизму, но и по ионному обмену с участием поверхностных гидроксильных групп сорбента с функциональными группами органических адсорбатов.
- Из кинетических зависимостей показано, что величина энергии активации 29 кДж/моль, складывается из энергии активации стадии диффузии одноименно заряженных ионов к слою Гельмгольца и хемосорбции адсорбата, которая протекает быстро и практически необратимо.
- Вся совокупность экспериментальных данных свидетельствует о том, что железоуглеродный сорбент можно использовать в качестве магнитного носителя лекарственных препаратов.
Рецензенты
- Коробочкин В.В., д.т.н., профессор, зав. кафедрой общей химической технологии, Институт природных ресурсов, Федеральное государственное бюджетное образовательное учреждение высшего профессионального образования «Национальный исследовательский Томский политехнический университет», г. Томск.
- Юсубов М.С., д.х.н., профессор, зав. кафедрой химии, фармацевтический факультет, Государственное бюджетное образовательное учреждение высшего профессионального образования «Сибирский государственный медицинский университет» Министерства здравоохранения и социального развития Российской Федерации, г. Томск.
Библиографическая ссылка
Галанов А.И., Юрмазова Т.А., Митькина В.А. АДСОРБЦИЯ ОРГАНИЧЕСКИХ ИОНОВ НА ЖЕЛЕЗОУГЛЕРОДНОМ СОРБЕНТЕ // Современные проблемы науки и образования. – 2012. – № 2. ;URL: https://science-education.ru/ru/article/view?id=5890 (дата обращения: 20.04.2024).



