Введение
Фармакогенетические исследования установили неоднородность человеческой популяции по способности метаболизировать лекарственные средства [2]. В одних случаях это приводит к увеличению концентрации в организме принимаемых ЛС и проявлению их токсического действия, в других – к низкой концентрации и недостаточным терапевтическим эффектам. Стандартные схемы эрадикационной терапии больных язвенной болезнью (ЯБ) не приводят гарантированно во всех случаях к полному уничтожению бактерий. В различных этносах эффективность эрадикации H.pylori (НР) варьирует от 30 до 90 % [4]. Одна из возможных причин – неэффективность антисекреторных средств. Индивидуальная терапевтическая эффективность стандартных доз ингибиторов протонной помпы (ИПП) варьирует в широких пределах (желудочная секреция снижается на 40–100 %). Известно, что биотрансформация ИПП происходит под воздействием системы цитохромов Р450, главным образом, – изоферментов CYP3A4 и CYP2C19, а полиморфизм гена, кодирующего активность CYP2C19, выраженно влияет на фармакокинетику омепразола и ланзопразола [5]. Этот полиморфизм даже при использовании стандартных доз определяет недостаточное снижение кислотопродукции как у здоровых добровольцев, так и у больных ЯБ гомозигот по обеим аллелям CYP2C19 («дикий тип») с быстрым метаболизмом ИПП [6]. Кроме более выраженного антисекреторного эффекта ИПП у медленных метаболизаторов выше и частота эрадикации НР при проведении двойной и тройной антихеликобактерной терапии (для достижения 100 % эрадикации при тройной терапии у них доза ИПП может быть в 4 раза ниже, чем у гомозигот) [9]. Проведение фармакогенетического анализа перед назначением ИПП может быть затратно-эффективной процедурой. Генотипирование CYP2C19 может сохранить примерно $5000 на каждые 100 протестированных пациентов [10].
Цель: индивидуализация выбора антисекреторной терапии больных ЯБ, ассоциированной с H. pylori, в зависимости от генотипа лекарственного метаболизма с учетом экономической эффективности.
Материалы и методы:
В исследование были включены 294 пациента с ЯБ, проходивших стационарное лечение в гастрохирургическом и гастротерапевтическом отделениях многопрофильного учреждения города Омска. Средний возраст включенных в исследование – 51,84±0,65 лет. Из них 198 – мужчин (67,35 %), 96 – женщин (32,65 %). У всех больных проводилось выявление полиморфизма гена CYP2C19. Использованные методы: молекулярно-генетический и статистический с использованием пакета STATISTICA-6.
Результаты и их обсуждение:
В обследованной популяции мутаций гена CYP2C19 по аллелю CYP2C19*3 не выявлено. Вероятным объяснением может служить относительно небольшая выборка пациентов. При исследовании полиморфизма CYP2C19*2 было выявлено, что 71,43±2,64 % пациентов имели генотип быстрых, 18,37±2,6 % – промежуточных, 10,2±1,77 % – медленных метаболизаторов.
На основании полученных результатов были построены модели фармакотерапии с учетом фармакогенетического профиля и посчитаны прямые затраты на лечение. Средняя стоимость ФЭГДС с верификацией НР (быстрый уреазный тест) в клиниках города Омска в 2012 году составила 1000 рублей. Ориентировочная стоимость анализа гена CYP2C19 – 650 рублей.
Проанализируем прямые затраты на реализацию 4-х моделей терапии больных ЯБ, ассоциированной НР (табл. 1). При этом отдаем себе отчет в том, что результаты анализа могут быть эффективными лишь при абсолютной комплаентности пациентов.
Таблица 1. Прямые затраты на фармакотерапию в ходе реализации стандарта лечения ЯБ*
|
Наименование препарата |
Разовая доза, мг |
Стоимость 1 дозы, руб.* |
|
Омепразол |
20 |
4,89 |
|
Лансопразол |
30 |
20,52 |
|
Рабепразол |
20 |
105,95 |
|
Эзомепразол |
20 |
94,49 |
|
Амоксициллин |
1000 |
12,74 |
|
Кларитромицин |
500 |
50,62 |
|
Тетрациклин |
500 |
4,45 |
|
Метронидазол |
500 |
5,04 |
|
Левофлоксацин |
500 |
61,98 |
|
Висмута трикалия дицитрат |
120 |
9,15 |
* – средняя стоимость 1 дозы рассчитывалась, исходя из стоимости препарата в аптеках города Омска по состоянию на 17.09.2012 года, http://www.omdrug.ru/information/drugs.php
В связи с достаточно низким уровнем резистентности НР к кларитромицину в России определение чувствительности к нему в расчетах мы учитывать не будем [1]. Резистентность НР к амоксициллину не развивается или же встречается очень редко [3].
Согласно модели № 1 лечение всех пациентов осуществляется согласно стандартам эрадикационной терапии (схема 1). До начала терапии и после проведения эрадикации всем пациентам предполагается выполнение ФЭГДС с верификацией НР. Терапия I линии назначается на 10 дней с дальнейшим долечиванием антисекреторными препаратами в половинных дозах в течение 4 недель. В случае неэффективности назначается эрадикационная терапия II линии.
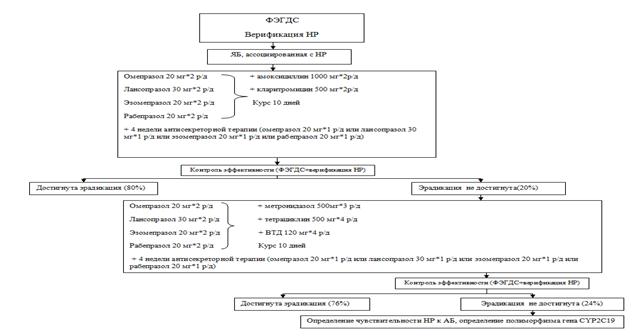
Схема 1. Стандартная фармакотерапия больных ЯБ, ассоциированной с НР.
Согласно результатам проведенного фармакоэпидемиологического исследования эффективность терапии I линии у больных ЯБ, ассоциированной с НР на территории Омской области составляет 78 %, т.е. в каждом четвертом случае будет необходима терапия II линии.
Даже при реализации терапии II линии средний показатель эрадикации составил 76 % (60–100 %) [8]. Кроме того, к недостаткам данной модели можно отнести тот факт, что при реализации терапии II линии пациенту необходимо ежедневно, до 4-х раз в сутки, принимать большое число таблеток и капсул (до 18 в сутки) с высокой вероятностью развития нежелательных явлений. Средняя стоимость 1 случая эффективной терапии на основе омепразола составит 3926,5 руб., лансопразола – 4841,8 руб., эзомепразола – 9173,48 руб., рабепразола – 9844,52 руб.
Модель № 2 предполагает исходно следование стандарту эрадикационной терапии (схема 2). До начала и после проведения эрадикации выполняется ФЭГДС с верификацией НР. Продолжительность терапии I линии 10 дней с дальнейшим долечиванием антисекреторными препаратами в половинных дозах в течение 4 недель. В случае неэффективности назначается эрадикационная терапия II линии. В качестве альтернативной нами была рассмотрена тройная терапия с левофлоксацином: ИПП в двойной дозе дважды в сутки в сочетании с амоксициллином (2000 мг/сут.) и левофлоксацином (1000 мг/сут.). В качестве эрадикационной терапии II линии после неудачной стандартной тройной терапии эта схема дает высокий результат [7]. Но с применением левофлоксацина связана проблема формирования резистентности к хинолонам вследствие целого ряда мутаций гена gyrA. Согласно результатам фармакогенетического исследования 89,8 % пациентов ЯБ на территории Омской области являются быстрыми или промежуточными метаболизаторами, в связи с чем, в схемах терапии II линии дозы омепразола и лансопразола увеличиваем в 2 раза, рабепразола и эзомепразола оставляем без изменений. По окончании курса терапии II линии пациентам вновь проводим ФЭГДС с верификацией НР. В случае неудовлетворительного результата определяем чувствительность НР.
Схема 2. Модифицированная фармакотерапия больных ЯБ, ассоциированной с НР (модель № 2)
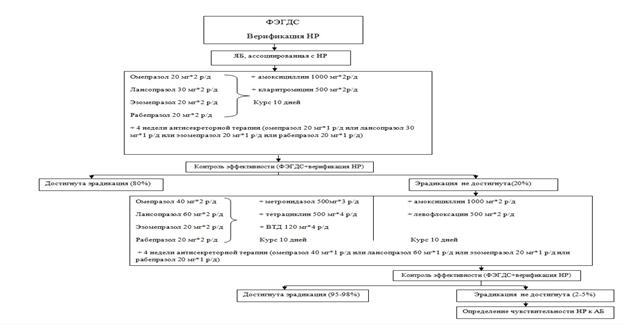
С учетом повторного курса терапии стандартными препаратами II линии 22 % пациентов (в связи с неэффективностью терапии I линии) средняя стоимость 1 случая эффективной терапии (тетрациклин, метронидазол, висмута трикалия дицитрат) на основе двойных доз омепразола и лансопразола составляет 3978,14 руб. и 5058,49 руб.; стандартных доз эзомепразола и рабепразола – 9173,48 руб. и 9844,58 руб. соответственно. При назначении альтернативной схемы (амоксициллин, левофлоксацин) стоимость возрастет и составит для схем на основе омепразола – 4153,96 руб., лансопразола – 5234,31 руб., эзомепразола – 9349,3 руб., рабепразола – 10020,4 руб.
В модели № 3 лечение всех пациентов осуществляется согласно стандартам эрадикационной терапии (схема 3). До начала терапии и после проведения эрадикации всем пациентам предполагается выполнение ФЭГДС с верификацией НР. Назначается терапия I линии на 10 дней с дальнейшим долечиванием антисекреторными препаратами в половинных дозах в течение 4 недель. Учитывая результаты фармакогенетического исследования пациентов ЯБ на территории Омской области, на старте назначаются двойные дозы омепразола и лансопразола, дозы эзомепразола и рабепразола – стандартные. В случае неэффективности терапии I линии – определение чувствительности НР.
Схема 3. Модифицированная фармакотерапия больных ЯБ, ассоциированной с НР (модель № 3)
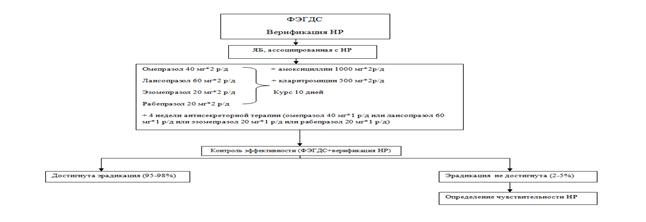
Эффективность такой терапии – 95–98 %. Средняя стоимость 1 случая эффективной терапии на основе омепразола составляет 3736,64 руб., лансопразола – 5237,12 руб., эзомепразола – 7802,72 руб., рабепразола – 8352,8 руб.
Лечение всех пациентов согласно модели № 4 осуществляется в соответствии со стандартами эрадикационной терапии (схема 4). До начала терапии и после проведения эрадикации всем пациентам выполняется ФЭГДС с верификацией НР и генотипирование с определением полиморфизма гена CYP2C19. Согласно результатам генотипирования пациентам с быстрым и промежуточным метаболизмом ИПП назначаются двойные дозы омепразола и лансопразола, дозы эзомепразола и рабепразола – стандартные; медленным метаболизаторам – все ИПП в стандартных дозировках. В случае неэффективности терапии I линии – определение чувствительности НР.
Схема 4. Модифицированная фармакотерапия больных ЯБ, ассоциированной с НР (модель № 4)
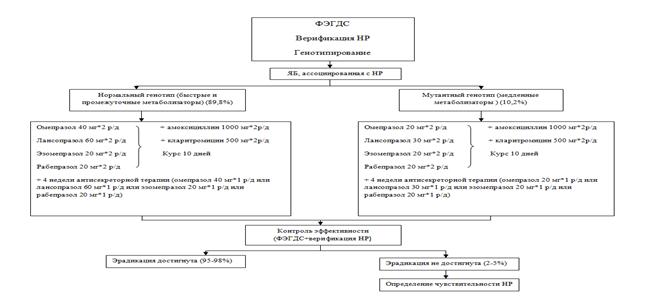
Эффективность терапии согласно такой модели лечения – 95–98 %. Средняя стоимость 1 случая эффективной терапии на основе омепразола составляет 4363,17 руб., лансопразола – 5788,62 руб., эзомепразола – 8452,67 руб., рабепразола – 9002,8 руб.
Результаты фармакоэкономических расчетов представлены в сводной таблице (табл. 2).
Таблица № 2. Сводные результаты фармакоэкономических расчетов представленных моделей
|
|
Средняя стоимость 1 случая эффективной терапии, руб. |
|||
|
омепразол |
лансопразол |
эзомепразол |
рабепразол |
|
|
Модель № 1 |
3926,5 |
4841,8 |
9173,48 |
9844,58 |
|
Модель № 2 альтернативная схема × тетрац+ метр+ВТД
× амо+левофл |
3978,14
4153,96 |
5058,49
5234,31 |
9173,48
9349,3 |
9844,58
10020,4 |
|
Модель № 3 |
3736,64 |
5237,12 |
7802,72 |
8352,8 |
|
Модель № 4 |
4363,17 |
5788,62 |
8452,72 |
9002,8 |
Выводы
Представленные модели предлагают наиболее вероятные схемы терапии больных ЯБ, ассоциированной с НР. Чаще на практике реализуется модель № 1. Но, согласно статистическим данным, 5 человек из 100, несмотря на выполнение всех рекомендаций и финансовые затраты, не получат эффективного лечения. Так как уровень резистентности НР к антибактериальным препаратам первой линии в РФ достаточно низок, наиболее вероятная причина неэффективности – особенности метаболизма ИПП (омепразол, лансопразол). Соответственно модель № 2, несмотря на большую стоимость, предполагает более высокую эффективность лечения. В реальной практике модель № 3 реализуется редко, но она является самой экономически выгодной. Тем более, что пациенты получат лишь один курс эрадикационной терапии, что, безусловно, повысит комплаентность, а также снизит риски побочных эффектов. Из всех представленных вариантов тактики ведения пациентов модель № 4 менее экономически выгодна. Реально в клинике не применяется, но, учитывая персонифицированный подход к пациенту согласно результатам генотипирования СYP2C19, перспективы у данной модели есть. Полученные результаты генотипирования помогут не только индивидуально подобрать схему фармакотерапии для каждого пациента, но и станут вкладом в генетический паспорт пациента и позволят индивидуализировать подход к назначению препаратов из других фармакологических групп.
Рецензенты:
Ливзан Мария Анатольевна, д.м.н., профессор, зав. кафедрой факультетской терапии с курсом профессиональных болезней ГБОУ ВПО «Омская государственная медицинская академия» Министерства здравоохранения РФ, г. Омск
Пеньевская Наталья Александровна, д.м.н., зав. кафедрой фармацевтической технологии с курсом биотехнологии ГБОУ ВПО «Омская государственная медицинская академия» Министерства здравоохранения РФ, г. Омск.
Библиографическая ссылка
Елохина Е.В., Скальский С.В., Костенко М.Б. ГЕНЕТИЧЕСКИЙ ПОЛИМОРФИЗМ ЛЕКАРСТВЕННОГО МЕТАБОЛИЗМА КАК ПРЕДИКТОР КЛИНИЧЕСКОЙ ЭФФЕКТИВНОСТИ ФАРМАКОТЕРАПИИ БОЛЬНЫХ ЯЗВЕННОЙ БОЛЕЗНЬЮ, АССОЦИИРОВАННОЙ С Н. PYLORI // Современные проблемы науки и образования. – 2012. – № 6. ;URL: https://science-education.ru/ru/article/view?id=7865 (дата обращения: 24.04.2024).



