Введение. Ситуация по туберкулезу в Российской Федерации остается напряженной, несмотря на некоторое улучшение отдельных эпидемических показателей. По данным официальных источников [5; 8], заболеваемость туберкулезом в 2011 году составила 73,0 на 100 тыс. населения (в 2010 году 77,4 на 100 тыс. населения; в 2009 году - 82,6 на 100 тыс. населения). Несмотря на тенденцию к снижению заболеваемости, серьезную проблему представляет собой увеличение количества больных с наличием лекарственно устойчивых штаммов M.Tuberculosis, что ведет к нарастанию резервуара туберкулезной инфекции [8]. Снизить инфекционную нагрузку на общество позволит качественное лечение впервые выявленных больных специфическим процессом. Как известно, все формы лекарственной устойчивости (ЛУ) возбудителя значительно утяжеляют терапевтический процесс, удлиняют сроки лечения и снижают его эффективность [3; 6; 8; 9]. Применение адекватной терапии способствует предупреждению развития лекарственной устойчивости возбудителя. В соответствии с нормативными документами России больным с высоким риском лекарственной устойчивости M.Tuberculosis до получения результатов микробиологического исследования назначается IIБ режим химиотерапии [3]. Для повышения комплаентности терапии большим количеством противотуберкулезных препаратов проводится разработка новых форм лекарственных веществ. С этой целью в последние годы широко изучается вопрос использования комбинированных химиопрепаратов с фиксированными дозировками [2]. По данным некоторых авторов, применение таких лекарственных форм способствует лучшей организации лечебного процесса [5; 10].
Цель исследования. Оценка и обоснование возможности использования комбинированного препарата с фиксированными дозировками Комбитуб-нео в лечении впервые выявленных больных с высоким риском развития ЛУ M.Tuberculosis (MБT) с позиций клинической эффективности.
Материалы и методы. Объектом исследования являлись 48 больных туберкулезом легких, лечившихся в Областном клиническом противотуберкулезном диспансере г. Саратова в 2011-2012 гг. Предметом – режим химиотерапии. Дизайн исследования определен как проспективное, рандомизированное. Критериями включения были - впервые выявленные пациенты с деструктивным туберкулезом легких, бактериовыделением и высоким риском ЛУ возбудителя, в возрасте от 18 до 60 лет, сроки лечения более 90 доз в условиях стационара. Критериями исключения являлись: тяжелая сопутствующая патология; ВИЧ-инфекция; беременность и период лактации; множественная ЛУ, выявленная на любом этапе лечения; ЛУ хотя бы к одному из химиопрепаратов, входящих в выбранную схему терапии; непереносимость одного из компонентов комбинированного противотуберкулезного препарата в анамнезе.
Стартовая химиотерапия проводилась по IIБ режиму в соответствии с Приказом № 109 от 21 марта 2003 года [3].
Наблюдаемые были разделены на 2 группы:
I – пациенты, у которых применялся комбинированный химиопрепарат с фиксированными дозировками (fixed dose combination) - комбитуб-нео (n=21) (Комбитуб-нео, «SIMPEX PHARMA Pvt. Ltd.», Индия). Комбитуб-нео содержит в 1 таблетке - 200 мг ломефлоксацина, 188 мг протионамида, 400 мг пиразинамида, 360 мг этамбутола. Схема лечения: больным комбитуб-нео назначался после приема пищи; суточная доза делилась на 2 приема и зависела от массы тела пациента, но не более 5 таблеток. Препарат дополнялся изониазидом из расчета 10 мг/кг массы тела, рифампицином – 10 мг/кг;
II - больные, в терапии которых использовался комплекс противотуберкулезных лекарственных средств, состоящий из монопрепаратов (МП) – изониазид 10 мг/кг (изониазид, «Фармсинтез», Россия), рифампицин 10 мг/кг (рифампицин, «Фармсинтез», Россия), пиразинамид-акри 25 мг/кг (пиразинамид, «Акрихин», Россия), этамбутол-акри 25 мг/кг (этамбутол, «Акрихин», Россия), ломефлоксацин 800 мг в сутки (ломефлоксацин, «Фармсинтез»), протионамид-акри 12,5 мг/кг (протионамид, «Акрихин») (n=27).
Критериями достигнутой эффективности терапии являлись прекращение бактериовыделения и заживление полостей распада. Мониторинг исследования включал: ежедневный клинический осмотр; ежемесячное исследование мокроты на МБТ методами люминесцентной микроскопии и посева на жидкие и плотные питательные среды; ежемесячный и по показаниям общий и биохимический анализы крови; рентгенологическое обследование до лечения и при получении 60, 90, 120 доз. При динамическом контроле эффективности терапии динамика исследуемых параметров ранжировалась как значительная, умеренная, незначительная положительная, отсутствие динамики, а также появление отрицательной направленности процесса. Безопасность схем лечения оценивали по частоте нежелательных явлений, связанных с терапией, и изменению лабораторных показателей, в первую очередь показателей билирубина, креатинина и трансаминаз.
Статистическая обработка материала проводилась с помощью унифицированных компьютерных программ Excel Microsoft Word и пакета прикладных программ Statistika. В работе проводилось сравнение частот бинарного признака в двух несвязанных группах с помощью оценки отношения шансов (ОШ); были построены таблицы сопряженности, содержащие частоты для взаимоисключающих значений изучаемого бинарного признака в каждой из групп. Доверительный интервал (ДИ) для отношения шансов вычислялся по методу Woolf. Сравнение двух групп по относительной частоте значений качественного признака проводилось способом проверки нулевой статистической гипотезы о равенстве относительных частот в двух популяциях.
Результаты исследования
Все пациенты были трудоспособного возраста. Поскольку распределение больных по возрасту в группах отличалось от нормального, мы рассчитали медиану в I группе - 38 лет, и оценили интерквартильный размах: от 28 до 45 лет, во II группе медиана составила 37 лет (25-й процентиль=31, 75-й процентиль=44) (рис. 1).
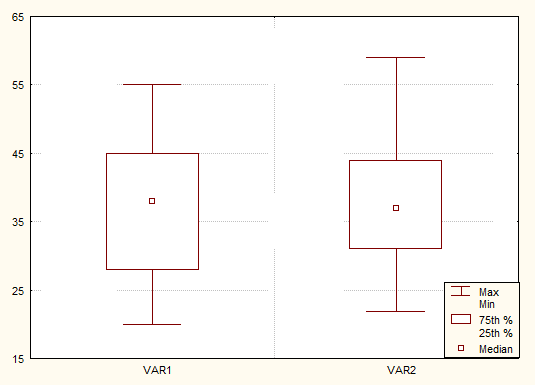
Рисунок 1. Распределение количественных данных по возрасту в группах наблюдения: медиана возраста, её 2 и 3 (25-75%) квартили, минимум, максимум.
(VAR1 – Комбитуб-нео, VAR2 – Комплекс из монопрепаратов)
Гендерная характеристика пациентов обеих групп достоверно не различалась (преобладали лица мужского пола - 76,1, 66,7% соответственно в I, II группах, р>0,05). У больных отмечались один или несколько факторов риска развития ЛУ (рис. 2). Ведущая роль в формировании агрессивной инфекционной среды принадлежит низкому социальному уровню жизни. В проведенном исследовании 90,5, 92,6% пациентов в I, II группах наблюдения соответственно относились к социально неблагополучным слоям общества. Из социальных предикторов доминировали: отсутствие постоянной работы - 76,2, 74,1%, злоупотребление алкоголем - 57,1, 59,3% и курение – 85,7, 88,9%. Среди обследованных отмечен высокий удельный вес одиноких пациентов, что является значимым фактором риска возникновении туберкулеза (23,8; 33,3%). Доля мигрантов составила 14,3, 11,1% соответственно в I, II группах. Пребывание раннее в пенитенциарной системе регистрировалось в анамнезе у 9,5, 11,1% больных. Таким образом, при анализе социальной принадлежности в группах наблюдения достоверных различий не получено (р>0,05).
Большинство пациентов в наблюдаемых группах в силу социальных особенностей существования имели контакт с больными туберкулезом. Достоверно наличие туберкулезного контакта установлено у 28,6 и 33,3% лиц I, II групп соответственно.
Несмотря на активную работу по своевременному выявлению впервые выявленных больных специфическим процессом в Саратовской области, треть пациентов в группах наблюдения не обследовалась более 2-х лет (33,3; 33,3%). Каждый десятый больной (14,3; 11,1% случаев (в I, II группах соответственно) уклонялся от госпитализации, что привело к позднему началу химиотерапии.
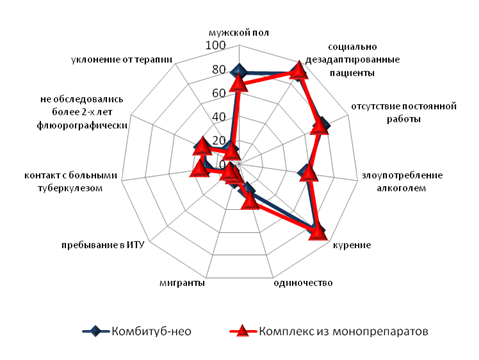
Рисунок 2. Факторы риска развития ЛУ форм туберкулеза у впервые выявленных больных (p>0,05)
Среди клинических форм туберкулеза органов дыхания лидирующей отмечен инфильтративный туберкулез (80,9 и 81,5%). На втором месте - диссеминированный туберкулез (подострое течение) 9,5, 11,1%. Фиброзно-кавернозный туберкулез (ФКТ) и казеозная пневмония зарегистрированы у 9,5, 7,4%.
Отягощенность наблюдаемых больных многообразной сопутствующей патологией можно расценить как следствие асоциального образа жизни, недостаточное внимание к своему здоровью, длительное воздействие агрессивных факторов (курение). У пациентов преобладали хронические неспецифические заболевания легких – 76,2, 74,1% и заболевания желудочно-кишечного тракта 47,6, 48,1%.
Группы сравнения были сопоставимы по клиническим характеристикам (рис. 3).
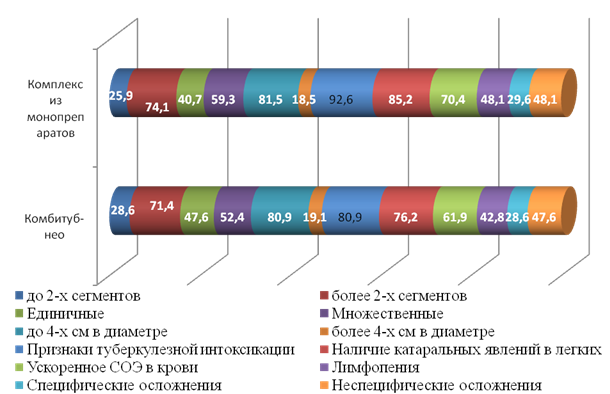
Рисунок 3. Характер туберкулезных изменений у больных с высоким риском ЛУ возбудителя*
* - статистически значимых различий не получено
Как видно из рисунка 3, у пациентов регистрировались преимущественно распространенные деструктивные легочные процессы, что подтверждает высокий риск развития ЛУ. Обширным локальным рентгенологическим проявлениям соответствовала выраженность клинической реакции. У подавляющего числа больных доминировали жалобы интоксикационного характера (80,9; 92,6% соответственно, p>0,05) в виде слабости, повышенной утомляемости, сниженной работоспособности, вегетативных дисфункций (гипергидроз, ухудшение аппетита со снижением массы тела, повышение температуры тела). Большинство пациентов отмечали у себя кашель с отделением мокроты (76,2; 77,8%, p>0,05).
По исходному лабораторному клинико-биохимическому профилю достоверных различий между показателями в группах сравнения не выявлено. При поступлении в группах наблюдения степень бактериальной агрессии статистически не различалась.
Анализ осложнений заболевания также показал отсутствие значимых различий у наблюдаемых пациентов. У трети больных каждой из групп регистрировались одно или несколько специфических осложнений туберкулезного процесса – туберкулез бронхов, кровохарканье, ателектаз, плеврит – 28,6, 29,6% в I, II группах соответственно. Неспецифические осложнения, являющиеся отражением воспалительного процесса и объема поражения легочной ткани - дыхательная и (или) сердечная недостаточность разной степени выраженности, кахексия, анемия - фиксировались почти у половины больных.
Результаты исследования на лекарственную устойчивость МБТ были получены на сроках от 60 до 90 доз. Анализ спектра ЛУ показал ее одинаковую частоту во всех группах. Наиболее часто – 72,6% - выявлялась ЛУ к стрептомицину; реже - к канамицину – 5,5% и офлоксацину – 4,1%. В том числе в 71,2% случаев определялась ЛУ к одному-двум химиопрепаратам (ХП); в 28,8% – к трем ХП.
По данным ряда исследователей, одной из причин недостаточной эффективности лечения туберкулеза является плохая переносимость лекарственных средств в связи с частым развитием нежелательных побочных реакций [7]. По данным В.Ю. Мишина [1], побочные реакции (ПР) на противотуберкулезные препараты при лечении пациентов с лекарственной устойчивостью регистрируются в 42,9% случаев. При оценке частоты и спектра ПР в наблюдаемой нами когорте лиц удельный вес нежелательных явлений составил 34,2%. Причинно-следственную связь с приемом конкретного препарата удалось установить только в 28,0% случаев. Нейротоксические реакции были связаны в основном с назначением изониазида, их удельный вес оставил 12,0%. Жалобы на артралгию, которая купировалась после назначения противовоспалительных средств и вероятнее всего была обусловлена наличием в схеме пиразинамида, предъявляли 4,0% больных. Тошнота и боль в эпигастральной области у 8,0% пациентов были связаны с приемом протионамида, так как изменение режима приема препарата привело к купированию ПР. Повышение уровня трансаминаз, связанное с рифампицином, зарегистрировано у 1 пациента (4,0%).
Следует отметить, что большинство побочных эффектов во всех группах наблюдалось в первые месяцы от начала химиотерапии. Медиана длительности наблюдения от начала химиотерапии до развития нежелательного эффекта составила 14 дней (интерквартильный размах 8-34 дня). У большинства пациентов (85,7%) реакции носили устранимый характер. Кожно-аллергические проявления купированы назначением таблетированных антигистаминных препаратов на 7-8 дней (19,0%). Удельный вес токсических реакций на химиопрепараты составил 81,0%, в их структуре преобладали нежелательные эффекты со стороны желудочно-кишечного тракта (47,1%), гепатотоксические (29,4%), нейротоксические (17,4%), артралгия (5,9%). Во всех случаях реакции устранены введением симптоматических средств (гепатопротекторы, гастропротекторы, витамины группы В и др.) без изменения схемы химиотерапии.
Полное прекращение химиотерапии и замена лекарственного вещества потребовалось в 3-х случаях. У 2-х больных развился токсический гепатит (агент не идентифицирован), что потребовало индивидуализировать лечение пациента, и при использовании МП зарегистрирована ПР на пиразинамид в виде выраженной артралгии, не купировавшейся назначением нестероидных противовоспалительных средств.
В табл. 1 представлена частота и структура ПР у впервые выявленных больных туберкулезом легких, получавших различные формы этиотропных препаратов.
Таблица 1
Структура нежелательных явлений при лечении больных туберкулезом различными схемами химиотерапии в рамках IIБ режима
|
|
Комбитуб-нео n=21 |
Комплекс из монопрепаратов n=27 |
p |
||
|
|
абс |
% |
абс |
% |
|
|
Всего |
7 |
33,3 |
10 |
37 |
Фишера p=0,5166* |
|
Сроки возникновения побочных реакций |
|
||||
|
до 30 дней |
5 |
71,4 |
7 |
70 |
p>0,05 |
|
30-60 дней |
2 |
28,6 |
2 |
20 |
p>0,05 |
|
более 60 дней |
|
|
1 |
10 |
p>0,05 |
|
Вид и выраженность реакций |
|
||||
|
Аллергические |
2 |
28,6 |
3 |
30 |
p>0,05 |
|
Токсические, из них: |
5 |
71,4 |
7 |
70 |
p>0,05 |
|
гепатотоксические |
1 |
20 |
3 |
42,9 |
p>0,05 |
|
гастротоксические |
3 |
60 |
2 |
28,6 |
p>0,05 |
|
нейротоксические |
1 |
20 |
1 |
14,3 |
p>0,05 |
|
артралгия |
|
|
1 |
14,3 |
p<0,05 |
|
Характер реакций |
|
||||
|
Устранимая |
6 |
85,7 |
8 |
80 |
p>0,05 |
|
Неустранимая |
1 |
14,3 |
2 |
20 |
p>0,05 |
* при сравнении малых групп с наличием побочных реакций дополнительно использовался точный критерий Фишера.
Как видно из таблицы 1, по структуре и частоте нежелательных явлений статистически значимых различий в группах пациентов, получавших разные формы этиотропных препаратов, получено не было (Фишера p=0,5166). В структуре токсических реакций при использовании МП доминировал гепатит (повышение уровня трансаминаз в 3 и более раз от верхней границы нормы); лечение комбинированным препаратом с фиксированными дозировками наиболее часто сопровождалось поражением желудочно-кишечного тракта.
Развившиеся неустранимые реакции привели к изменению схемы лечения в виде исключения агента, вызвавшего ПР, эффективность терапии оценивалась в I группе (комбитуб-нео) у 20 человек, во II группе (комбинация из МП) – у 25 чел.
Оценка клинической динамики на фоне проводимой ХТ показала, что после получения 90 доз значительное и умеренное клиническое улучшение у пациентов наблюдалось в 90,0% (n=18) и 92,0% (n=23) (p>0,05). У больных к этому сроку фиксировались: купирование катаральных явлений в легких, нормализация температуры, прибавка массы тела от 1,5 до 3 кг. Прекращение бактериовыделения на 90 дозах отмечено лишь у 35,0% (n=7) наблюдаемых I группы и 36,0% (n=9) лиц II группы (p>0,05). Однако значительное уменьшение интенсивности бактериовыделения получено у значительно большего числа пациентов: 45,0% (n=9), 44,0% (n=11) (p>0,05). Рубцевание деструкций по получении 90 доз ХТ достигнуто в 20,0% (n=4) случаев в I группе и в 20,0% (n=5) – в II группе (p>0,05). При этом отмечена тенденция к более быстрому рассасыванию инфильтративных изменений и уменьшению размеров полостей распада у больных.
После получения пациентами 120 доз ХП нормализация клинической картины получена у 100% (n=20) больных I группы, 96,0% (n=24) II группы лиц (p>0,05). Показатели прекращения бактериовыделения у больных в I группе составили 70,0% (n=14), во II группе 72,0% (n=18). Рубцевание полостей распада в двух группах оставалось недостаточным: 35,0% (n=7) в I группе и 36,0% (n=9) - во II группе, но выраженная рентгенологическая динамика в виде рассасывания инфильтрации, очагов обсеменения, уменьшение числа и размеров деструкций отмечена в большем проценте случаев: 70,0% (n=14) против 72,0% (n=18) (p>0,05) – II группа (рис. 4).
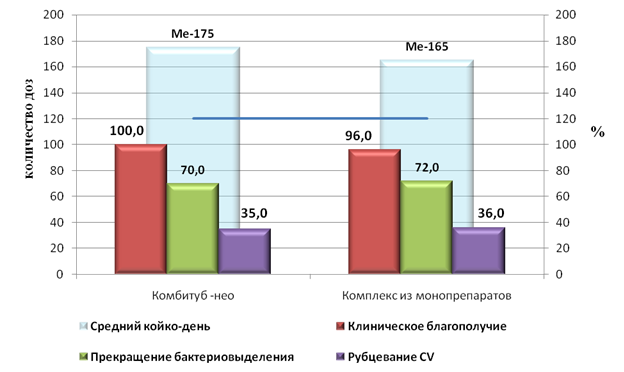
Рисунок 4. Удельный вес эффективно пролеченных пациентов на 120 дозах химиотерапии с указанием средних сроков пребывания в стационаре
По окончании стационарного этапа химиотерапии полное клиническое и эпидемическое благополучие было достигнуто у 80,0% (n=16) пациентов I группы и 80,0% (n=20) больных II группы соответственно (p>0,05). Рубцевание полостей распада среди больных I группы отмечалось в 55,0% (n=11), во II группе – в 56,0% (n=14) (p>0,05). У 10,0% (n=2), 12,0% (n=3) больных наблюдаемых групп отмечалось прогрессирование процесса.
Изучили продолжительность химиотерапии у эффективно пролеченных больных туберкулезом легких. Тип распределения данных отличался от нормального, поэтому средние показатели не рассчитывали. Число принятых суточных доз в I группе составило: медиана - 175, минимум - 155, максимум - 186 (n=11). При проведении квартильного анализа больных I группы было установлено, что длительность терапии у больных, вошедших во 2-й и 3-й квартили (50% от их числа) составила от 174 до 185 суточных доз. Аналогичное исследование было проведено и для пациентов II группы. Длительность терапии: медиана - 165, минимум - 149, максимум – 197 (n=14). Продолжительность химиотерапии по квартилям – от 155 до 185 суточных доз.
Сравнивая вероятность наступления клинического излечения в группах при использовании разных форм этиотропных препаратов по критерию «прекращение бактериовыделения», получено OШ 1,0 [95%-ный ДИ -1,56-1,56], то есть различия между группами статистически незначимы. Аналогичные данные установлены и по признаку «заживление деструкций» - OШ 0,96 [95%-ный ДИ -1,28-1,20].
Выводы
1. При лечении впервые выявленных пациентов с высоким риском развития ЛУ возбудителя использование различных форм этиотропных препаратов не оказывает статистически значимого влияния на эффективность терапии.
2. Для достижения адекватной результативности при назначении стартового IIБ режима химиотерапии целесообразно не менее 120 доз интенсивной фазы стационарного этапа ведения пациентов.
3. Применение комбинированного препарата Комбитуб-нео не вызывает повышения частоты неустранимых побочных реакций при лечении впервые выявленного туберкулеза легких по IIБ режиму химиотерапии.
Рецензенты:
Казимирова Наталия Евгеньевна, доктор медицинских наук, профессор, заведующий кафедрой фтизиопульмонологии ГБОУ ВПО «Саратовский государственный медицинский университет им. В.И. Разумовского Минздрава России», г. Саратов.
Салина Татьяна Юрьевна, доктор медицинских наук, доцент кафедры фтизиатрии ФПК и ППС ГБОУ ВПО «Саратовский государственный медицинский университет им. В.И. Разумовского Минздрава России», г. Саратов.
Библиографическая ссылка
Морозова Т.И., Морозова Т.И., Докторова Н.П., Докторова Н.П., Баринбойм О.Н., Баринбойм О.Н., Паролина Л.Е. КЛИНИЧЕСКОЕ ИССЛЕДОВАНИЕ ПРИМЕНЕНИЯ КОМБИНИРОВАННЫХ ХИМИОПРЕПАРАТОВ В КОМПЛЕКСНОМ ЛЕЧЕНИИ БОЛЬНЫХ ТУБЕРКУЛЕЗОМ // Современные проблемы науки и образования. – 2013. – № 2. ;URL: https://science-education.ru/ru/article/view?id=9048 (дата обращения: 19.04.2024).



