У пациентов, перенесших травму спинного мозга (ТСМ), помимо патологических процессов, происходящих в эпицентре травмы, развиваются различные осложнения, характеризующиеся полиорганной дисфункцией [1, 2]. Патологические состояния, возникающие во время острой фазы, представляют наибольшую опасность для жизни и являются частой причиной смертности. Вторичные системные осложнения, развивающиеся в отдаленном периоде, приводят к значительному снижению качества жизни и длительной реабилитации [3, 4]. Частота и тяжесть осложнений коррелируют с уровнем травмы и степенью повреждения спинного мозга. После ТСМ наряду с моторным и сенсорным дефицитом часто наблюдается дисфункция сердечно-сосудистой, респираторной, мочевыделительной и желудочно-кишечной систем.
В настоящее время продолжается поиск стратегий, позволяющих улучшить состояние спинного мозга после его травматического повреждения и способствующих восстановлению нервной ткани [5, 6]. Одним из направлений стимуляции восстановительных процессов в поврежденных невральных структурах является использование нейропротекторов антиоксидантного типа действия [7]. Другим перспективным направлением влияния на посттравматические процессы представляется применение гидрогелей на основе синтетических биосовместимых и биодеградируемых материалов [8]. Однако возможность использования гидрогеля в качестве среды-носителя для фармакологических нейропротекторов и их локального применения на сегодняшний день остается нереализованной. Между тем попытки минимизировать возникновение локальных осложнений ТСМ и стимулировать восстановительные процессы в нервной ткани могут привести к снижению вторичных системных осложнений.
Цель исследования – изучить частоту и характер вторичных системных осложнений у крыс в условиях применения геля «Антиадгезин» и препарата Мексидол в различных комбинациях при моделировании ТСМ.
Материал и методы исследования. Исследование проведено на 95 самках крыс линии Вистар (8–12 месяцев, 270–320 г). Все экспериментальные исследования и манипуляции выполнялись в соответствии с требованиями «Европейской конвенции по защите позвоночных животных, используемых для экспериментальных и других научных целей» (Страсбург, 1986) и Директивы 2010/63/EU Европейского парламента и Совета Европейского союза по охране животных, а также были одобрены Комитетом по этике ФГБУ «“НМИЦ ТО” им. академика Г.А. Илизарова». Содержание и уход за животными осуществляли в соответствии с ГОСТ 33216-2014.
Животные были разделены на 4 группы случайным образом. Всем крысам под общим наркозом выполняли ляминэктомию на уровне ТhIX с последующим моделированием контузионной травмы спинного мозга средней степени тяжести путем свободного падения калиброванного груза на объект с заданной высоты [9]. Крысам 1-й группы (n=20) операционную рану ушивали без дополнительных манипуляций. Крысам 2-й группы (n=25) на твердую мозговую оболочку наносили 0,2 мл противоспаечного рассасывающегося геля «Антиадгезин», крысам 3-й группы (n=25) – 0,2 мл «Антиадгезина» и 0,08 мл Мексидола, смешанных до однородной консистенции, крысам 4-й группы (n=25) – 0,2 мл геля «Антиадгезин» в сочетании с однократным внутрибрюшинным введением 0,08 мл Мексидола. В послеоперационном периоде проводили ряд мероприятий, направленных на предотвращение послеоперационных осложнений (профилактику дегидратации, гемостатическую терапию, антибиотикотерапию).
Животных выводили из эксперимента на 5-е, 15-е, 30-е, 60-е и 90-е сутки. Падеж экспериментальных животных регистрировали на 2-е, 3-и, 4-е, 6-е, 7-е, 15-е и 55-е сутки. Вскрытие трупов проводили по стандартной методике.
Результаты исследования и их обсуждение
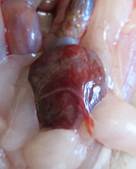
В 1-й группе животных на ранних сроках эксперимента (2–5 суток) летальность была достаточно высокой: погибли 4 крысы из 5. В процессе вскрытия у всех крыс были выявлены идентичные изменения в слизистой оболочке мочевого пузыря, указывающие на развитие острого геморрагического цистита: отек, гиперемия, расширенные сосуды и множественные кровоизлияния (рис. 1а). В 1 случае патология осложнялась почечной апоплексией и токсической гепатопатией неустановленного генеза, о чем свидетельствовали охряно-желтый цвет органа, незначительное его увеличение, дрябловатость паренхимы и наличие признаков единичных очагов некроза на разрезе. Помимо этого, у двух крыс, павших на сроке 4 суток, обнаружена гиперплазия элементов лимфоидной ткани большого сальника. Также диагностирована единичная пневмопатия, представленная отеком легких.
|
|
|
|
|
а |
б |
в |
|
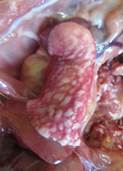
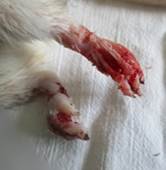
Рис. 1. Патологически измененные внутренние органы крыс: а – мочевой пузырь с обширными кровоизлияниями, срок эксперимента 3 суток, 1-я группа; б – гнойная пневмония, срок эксперимента 15 суток, 2-я группа; в – аутомутиляция тазовых конечностей, 2-я группа |
||
На 15-е сутки эксперимента в структуре патологии доминировало поражение мочевыделительной системы: острый и подострый геморрагический цистит отмечали у всех животных. Аутопсия крысы, павшей на этом сроке, выявила совокупность признаков, указывающих на токсическую висцеропатию: дряблость и ярко-желтая окраска печени с красными вкраплениями на разрезе, дряблость селезенки, энтерит, а также многочисленные серозно-гнойные узелковые поражения брыжейки, тонкого кишечника и легких.
К 30-м суткам эксперимента патологические процессы мочевыделительной системы наблюдали также у всех животных, однако признаки стали менее выражены и ограничивались утолщением стенки мочевого пузыря и наличием в ней единичных петехий. Вместе с тем у половины крыс патология была осложнена патологией почек: они были набухшими, с полнокровным корковым слоем, в котором имелись множественные включения темно-красного цвета, что указывало на развитие гломерулонефрита.
На сроке 55 суток от начала эксперимента 1 животное погибло с выраженными признаками боли и судорогами. Исследование секционного материала выявило разрыв мочевого пузыря на фоне уролитиаза с выходом в брюшную полость около 20 мл мочи.
На 60-е сутки эксперимента еще у 1 из крыс зафиксировано хроническое воспаление мочевого пузыря с наличием в полости небольшого количества песка, скорее всего, фосфатного происхождения. Кроме того, у 2 животных выявлены осложнения инфекционного характера, представленные серозно-гнойным очаговым воспалением легких и кишечника.
В отдаленные сроки после начала эксперимента (90 суток) только у 3 крыс были выявлены изменения внутренних органов. При этом в структуре патологии отмечали хронические заболевания мочевыделительной системы (хронические циститы и нефросклероз) и множественные мелкие абсцессы легких, кишечника и почек.
Помимо этого, на каждой стадии эксперимента у всех животных контрольной группы диагностировали дряблость и атрофичность мышц тазовых конечностей.
Общая летальность животных в данной группе составила 30%, при этом большинство случаев гибели приходилось на ранние сроки эксперимента (до 5 суток).
Во 2-й группе на ранних сроках эксперимента наблюдали гибель 2 животных. 1 крыса пала на 3-и сутки в результате отека легких с сопутствующей патологией – острым геморрагическим циститом. Гибель еще 1 крысы пришлась на срок 7 суток от начала эксперимента, аутопсия выявила множественные участки некротического поражения коркового вещества почек и гепатопатию неустановленного генеза. Патология органов на ранних сроках была определена у всех животных данной группы. На первом месте фигурировали заболевания мочевого пузыря воспалительного характера с наличием кровоизлияний, в двух случаях – в сочетании с токсическим поражением печени.
На 15-е сутки эксперимента количество осложнений несколько снизилось – изменения внутренних органов были диагностированы у 4 животных из 5. Доминирующее положение занимала патология почек: почечные инфаркты (у 2 крыс), в одном случае в совокупности с подострым циститом и умеренной спленомегалией, а также эпизод почечной кисты. Гнойная пневмония зафиксирована у 1 крысы (рис. 1б).
На 30-е сутки эксперимента в основном диагностировали осложнения инфекционного характера: по одному случаю двухсторонней гнойной пневмонии и отека легких в сочетании с хроническим циститом.
На сроке 60 суток диагностирован лишь единичный случай хронического цистита, у остальных животных изменений внутренних органов не выявлено.
Через 90 суток все патологоанатомические находки имели хронический характер: одиночная почечная киста и хронический цистит. Еще у 2 животных обнаружены объемные опухолевидные образования, расположенные на большом сальнике, предположительно состоящие из лимфоидной и жировой тканей. В этот же период появляются признаки мышечной атрофии тазовых конечностей (3 крысы).
Общая летальность в данной группе животных составила 8%.
В 3-й группе на ранних сроках эксперимента превалировала патология печени: у трех животных на вскрытии обнаружена токсическая гепатопатия. У этих же крыс отмечали гиперплазию лимфоидных структур сальника, что может указывать на наличие воспалительных или иммунных процессов в организме. Патология мочевыделительной системы, представленная острым циститом, выявлена лишь у 2 подопытных животных.
Через 2 недели после начала эксперимента процент крыс с поражением органов мочевыделения сохранялся на том же уровне, но воспаление мочевого пузыря носило подострый характер. В одном случае цистит был сопряжен с очаговыми изменениями в почках, напоминающими поражения тубулярного аппарата: корковое вещество на разрезе серо-желтоватого оттенка, прилежащее мозговое вещество полнокровное, серо-красное, с незначительным выбуханием. Данное животное погибло. Также выявлены отдельные эпизоды гепатолиенального синдрома, гипотрофии мышц тазовых конечностей и узелковое поражение структур сальника воспалительного характера.
На 30-е сутки эксперимента заболевания мочевыделительной системы в виде хронического цистита обнаружены лишь у 2 животных, у 1 из них данная патология сочеталась с наличием опухолевидного образования лимфоидных структур большого сальника и спленомегалией. У второго животного в результате мышечной ригидности, вероятно, нейрогенного характера, развились атрофия мышц тазовых конечностей и артриты коленных суставов. У остальных 3 животных на данном этапе эксперимента видимых патологических изменений органов не выявлено.
Через 60 суток после оперативного вмешательства органопатология зафиксирована всего у 2 крыс: гидронефроз на фоне уролитиаза и гепатолиенальный синдром.
На последнем этапе эксперимента (90 суток) изменения органов диагностированы у 3 животных. Все они представлены хроническим циститом, в одном случае в комбинации с токсическим поражением печени.
Летальность в данной группе составила 4%.
Среди животных 4-й группы на 5-е сутки только у 4 крыс из 5 были выявлены изменения внутренних органов. В основном они приходились на мочевыделительную систему: острый цистит с единичными кровоизлияниями в стенке мочевого пузыря (3 крысы), у 2 животных данная патология была в сочетании с гиперплазией лимфоидных структур большого сальника. Также диагностирован случай острого гломерулонефрита.
Через 15 суток после начала эксперимента количество выявленной патологии сократилось до двух случаев: эпизод лобарной гнойной пневмонии и наличие опухолеподобных образований большого сальника, сочетанное с токсической дистрофией печени.
На 30-е сутки эксперимента большинство изменений приходится на почки: одиночный инфаркт и односторонний нефросклероз в сочетании с хроническим циститом и поверхностными кистами селезенки. Кроме того, выявлены гипотрофия мышц тазовых конечностей у 1 крысы и формирование опухолеподобного образования большого сальника.
Через 60 суток изменения органов, определенные в результате вскрытия, были достаточно скудные. В одном случае диагностировано опухолевидное образование большого сальника, в другом – малочисленные узелковые поражения сальника и печени, предположительно бактериальной природы.
На 90-е сутки эксперимента находки также были немногочисленны и представлены токсическим поражением печени и кишечника и эпизодом кистозного поражения большого сальника.
Летальных случаев в группе 4 не наблюдали.
При оценке состояния трупов альтерация кожных покровов, хвоста и конечностей выявлена у 26 животных. Распределение в группах было равномерным, за исключением группы 4, где их количество было минимальным и выявлено всего у 2 крыс. При этом среди животных 1-й группы кожные эрозии и язвы имели в основном трофическое происхождение, в то время как в остальных группах – преимущественно аутодеструктивное (рис. 1в).
ТСМ является одной из наиболее серьезных патологий и опасна развитием тяжелых осложнений, выраженность и характер которых зависят от уровня поражения спинного мозга [2, 10]. Согласно многочисленным источникам, наибольший удельный вес (от 13% до 90%) среди последствий ТСМ имеет расстройство функций системы мочевыделения [11, 12]. В данном эксперименте основная группа выявленных осложнений – это патология мочевыделительной системы. Различные формы цистита были диагностированы у 37,9% всех исследованных животных, более чем у половины из них – в сочетании с различной почечной патологией, чаще всего одиночными и множественными инфарктами и различными воспалительными процессами в почках. Однако в разных группах картина заболеваний мочевыделительной системы отличалась. В группе 1 животных данная патология была наиболее тяжелой и распространенной, к концу эксперимента имела характер хронического течения. В группе 3 заболевания мочевого пузыря также занимали большой удельный вес среди всех выявленных осложнений, но протекали в более легкой форме. Наилучшие результаты по данному показателю были представлены в группах 2 и 4. Однако в группе 2 по сравнению с группой 4 у животных наблюдали достаточно высокий процент патологии почек невоспалительного характера (инфаркты, липомы), что может быть результатом нарушения кровообращения и/или действия токсических факторов.
Повреждения спинного мозга на уровне грудного отдела позвоночника у 22–65% пациентов способны вызвать нарушение функций органов дыхания, чаще в виде пневмоний, ателектаза и дыхательной недостаточности [2, 13]. В проведенном эксперименте поражение легких выявили у 10,5% от всего количества животных, из них 60% случаев встречались в группе 1. В ранние сроки после ТСМ легочная патология имела единичные случаи появления и выражалась отеком легких. Основную массу гнойных поражений фиксировали с 30–60-х суток эксперимента.
Нарушения функций печени и желудочно-кишечного тракта достаточно распространены среди пациентов с ТСМ [2, 14]. В данном исследовании поражения кишечника занимали всего 7,4% от всего количества животных, причем большинство из этих случаев (85,7%) имели инфекционный характер и были диагностированы у животных 1-й группы. Найденные патологические изменения в печени указывали на интоксикацию организма и выявлены у 14,7% от общего количества крыс. Почти половина этих случаев (42,8%) обнаружена у животных 3-й группы. В остальных группах поражение печени встречалось в основном до 15-х суток эксперимента.
Привлекает внимание в исследовании патология сальника. Известно, что большой сальник обеспечивает иммунореактивность брюшной полости и размещенных в ней органов, а реактивная гиперплазия лимфоструктур может быть ответом на воспалительные процессы [15]. Наибольшее количество случаев гиперплазии и напоминающих опухоли образований лимфоидных элементов большого сальника выявлено в группах с введением Мексидола. Возможно, его применение способно индуцировать локальную воспалительную реакцию.
В целом более благоприятные показатели по развитию последствий ТСМ были среди животных группы 4. Здесь был выявлен наименьший процент осложнений, они протекали в более легкой форме. Похожие показатели имели животные в группе 2, но в данном случае поражение различных органов носило комплексный характер и было более выраженным на начальных этапах эксперимента. Наихудшие результаты наблюдали в группе 1, где количество и тяжесть осложнений, а также смертность от них были самыми высокими. Промежуточные значения наблюдали в группе 3, при этом отмечали достаточно большой процент токсического поражения органов.
Выводы
Период максимального развития осложнений контузионной травмы спинного мозга приходится на ранние сроки после повреждения, при этом наибольший удельный вес в структуре патологии занимает поражение мочевыделительной системы. Более того, при отсутствии лечебных мероприятий патологические процессы прогрессируют и приобретают характер хронического течения. Совместное применение противоспаечного геля «Антиадгезин» и нейропротектора антиоксидантного типа действия Мексидол обеспечивает положительный терапевтический эффект, при этом наилучшие результаты получены при использовании комбинации местного применения «Антиадгезина» с внутрибрюшинным введением Мексидола.
Работа выполнена в соответствии с планом научных исследований в рамках программы НИР государственного задания 2018–2020 гг. ФГБУ «НМИЦ ТО имени академика Г.А. Илизарова» Минздрава России.
Авторы заявляют об отсутствии конфликта интересов. Исследование не имело спонсорской поддержки от производителей препаратов.
Библиографическая ссылка
Кирсанова А.Ю., Кубрак Н.В. СРАВНИТЕЛЬНАЯ ХАРАКТЕРИСТИКА СИСТЕМНЫХ ОСЛОЖНЕНИЙ ПОСЛЕ МОДЕЛИРОВАНИЯ ТРАВМЫ СПИННОГО МОЗГА У КРЫС НА ФОНЕ ПРИМЕНЕНИЯ ГИДРОГЕЛЯ И НЕЙРОПРОТЕКТОРА // Современные проблемы науки и образования. – 2020. – № 6. ;URL: https://science-education.ru/ru/article/view?id=30401 (дата обращения: 25.04.2024).