Бактенецины - катионные обогащенные пролином пептиды (Prolin-Rich Peptides, PRP) системы врожденного иммунитета млекопитающих. Обогащенные пролином пептиды (ОПП) проявляют высокую антимикробную активность, причем в отличие от многих других антимикробных пептидов, которые в концентрациях, превышающих антибактериальные, токсичны и для эукариотических клеток, большинство ОПП даже в высоких концентрациях не обладают токсическим действием в отношении клеток макроорганизма [4]. Благодаря высокому содержанию пролина ОПП могут вступать во взаимодействие с разнообразными белковыми молекулами и модулировать их функциональную активность, в том числе активность белков, участвующих в ключевых биохимических процессах, протекающих как в микробных, так и в эукариотических клетках. Поэтому, кроме антимикробной активности, для некоторых ОПП показана способность влиять на целый ряд важнейших защитных реакций, протекающих при разных видах патологии. Например, для PR-39 из лейкоцитов свиньи в литературе описана способность индуцировать ангиогенез, ускорять заживление ран, ингибировать активность NADPH-оксидазной системы нейтрофилов [2; 5; 10]. Таким образом, ОПП в настоящее время рассматриваются как перспективная основа для создания новых антибиотических и иммуномодулирующих лекарственных препаратов, а детальное изучение биологических свойств различных ОПП является актуальной задачей экспериментальной медицины.
Объектом данной работы явился антимикробный пептид из семейства бактенецинов - ChВас5, выделенный нами ранее из лейкоцитов козы и, как было показано, обладающий высокой антимикробной активностью и низкой токсичностью для клеток человека [1; 9], что свидетельствовало о перспективности детального изучения этого пептида для разработки впоследствии лекарственных препаратов на основе его структуры. Исследование биологической активности пептида в отношении клеток макроорганизма представляло несомненный интерес.
Целью работы было изучение влияния бактенецина 5 из лейкоцитов козы (ChВас5) на пролиферацию фибробластов кожи человека in vitro, а также на процесс заживления кожной раны у мышей (динамику уменьшения площади раневой поверхности).
В задачи данной работы входило также исследование активности укороченных фрагментов ChBac5: N-концевого фрагмента (1-20), С-концевого фрагмента (20-43), фрагмента 7-22 и фрагмента 7-14. Изучение свойств пептидов, представляющих собой различные участки молекул природных пептидов, позволяет сделать предположение, какая часть молекулы наиболее важна для проявления того или иного вида биологической активности, а также предоставляет информацию, важную для разработки лекарсвенных препаратов на основе структур молекул пептидов. Так, проявление многих биологических свойств пептида PR-39 большинство исследователей связывает с наличием в его структуре участка, который взаимодействует с SH3 (Src Homology 3) доменами ряда белков и модулирует тем самым их функции [2; 5; 10]. Интересно, что последовательность 7-14 в молекуле ChBac5 представляет собой участок RxxPxхP (где R - остаток аргинина, Р - пролина, х - другие аминокислотные остатки), который у многих белков, в том числе PR-39, отвечает за связывание с SH3-доменами. Поэтому в работе изучали и активность фрагментов ChBac5, содержащих этот участок.
Материалы и методы
В работе использовали химически синтезированный пептид ChBac5 и его фрагменты. Пептиды были получены последовательным наращиванием пептидной цепи на р-метилбензгидриламино-полимере (Sigma, США) на синтезаторе Vega Coupler 250 (США) с помощью оксибензотриазоловых эфиров и нейтрализацией in situ, используя Boc-технологию [6]. Очистку пептидов проводили с помощью обращенно-фазовой высокоэффективной жидкостной хроматографии. Чистота полученных бактенецинов была более 99%. Они были индивидуальны по данным аналитической ВЭЖХ и аминокислотного анализа, а их молекулярные массы по данным масс-спектрометрии соответствовали расчетным.
Фибробласты кожи человека культивировали в CO2-инкубаторе в среде ДМЕМ («Биолот», Россия), дополненной глутамином, гентамицином и 10%-ной эмбриональной телячьей сывороткой. Для оценки влияния пептидов на пролиферацию фибробластов использовали МТТ-тест, основанный на способности ферментов дыхательной цепи митохондрий живых клеток восстанавливать неокрашенные формы 3-4,5-диметилтиазол-2-ил-2,5-дифенилтераразола (МТТ-реагента) до голубого кристаллического формазана [7]. Клетки (90 мкл) высеивали в стерильные планшеты (Orange Scientific, Бельгия) по 10 000 клеток на лунку. Серийные двукратные разведения пептидов проводили в среде ДМЕМ с 10%-ной эмбриональной телячьей сывороткой и вносили по 10 мкл в лунки планшетов с клетками, в четырех параллелях. В контрольные лунки добавляли по 10 мкл среды. Планшеты далее инкубировали в CO2-инкубаторе в течение 72 часов. За три часа до окончания срока инкубации в лунки планшетов добавляли по 10 мкл раствора МТТ (5 мг/мл в ЗФР). По окончании инкубации в лунки планшета вносили по 100 мкл изопропанола с 0.04 М НСl. Далее проводили измерение оптической плотности раствора в лунках планшета при длине волны 540 нм (вычитая величину оптической плотности при 690 нм, как фоновую) на спектрофотометре Spectra Max 250 (США). Для построения графиков и расчета медианной ингибирующей концентрации пептидов (ИК50) использовали программу Sigma Plot 9. При проведении статистической обработки подсчитывали среднее арифметическое и среднеквадратичное отклонение. Токсичность пептидов в отношении фибробластов кожи человека оценивали также с использованием МТТ-теста по стандартной методике.
Эксперименты по изучению влияния пептидов на процесс заживления кожной раны выполнены на взрослых мышах-самцах гибридах I поколения линии СВА (F1) , массой 18-22 г, полученных из питомника РАМН «Рапполово» (Санкт-Петербург). Животных содержали в условиях вивария при комнатной температуре, со свободным доступом к воде и пище, на стандартной диете в соответствии с нормами содержания лабораторных животных. Условия работы с животными соответствовали правилам Европейской Конвенции ЕТ/S 129, 1986 и директивам 86/609 ЕSС. Нанесение ран животным проводили под легким эфирным наркозом; на нижней части спины удаляли шерсть, кожу протирали 70%-ным этанолом и одноразовыми круглыми скальпелями для биопсий диаметром 6 мм (Stiefel, Германия) наносили по две полнослойные кожные раны. В 1, 2, 4, 6 и 8-й день эксперимента животным опытной группы на поверхность ран наносили раствор ChВас5 в концентрации 2 или 10 мкМ в полиэтиленгликоле; животным контрольной группы по той же схеме наносили полиэтиленгликоль. Для определения площади раневой поверхности раны, начиная со второго дня после воздействия, животных фотографировали цифровой фотокамерой, изображения переносили на компьютер, калибровали и измеряли площадь раневого поражения с помощью программы ImageJ 1.44p (NIH, USA). Результаты выражали в процентах от исходной площади в контрольной группе (в предварительных экспериментах было показано, что у мышей, раны которых обрабатывали полиэтиленгликолем, и у животных, раны которых не обрабатывали, площади раневой поверхности достоверно не отличались в течение всего периода наблюдений).
При проведении статистической обработки использовали программу Statistica 6. Результаты представлены как среднее арифметическое ± среднеквадратичное отклонение. Достоверность различий оценивали с использованием t-теста Стьюдента, за достоверный принимали 95%-ный уровень значимости (Р<0,05), n = 6.
Результаты исследования и их обсуждение
Структуры исследуемых в работе пептидов - обогащенного пролином линейного пептида системы врожденного иммунитета бактенецина 5 из лейкоцитов козы и пептидов, являющихся более короткими фрагментами его молекулы, представлены на рисунке 1.
1 11 21 31 41
ChBac5 RFRPPIRRPPIRPPFNPPFRPPVRPPFRPPFRPPFRPPIGPFP
ChBac5 (1-20) RFRPPIRRPPIRPPFNPPFR
ChBac5 (20-43) RPPVRPPFRPPFRPPFRPPIGPFP
ChBac5 (7-14) RRPPIRPP
ChBac5 (7-22) RRPPIRPPFNPPFRPP
Рис. 1. Первичная структура антимикробного пептида ChBac5 [9] и его производных.
Ранее нами было показано, что ChBac5 не токсичен для большинства клеток млекопитающих [1]. В данной работе была проведена серия экспериментов, подтверждающих отсутствие токсического действия этого пептида и исследуемых фрагментов его молекулы в отношении фибробластов человека. По данным МТТ-теста, ИК50 (ингибирующая концентрация 50%) для ChBac5 и всех его производных составляет более 50 мкМ (максимальная используемая концентрация пептидов). Таким образом, токсические эффекты пептидов в применяемом диапазоне концентраций не наблюдались.
Для оценки влияния ChBac5 и его фрагментов на пролиферацию фибробластов кожи человека пептиды в разных концентрациях инкубировали с клетками в течение 72 часов при 37 °С в атмосфере СО2. По данным МТТ-теста, количество жизнеспособных клеток в пробах, где присутствовал ChBac5 в концентрациях 1.25, 2.5, 5 и 10 мкМ, достоверно выше, чем в контрольных пробах, где клетки инкубировали без пептидов (рис. 2). В присутствии ChBac5 (1-20) в концентрации 10 мкМ (но не в концентрации 5, 2.5, и 1.25 мкМ) тоже наблюдается увеличение количества жизнеспособных клеток В случае других фрагментов ChBac5 достоверных различий с контролем выявлено не было.
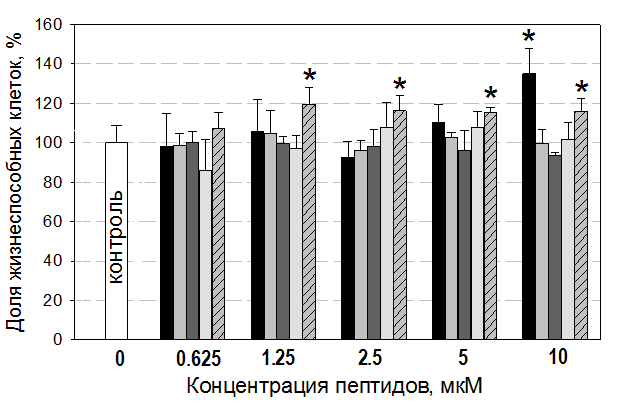
Рис. 2. Влияние бактенецина ChBac5 и его укороченных фрагментов на пролиферацию фибробластов кожи человека при инкубации пептидов с клетками 72 часа при 37 °С в атмосфере СО2 (данные МТТ-теста).
По оси Y - доля жизнеподобных клеток в процентах от контроля (фибробласты, которые инкубировали без добавления пептидов). По оси Х - концентрация пептидов в мкМ.
 - ChBac5;
- ChBac5;  - ChBac5 (1-20);
- ChBac5 (1-20); ![]() - ChBac5 (7-14);
- ChBac5 (7-14);
![]() - ChBac5 (7-22);
- ChBac5 (7-22); ![]() - ChBac5 (20-43).
- ChBac5 (20-43).
* - р < 0.05 по сравнению с контролем, n=6 (t-критерий Стьюдента).
Таким образом, полноразмерный пептид ChBac5 оказывает стимулирующее действие на пролиферацию фибробластов, его N-концевой фрагмент проявляет аналогичное действие, хотя и в меньшей степени. Эти данные согласуются с результатами, описанными в литературе для обогащенного пролином пептида из лейкоцитов свиньи PR-39: биологическая активность, связанная с взаимодействием с SH3 доменами, показанная для полноразмерного PR-39, наблюдалась лишь для фрагментов его молекулы, содержащих как SH3-связывающий участок, так и N-концевые аминокислоты. Важность N-концевого фрагмента была показана для ряда бактенецинов [4]. Интересно, что у бактенецина 5 быка, имеющего значительное структурное сходство с бактенецином 5 козы, не только N-концевой фрагмент проявляет антимикробную активность, но и участок, сходный с участком 7-22 ChBac5 [8], в то время как у бактенецина 5 козы, как было нами ранее показано, фрагмент 7-22 лишен антимикробной активности. Полученные данные позволяют сделать заключение о важности N-концевого участка молекулы ChBac5 не только для проявления антимикробной, но и митогенной активности.
Учитывая полученные данные о влиянии бактенецина козы ChBac5 на пролиферацию фибробластов, возник вопрос, обладает ли этот пептид влиянием на процесс заживления ран. Для выявления эффекта действия этого пептида на процесс ранозаживления у мышей использовали следующую модель: экспериментальным животным наносили две полнослойные кожные раны диаметром 6 мм и обрабатывали раневую поверхность раствором ChВас5 в полиэтиленгликоле (2 мкМ и 10 мкМ) на 1, 2, 4, 6 и 8-й дни. Площадь раневой поверхности измеряли, фотографируя животных цифровой фотокамерой и анализируя полученные изображения с помощью программы ImageJ 1.44p (NIH, USA).
Уже на второй день после воздействия площадь раневого поражения достоверно ниже у мышей, раны которых обрабатывали пептидом в концентрации 10 мкМ по сравнению с контрольной группой животных, у которых раны обрабатывали тем же растворителем, но без пептида (p<0.05, t-критерий Стьюдента) - рисунок 3.
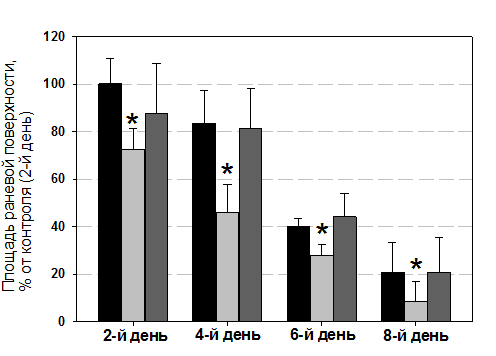
Рисунок 3. Влияние ChBac5 на динамику уменьшения площади раневой поверхности (модель полнослойной кожной раны у мышей).
По оси Y - площадь раневой поверхности в процентах от контроля (площадь раневой поверхности у животных, раны которых обрабатывали раствором, не содержащим пептид; измерения проводили на 2-й день после нанесения раны). По оси Х - концентрация пептидов в мкМ. ![]() - ChBac5 (10 мкМ);
- ChBac5 (10 мкМ); ![]() - ChBac5 (2 мкМ);
- ChBac5 (2 мкМ);![]() - контроль (без пептида).
- контроль (без пептида).
* - р < 0.05 по сравнению с контрольной группой, в которой измерения проводили в тот же день, n=6 (t-критерий Стьюдента).
В предварительных экспериментах было показано, что у мышей, раны которых обрабатывали полиэтиленгликолем, и у животных, раны которых не обрабатывали, площади раневой поверхности достоверно не отличались в течение всего периода наблюдений, поэтому на рисунке данные для этой группы животных не приводятся.
На 4, 6 и 8-й дни площадь раневой поверхности также была примерно на 30% ниже при обработке ран 10 мкМ раствором ChВас5, в то время как пептид в концентрации 2 мкМ не влиял на заживление ран на всем промежутке времени наблюдения за течением раневого процесса. На 11-й день площадь раневого дефекта была незначительна для всех исследуемых групп животных. Во всех группах раны заживали без инфицирования. На более поздних сроках наблюдения существенного образования рубцов в контроле и опытных пробах не выявлялось. Таким образом, хотя на данном этапе не проводили детального изучения влияния аппликации пептида на морфологические показатели, характеризующие процесс регенерации кожи, показано, что применение ChBac5 влияет на динамику заживления ран у экспериментальных животных. Дальнейшее изучение этого эффекта позволит прояснить механизм действия пептида.
Заключение
Таким образом, в результате проведенной работы показано, что ChBac5 оказывает стимулирующее действие на пролиферацию фибробластов кожи человека, причем из исследованных укороченных фрагментов молекулы бактенецина этим видом активности обладает лишь его N-концевой фрагмент 1-20. Кроме того, показано, что обработка кожных ран у экспериментальных животных приводит к более быстрому уменьшению площади раневой поверхности по сравнению с контрольными животными. Таким образом, полученные данные позволяют предположить, что данный вид активности обогащенных пролином пептидов не является случайным, обнаруженным только для АМП одного вида животного, а может играть важную роль в модуляции защитных реакций организма. Кроме того, ранозаживляющее действие бактенецина ChBac5 в сочетании с его антибактериальной активностью свидетельствует о возможном применении этого пептида для коррекции патологических процессов, связанных с раневыми инфекциями.
Благодарности
Авторы выражают искреннюю благодарность сотрудникам ГосНИИ ОЧБ А.Г. Александрову и Е.А. Варюшиной за консультативную помощь.
Рецензенты
- Янковский О.Ю., д.биол.н., зав. отделом Медицинской биотехнологии, ООО «Аллерготест», г. Санкт-Петербург.
- Рыбакина Е.Г., д.биол.н., зав. лабораторией нейроиммуномодуляции, ФГБУ НИИЭМ СЗО РАМН, г. Санкт-Петербург.
Библиографическая ссылка
Ямщикова Е.В., Орлов Д.С., Пазина Т.Ю., Трулев А.С., Орлов С.Б., Григорьев А.В., Колодкин Н.И., Кокряков В.Н., Шамова О.В. ВЛИЯНИЕ АНТИМИКРОБНОГО ПЕПТИДА БАКТЕНЕЦИНА 5 И ЕГО УКОРОЧЕННЫХ ФРАГМЕНТОВ НА ПРОЛИФЕРАЦИЮ ФИБРОБЛАСТОВ КОЖИ ЧЕЛОВЕКА И НА ПРОЦЕСС ЗАЖИВЛЕНИЯ РАН У ЭКСПЕРИМЕНТАЛЬНЫХ ЖИВОТНЫХ // Современные проблемы науки и образования. – 2012. – № 3. ;URL: https://science-education.ru/ru/article/view?id=6127 (дата обращения: 25.04.2024).



