В последние годы обнаружена группа заболеваний, характеризующихся прогрессирующим поражением различных отделов нервной системы и имеющих необычный генетический механизм возникновения и развития. На основании сходства морфологического дефекта при этих заболеваниях их объединяют в группу спонгиоформных энцефалопатий [3]. Долгое время считалось, что клинические симптомы этих болезней возникают при попадании в организм инфекционного агента, имеющего антигенное сродство к нервным клеткам. Предполагалось, что в этом случае запускается механизм иммунного ответа, продолжающийся и после исчезновения из организма инфекционного агента, что приводит к образованию комплекса «антиген-антитело» и гибели нейронов [3].
Вскоре стало ясно, что основная патогенетическая роль в развитии этих заболеваний принадлежит белковому агенту, который было предложено называть прионом [1, 2]. В группу прионных болезней входят куру, болезнь Крейтцфельдта-Якоба (БКЯ), болезнь Герстмана-Штросслера и летальная семейная инсомния.
Одним из сложных вопросов является диагностика прионных заболеваний. За последние 20 лет разработан ряд методик для диагностики прионных инфекций, и все они, за редким исключением, рассчитаны на постмортальное исследование мозга. Основными современными методами диагностики прионной патологии остаются различные варианты иммунологического анализа, а именно: иммуногистохимическое (ИГХ) выявление аномальной формы приона на срезах тканей мозга, вестерн-блот и выявление фибриллярных структур губчатой энцефалопатии крупного рогатого скота, аналогичных скрепи-ассоциированным фибриллам [4].
Известные методы определения видовой принадлежности животных белков не всегда оказываются эффективными. Поэтому актуальной задачей является разработка молекулярно-генетических методов идентификации прионных болезней животных. Особый интерес в данном направлении представляет разработка тест-систем на основе полимеразной цепной реакции (ПЦР).
Важным фактором, определяющим эффективность ПЦР-метода идентификации прионных болезней животных, является способ консервирования биологической пробы (ДНК).
Консервирование при низких температурах (криоконсервирование) является самым распространенным и эффективным методом сохранения качества животного и растительного сырья. Известно, что охлаждение проб, содержащих нуклеиновые кислоты, до +4 °С может лишь приостановить процессы биодеградации. Для более длительного хранения используют низкие температуры от -20 °С до -195,8 °С, например, в условиях промышленных холодильных установок или в жидком азоте [6].
К недостаткам метода криоконсервации биологических проб следует отнести потенциальную возможность сохранения патогенных возбудителей вместе с образцом, необходимость постоянного поддержания бесперебойной работы холодильного оборудования и обязательной организации фиксации терморежимов хранения и бесперебойного энергоснабжения [6].
Возможна консервация ДНК-содержащих образцов этиловым спиртом, формалином или их сочетанием, которые обезвоживают ткани и обладают антимикробным, антиферментным и антиокислительным действием [7].
Известен способ хранения проб биологического происхождения методом FTA Gene Guard [5]. Метод FTA Gene Guard предполагает нанесение проб биологических жидкостей на фильтровальную бумагу, обработанную буфером, содержащим мощные денатурирующие вещества, которые также предотвращают рост бактерий и других микроорганизмов. Клеточные элементы биологической пробы на FTA-бумаге подвергаются лизису. ДНК высвобождается из ядер лейкоцитов и иммобилизуется на матриксе бумаги. Связанная таким образом ДНК может быть освобождена от гема или других ингибиторов ПЦР отмыванием, после чего FTA-бумага с иммобилизованной на ней ДНК может вводиться непосредственно в соответствующую амплификационную смесь.
Предложен метод консервирования проб для ПЦР-анализа, предполагающий инкапсулирование предварительно обезвоженных молекул ДНК в герметичную нержавеющую металлическую капсулу в атмосфере, состоящей из одного или нескольких инертных газов и имеющей степень влажности меньше или равную 1 млн-1 воды [5].
Эффективным является способ хранения биологического материала, заключающийся в следующем. После выделения и очистки образец ДНК в виде 100-500 мкл водного раствора наносят на обеззоленную фильтровальную бумагу, аккуратно промывают двойным объемом 96 %-го этанола. Полученные носители с ДНК в течение 30 минут подсушивают в термостате при температуре 50 °С и ламинируют, поместив последовательно между листами стандартной офисной бумаги (например, SVETOCOPY, плотностью 80 г/м2) и ламинатной пленкой (толщина 80-150 мкм). Предлагаемый способ прост в исполнении, имеет низкую себестоимость и при этом длительное время хранения, не влияет на качество иммобилизованной ДНК, что позволяет использовать такие препараты для методов молекулярно-генетического анализа, основанных на амплификации как митохондриальной, так и ядерной ДНК [5].
Цель исследования
Настоящее исследование направлено на изучение влияния условий хранения биологического образца на эффективность ПЦР-анализа при идентификации прионных болезней животных.
Материалы и методы исследования
Выделение ДНК из образцов осуществляли путем лизиса на основе гуанидинтиоционата с последующей нуклеосорбцией на магнитном силикагеле с использованием коммерческого набора реагентов «Magn S_DNA-uni» («Биоком», Москва). В состав коммерческого набора реагентов входят следующие растворы: лизирующий буфер ЛБ, отмывочный буфер ОБ, отмывочный буфер ОБ 2, буфер ТЕ, магнитный сорбент.
Схема выделения и очистки ДНК при помощи набора «Magn S_DNA-uni» представлена на рис. 1.
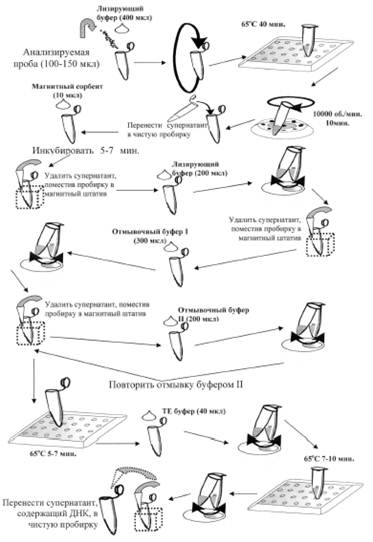
Рис. 1. Схема выделения и очистки ДНК при помощи набора «Magn S_DNA-uni»
Результаты исследования и их обсуждение
В настоящей работе исследовали влияние способа консервирования биологического образца (ДНК свиньи) на эффективность ранее разработанного ПЦР-метода идентификации прионных болезней животных. Были исследованы следующие способы консервирования:
- температура +4 °С;
- температура -20 °С;
- температура -195,8 °С;
- метод FTA Gene Guard;
- инкапсулирование обезвоженных молекул ДНК;
- нанесение водного раствора ДНК на обеззоленную фильтровальную бумагу.
Полученные результаты представлены в табл. 1.
Таблица 1 Влияние способа консервирования биологического образца на эффективность ПЦР метода
|
№, п/п |
Способ консервирования |
Количество исследованных проб |
Количество положительных проб |
% положительных проб от общего числа исследованных |
|
1 |
Температура +4 °С |
35 |
3 |
8,6 |
|
2 |
Температура -20 °С |
60 |
26 |
43,3 |
|
3 |
Температура -195,8°С |
55 |
21 |
38,2 |
|
4 |
Метод FTA Gene Guard |
70 |
54 |
77,1 |
|
5 |
Инкапсулирование обезвоженных молекул ДНК |
25 |
5 |
20,0 |
|
6 |
Нанесение водного раствора ДНК на обеззоленную фильтровальную бумагу |
40 |
24 |
60,0 |
Из табл.1 следует, что наиболее эффективными способами консервирования образцов ДНК свиньи являются метод FTA Gene Guard (77,1 % положительных проб от общего числа исследованных), нанесение водного раствора ДНК на обеззоленную фильтровальную бумагу (60,0 %) и замораживание до температуры -20 °С (43,3 %). Наименее предпочтительным способом консервирования является хранение при температуре +4 °С (8,6 %).
Далее с использованием разработанной ПЦР-тест-системы были протестированы пробы материала, взятого у свиней и хранившегося в течение 2-х недель методом FTA Gene Guard. Параметры ПЦР-анализа для исследования проб представлены в табл. 2.
Таблица 2 Компоненты полимеразной цепной реакции для исследования образца ДНК свиньи
|
Компонент |
Конечная концентрация |
Количество компонента на 50 мкл смеси |
|
1 |
2 |
3 |
|
10X ПЦР-буфер |
1X |
5 мкл |
|
10 мМ смесь дезоксинуклеотидтрифосфатов (дНТФ) |
0,2 мМ каждого |
1 мкл |
|
Праймер 1 (50 мкМ) |
1 мкМ |
1 мкл |
Продолжение таблицы 2
|
1 |
2 |
3 |
|
Праймер 2 (50 мкМ) |
1 мкМ |
1 мкл |
|
Taq-ДНК-полимераза |
1,25 ед. |
0,5 мкл |
|
25 мМ МgCl2 |
1-5 мМ |
2-5 мкл |
|
ДНК-матрица |
0,1-1 мкг |
Варьирует от концентрации образца |
|
Деионизированная вода |
- |
До 50 мкл |
Параметры амплификации представлены в табл. 3
Таблица 3 Параметры амплификации
|
Стадия |
Количество циклов |
Температура,°С |
Время инкубации |
|
|
Предварительная денатурация |
1 |
95 |
1 мин |
|
|
Денатурация |
30 |
95 |
30 с |
|
|
Отжиг |
56 |
1 мин |
||
|
Элонгация |
72 |
30 с |
||
Результаты, полученные в ходе эксперимента при исследовании материала ДНК свиньи, представлены в табл. 4.
Таблица 4
Результаты идентификации ДНК в исследуемом материале
№, п/п |
Наименование |
Длина ПЦР-ампликона, п.н. |
1 |
Положительный контроль |
153 |
2 |
Исследуемый образец |
- |
Таким образом, разработанная ПЦР-тест-система дает возможность проводить диагностику прионных болезней с высокой чувствительностью и надежностью.
Заключение
В работе исследованы шесть способов хранения биологического образца (ДНК свиньи) на эффективность ПЦР-анализа. Установлено, что наиболее эффективными способами консервирования образцов ДНК свиньи являются метод FTA Gene Guard (77,1 % положительных проб от общего числа исследованных), нанесение водного раствора ДНК на обеззоленную фильтровальную бумагу (60,0 %) и замораживание до температуры -20 °С (43,3 %). Наименее предпочтительным способом консервирования является хранение при температуре +4 °С (8,6 %).
*Работа выполнена в рамках федеральной целевой программы «Исследования и разработки по приоритетным направлениям развития научно-технологического комплекса России на 2007-2013 годы» (государственный контракт № 16.512.11.2077).
Рецензенты:
- Просеков Александр Юрьевич, доктор технических наук, профессор, проректор по НИР ФГБОУ ВПО «Кемеровский технологический институт пищевой промышленности», г. Кемерово.
- Майоров Александр Альбертович, доктор технических наук, профессор, директор ГНУ СибНИИС СО Россельхозакадемии, г. Барнаул.
Библиографическая ссылка
Асякина Л.К., Сухих С.А., Изгарышев А.В., Линник А.И. ВЛИЯНИЕ УСЛОВИЙ ХРАНЕНИЯ БИОЛОГИЧЕСКОГО ОБРАЗЦА НА ЭФФЕКТИВНОСТЬ ПОЛИМЕРАЗНОЙ ЦЕПНОЙ РЕАКЦИИ ПРИ ИДЕНТИФИКАЦИИ ПРИОННЫХ БОЛЕЗНЕЙ ЖИВОТНЫХ // Современные проблемы науки и образования. – 2012. – № 3. ;URL: https://science-education.ru/ru/article/view?id=6390 (дата обращения: 19.04.2024).



