Введение
Аммиак используется в химической промышленности при производстве минеральных удобрений и азотной кислоты. Но наиболее широко он применяется в качестве хладагента в холодильных установках на предприятиях пищевой промышленности. На этих предприятиях возможны утечки газа, что является опасным как для персонала, работающего на предприятии, так и для населения близлежащих районов, поэтому проблемы улавливания аммиака в вентиляционных выбросах, а также защиты органов дыхания во время аварийных выбросов являются очень актуальными.
Известно, что кремнеземные адсорбенты нашли разнообразное применение в качестве избирательных поглотителей, носителей активной фазы в катализе и т.п. Большое развитие получило химическое модифицирование поверхности дисперсного кремнезема с целью направленного изменения его сорбционных свойств. Наиболее распространенными кремнеземными сорбентами являются силикагели. Поглотительные свойства сорбентов и силикагелей в том числе, в значительной степени определяются такими основными характеристиками, как пористая структура, химический состав и строение поверхности. Роль природы поверхности в процессах адсорбции приобретает особенно большое значение в связи с разработкой новых приемов модифицирования поверхности адсорбентов, а также в результате бурно развивающихся в последние десятилетия новых направлений - нанотехнологии и наноматериалов.
Перспективным направлением является ультразвуковая пропитка пористых тел, которая основана на звукокапиллярном эффекте [6]. При этом жидкость как бы «вгоняется» в капилляры, и эффективность обработки значительно повышается. Использование акустических колебаний в процессах сорбции позволяет резко сократить продолжительность насыщения сорбента, а в некоторых случаях и увеличить его емкость.
Наша исследовательская группа изучала влияние модифицирования на сорбционную способность силикагелей. Ранее установлено [1] , что размер пор силикагелей влияет на их поглотительные свойства по отношению к аммиаку. Показано, что термически модифицированный мелкопористый силикагель обладает лучшими сорбционными свойствами.
Целью настоящей работы явилось выявление механизма удерживания аммиака поверхностью термохимически модифицированных силикагелей, в том числе после пропитки сорбентов активирующим раствором в ультразвуковом поле.
Материалы и методы исследования
Исследовали силикагели марок КСКГ (крупнопористый силикагель) и КСМГ (мелкопористый силикагель). Диаметр пор крупнопористого силикагеля до 100 нм, мелкопористого - до 3 нм, удельная поверхность у КСКГ от 210 до 350 м2/г, у КСМГ от 550 до 900 м2/г. Исходя из этого, данные сорбенты можно отнести к нанопористым силикагелям: КСКГ100 и КСМГ3. Химическую обработку термически активированных сорбентов проводили в 0,1 М растворе сульфата меди в течение 24 часов при комнатной температуре, после чего высушивали при температуре 120 - 130 оС до постоянной массы. Фотоколориметрическим методом установили время, в течение которого происходило насыщение сорбентов активирующим раствором, для чего использовали фотоколориметр марки КФК - 2 - УХЛ 4.2, кювету 5 см, светофильтр с длиной волны λ = 590 нм. Кроме того, пропитку сорбентов проводили в ультразвуковой установке ULTRASONIC CLEANER (WAH LUEN ELTRTRONIC TOOLS. CO. LTD) при заранее выбранном оптимальном режиме [2]: мощность 60 Вт и время 100 с. Адсорбцию паров аммиака изучали гравиметрическим методом в статических условиях [3]. В эксикаторах создавали среду аммиака с объемными концентрациями паров 5, 10, 20, 50, 100, 200 и 400 мг/м3, для чего готовили растворы аммиака различной концентрации в соответствии с данными справочника [5]. Поскольку в исследуемых условиях содержание паров воды в 1,3 - 1,6 раз меньше, чем аммиака, то преимущественно сорбируется аммиак. Десорбцию аммиака химически модифицированными силикагелями изучали на сорбентах, насыщенных в среде аммиака с объемной концентрацией 200 мг/м3, при комнатной температуре, а также в потоке горячего воздуха при температурах 150 - 175 0С и 250 - 2750С в сушильном шкафу марки ШC - 80 СПУ. Исследование оптического поглощения в ИК-области спектра (4000-550 см-1) проводили с помощью ИК - Фурье спектрометра Vertex 70 (Брукер) с приставкой НПВО, применяли призму из ZnSe с алмазным покрытием.
Результаты исследования и их обсуждение
На рис.1 приведены кинетические зависимости пропитки силикагелей раствором медного купороса, на основе данных можно сделать два вывода. Во-первых, насыщение сорбентов раствором сульфата меди происходит через 10 часов.
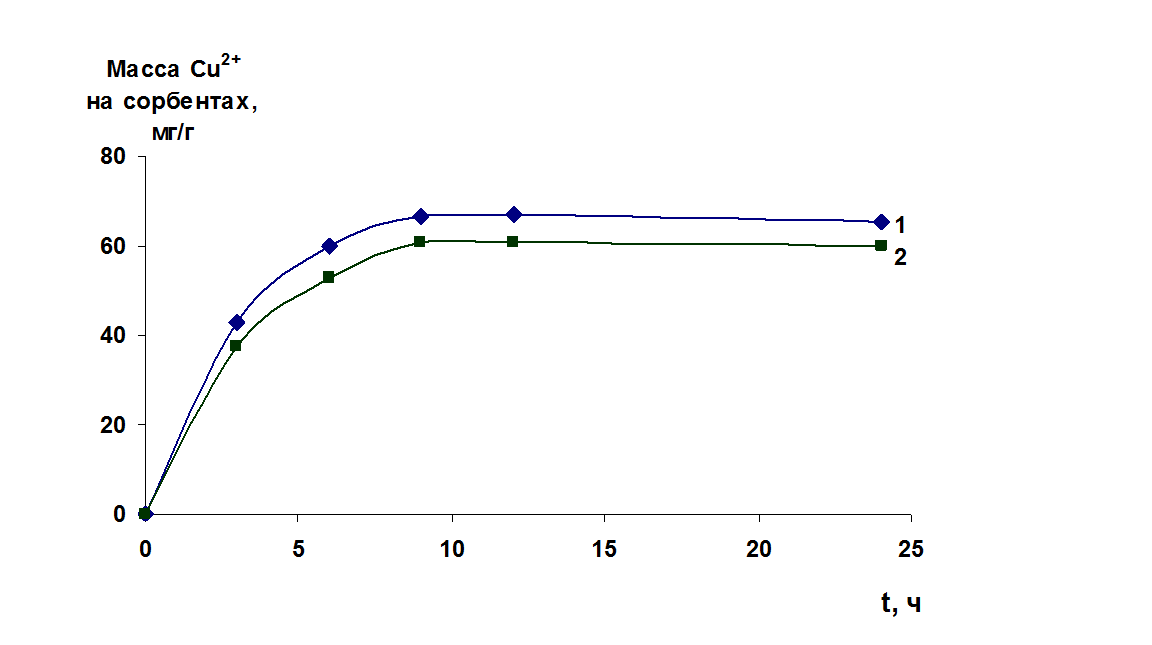
Рис.1. Зависимость массы катионов меди на сорбентах в процессе пропитки раствором CuSO4 от времени: 1 - силикагель марки КСКГ100; 2 - силикагель марки КСМГ3
Во-вторых, на поверхности образца КСКГ100 концентрация катионов меди больше, чем у образца КСМГ3. Результаты импрегнирования сорбентов в ультразвуковом поле показаны в табл.1
Таблица 1 Адсорбция аммиака сорбентами, пропитанными раствором CuSO4 в ультразвуковом поле
|
Условия обработки сорбентов |
Адсорбция (а, мг/г) в течение 46 ч в среде аммиака с объемной концентрацией 100 мг/м3 |
|
|
Силикагель КСКГ100 |
Силикагель КСМГ3 |
|
|
УЗ обработка при мощности 60 вт в течение 100 с |
140,3 |
300,7 |
|
Без УЗ обработки |
129,0 |
285 |
|
Результат |
Адсорбция увеличилась на 8 % |
Адсорбция увеличилась на 5 % |
В условиях настоящих исследований в ультразвуковом поле происходит пропитка пор сорбентов раствором сульфата меди. В растворе, как известно, катионы Cu2+ в свободном виде не существуют. Они образует аквакомплексы с молекулами воды, которые придают раствору голубую окраску. Комплексные катионы имеют пространственную форму квадрата (рис. 2):
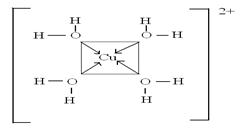
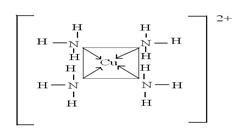
а) б)
Рис.2. Строение комплексных ионов, образующихся при насыщении сорбентов раствором CuSO4, и дальнейшей адсорбцией аммиака в их порах: а) аквакомплекс; б) амминокомплекс
Размеры сторон квадрата ~ 0,4 нм, а диагонали ~ 0,6 нм. Комплексные ионы легче проходят в крупные поры, чем в мелкие. Таким образом, в результате пропитки силикагелей раствором медного купороса их поры содержат аквакомплексы [Cu(H2O)4]2+. Характерный голубой цвет появляется после обработки раствором CuSO4 на гранулах крупнопористого силикагеля. У мелкопористого силикагеля голубой цвет выражен слабее. После проведения процесса сорбции на силикагеле КСКГ100 наблюдается интенсивный синий цвет, характерный для амминокомплексов меди [Cu(NH3)4]2+, что можно расценить как своеобразный аналитический сигнал. Следовательно, происходит реакция
[Cu(H2O)4]2+ + 4NH3 = [Cu(NH3)4]2+ + 4H2O.
Прочность этого амминокомплекса сравнительно велика [5]: рК = - lg Kнест. = 12,03. У нанопористого силикагеля КСМГ3 цвет изменяется в меньшей мере, преимущественно при больших объемных концентрациях аммиака.
Результаты опытов показали (табл.1), что у КСКГ100 после воздействия ультразвука адсорбция увеличивается в большей степени, чем у КСМГ3, что обусловлено, в основном, образованием донорно-акцепторных связей с катионами меди по приведенной выше реакции. Поэтому у КСКГ100 химическая составляющая адсорбции больше, чем у КСМГ3.
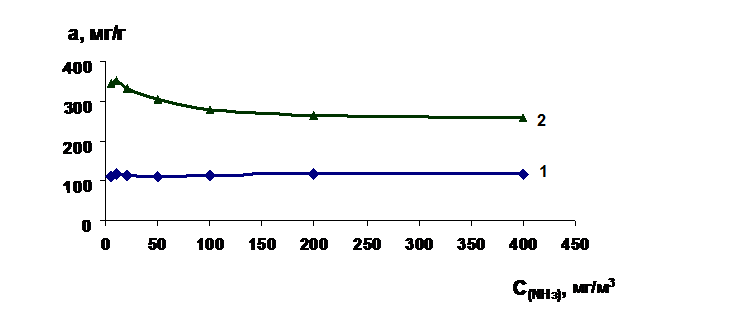
Рис. 3. Изотермы адсорбции химически модифицированных силикагелей разной пористости: 1 - силикагель КСКГ100; 2 - силикагель КСМГ3
На основе изучения адсорбции аммиака термохимически модифицированными силикагелями разной пористости получили изотерму адсорбции (рис.3).
Обращает на себя внимание то обстоятельство, что КСМГ3 обладает большей сорбционной способностью по отношению к аммиаку по сравнению с крупнопористым силикагелем КСКГ100. Это связано с особенностями поверхностной структуры кремнеземных сорбентов. Известно [7,4], что на поверхности силикагелей имеются силанольные группы ≡ SiOH , которые при сближении друг с другом на расстояние 0,3 нм могут взаимодействовать друг с другом, образуя водородную связь. При этом возникают вицинальные группы (рис.4). Эти поверхностные группы являются очень активными. Они могут образовывать водородную связь с полярными молекулами, в том числе с аммиаком. Так как удельная поверхность у КСМГ3 больше, чем у КСКГ100 , то таких активных групп у него также больше.
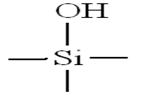
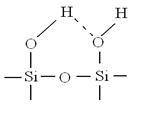
а) б)
Рис. 4. Активные структурные группы, имеющиеся на поверхности силикагелей: а) силанольная группа; б) вицинальная группа
С целью подтверждения предполагаемого механизма сорбции проведено изучение десорбционных процессов аммиака при комнатной температуре, а также при повышенных температурах в потоке горячего воздуха. Результаты представлены в табл.2.
Таблица 2 Десорбция аммиака (мг/г) термохимически модифицированными сорбентами, насыщенными в парах аммиака с объемной концентрацией 200 мг/м3
|
Условия десорбции |
Силикагель КСКГ100 |
Силикагель КСМГ3 |
|
На воздухе при комнатной температуре |
65,3 |
97.8 |
|
В потоке горячего воздуха при 150-175 оС, (время 3 ч) |
53,2 |
216,9 |
|
В потоке горячего воздуха при 250-275 оС, (время 3 ч) |
15,2 |
4,4 |
При комнатной температуре большая десорбция наблюдается у КСМГ3. Это можно объяснить тем, что в среде с большим содержанием адсорбтива в мелких порах происходит многослойное заполнение за счет физических сил взаимодействия между слоями молекул. Чем больше объемная концентрация аммиака, тем больше происходит заполнение микропор. Что касается крупных пор, то они являются лишь транспортными каналами, по которым проходят молекулы адсорбата к более эффективным в смысле адсорбции узким порам [3]. В крупных порах ван-дер-ваальсовы силы могут проявить свое действие лишь в пределах мономолекулярного слоя.
Выдерживание адсорбентов, насыщенных в среде аммиака с концентрацией 200 мг/м3, при 150 - 175 0С показало, что десорбция аммиака с поверхности крупнопористого силикагеля составила за 3 часа 53,2 мг/г, а мелкопористого - 216,9 мг/г. Причем дополнительное выдерживание образцов при этой температуре еще 4 часа не увеличило десорбцию аммиака. Можно предположить, что при температуре 150 - 175 оС десорбируются с поверхности сорбентов молекулы аммиака, связанные с ними водородными связями. Результаты опыта показывают, что у КСМГ3 преобладает адсорбция, обусловленная водородными связями. Десорбция химически связанных молекул аммиака в амминокомплексах с катионом меди происходит при 250 - 275 оС и сопровождается изменением цвета. Крупнопористый силикагель приобретает более светлую окраску голубовато-зеленых тонов, а мелкопористый силикагель становится бесцветным. Это свидетельствует о том, что с разрушением амминокомплексов начинается удаление молекул аммиака, связанных с катионами меди Cu2+ донорно-акцепторными связями. Эти процессы более выражены у силикагеля КСКГ100, что обусловлено тем, что химическая составляющая адсорбции у него больше, чем КСМГ3.
Результаты исследования адсорбционно-десорбционных процессов хорошо согласуются с данными ИК-спектроскопии. Уменьшение интегральной интенсивности валентных колебаний ОН-групп (950 см-1) при адсорбции аммиака с одновременным появлением ярко выраженного пика в области 3280-3400 см-1, принадлежащего валентным колебаниям связи N-H, указывает на образование водородной связи групп N-H с гидроксильными группами. Интегральная интенсивность полосы поглощения аммиака в образцах КСМГ3 заметно больше (в ~ 2,3 раза), чем в крупнопористом, что указывает на более высокую адсорбционную способность мелкопористого силикагеля. Отсутствие у обработанных раствором CuSO4 силикагелей ярко выраженной полосы поглощения в области 3280-3400 см-1 является следствием образования аммиаком амминокомплекса с медью.
Заключение
Таким образом, исследовано поглощение аммиака термохимически модифицированными силикагелями разной пористости с целью выявления механизма процесса. Показано, что у силикагеля КСМГ3 преобладает удерживание молекул аммиака ван-дер-ваальсовыми силами физической адсорбции, а также водородной связью с активными структурными группами на его поверхности (силанольными и вицинальными). У крупнопористого силикагеля превалирует химическая составляющая адсорбции за счет образования донорно-акцепторной связи с катионами меди активирующего раствора. Знание механизма процесса адсорбции аммиака данными сорбентами позволит выбрать оптимальные условия их промышленного использования.
Работа выполнена на оборудовании ЦКП «НЭНТП» в рамках госконтракта № 16.552.11.7048
Рецензенты:
- Бельчинская Лариса Ивановна, доктор технических наук, профессор, заведующая кафедрой химии Воронежской государственной лесотехнической академии, г. Воронеж.
- Хохлов Владимир Юрьевич, доктор химических наук, профессор кафедры аналитической химии Воронежского государственного университета, Воронеж.
Библиографическая ссылка
Горшунова В.П., Небольсин В.А., Лукин А.Н. МЕХАНИЗМ ПОГЛОЩЕНИЯ АММИАКА ТЕРМОХИМИЧЕСКИ МОДИФИЦИРОВАННЫМИ НАНОПОРИСТЫМИ КРЕМНЕЗЕМНЫМИ СОРБЕНТАМИ // Современные проблемы науки и образования. – 2012. – № 3. ;URL: https://science-education.ru/ru/article/view?id=6437 (дата обращения: 20.04.2024).



