Незаразные болезни у птиц возникают в результате суммарного воздействия неблагоприятных факторов и имеют стертые клинические признаки, поэтому диагностика заболеваний вызывает затруднения [1]. При скармливании малопереваримых грубых, бедных минералами и витаминами А, D и группы В (особенно В2) кормов, вызывающих раздражение слизистой оболочки клоаки, у кур может развиться клоацит. Иногда причинами клоацита у молодых несушек может быть затрудненная яйцекладка. Способствующим фактором в развитии болезни является нарушение санитарно-гигиенических условий содержания (высокая влажность, наличие вредных газов, гниющие остатки корма и разлагающегося помета).
По нашим наблюдениям на отдельных птицеводческих предприятиях от воспаления клоаки страдают от 5,6 до 12% кур продуктивного возраста. В фермерских и личных подсобных хозяйствах в случаях нарушения условий кормления и содержания, игнорирования первых признаках заболевания возможно появление массовых клоацитов [2].
Гипотеза: воспаление клоаки у кур сопровождается рядом сопутствующих синдромов или заболеваний.
Цель исследования: комплексная диагностика и разработка стратегии терапевтической помощи больным птицам.
Условия, объект, предметы и методы исследований
Больные куры кросса «Хайсекс-браун» 2-летнего возраста поступили в стационар при кафедре акушерства, хирургии и незаразных болезней животных ФГБОУ ВПО «ИГСХА им. акад. Д.К. Беляева» 21.11.2014 г. с жалобами владельца личного подсобного хозяйства на затяжную линьку, прекращение яйцекладки, угнетение, снижение аппетита, повышенную жажду у птиц, выделение из клоаки зловонного пенистого помета.
Объектом исследования были больные куры.
Предметом для исследования послужили: клиническое состояние пациентов, кровь и помет птиц.
Методы исследования. Начальный этап диагностики включал клинические методы исследования, такие как осмотр, пальпацию, термометрию.
Взятие крови проводили из подкрыльцовой вены в вакуумные пробирки для специальных биохимических и гематологических исследований сыворотки и цельной крови с активатором свертывания и К2+ЭДТА соответственно.
Содержание гемоглобина оценивали по методу Сали, подсчет форменных элементов проводили в камере Горяева с реактивом Фриеда и Лукачевой (в модификации И.А. Болотникова), дифференцированный подсчет лейкоцитов в мазках крови, окрашенных по Diff-Quick, осуществляли с помощью микроскопа Микмед-2 при увеличении х1600 (окуляр х16, объектив х100).
Анализ состава сыворотки и плазмы крови проводили на предмет содержания общего белка, альбуминов, мочевины, глюкозы, холестерола, триглицеридов, кальция, фосфора, аспартатаминотрансферазы (АСТ), лактатдегидрогеназы (ЛДГ), щелочной фосфатазы (ЩФ), α-амилазы на биохимических анализаторах BioChem BA и BA-88A (mindray) Semi-auto-chemistry Analyzer в сертифицированном лечебно-профилактическом и лабораторно-диагностическом центре «Ветасс», организованном при кафедре.
Для копрологических исследований проводили забор помета из клоаки. Исследования проводили путем визуальной оценки. Для клинического анализа кала использовали набор реагентов «Клиника-кал» (ЗАО «ЭКОлаб»). Оценку рН выполнили универсальной индикаторной полоской; определение переваримой и непереваримой клетчатки путем приготовления нативных неокрашенных препаратов с глицерином; крахмала внутриклеточного и внеклеточного, цист простейших, нормальной и патологической йодофильной микрофлоры, эритроцитов, лейкоцитов, эпителия – с раствором Люголя; выявление нейтральных жиров и капель жирных кислот – Суданом III; для дифференциации капель жирных кислот от капель нейтрального жира – раствором метиленового синего; определение скрытой крови – раствором бензидина; билирубина – реактивом Фуше.
Результаты и их интерпретация. Клинически установлены угнетение, слабо развитые грудные мышцы, киль острый с незначительной деформацией, упитанность неудовлетворительная, видимая слизистая оболочка ротовой полости бледная, зоб умеренно наполненный, живот мягкий. Температура тела кур 41,4―41,8ºС, частота дыхательных движений в течение одной минуты 27±2,7, частота сердечных сокращений 136±3 удара в минуту.
Перьевой покров взъерошенный, матовый, в области клоаки и нижней части брюшной стенки оперение загрязнено фекалиями. Клоачное кольцо гиперемировано, отечно, отмечается геморрагическое воспаление слизистой оболочки клоаки вглубь до 2,5–3,0 см, с выделением пенистого помета светло-коричневого цвета и неприятного запаха.
Содержание гемоглобина в крови у птиц составило 120,5–124,0 г/л, эритроцитов (х1012/л) – 4,33–4,69, что несколько превышает нормы, установленные Н.С. Мотузко и соавторами (2001) [5]. Повышенное содержание гемоглобина и эритроцитов обусловлено гемоконцентрацией в результате дегидратации у кур, а цветовой показатель 0,79–0,83 свидетельствует о развитии нормохромной анемии. Лейкоцитоз и эозинофилия (21%) в сочетании с моноцитопенией (2%) связаны с воспалительным процессом, вызванным заболеванием.
При биохимическом исследовании сыворотки крови установлено, что содержание общего белка находится в пределах физиологической нормы, однако уровень альбуминов снижен на 21,0–33,5%. Снижение количества альбуминов в крови повлекло за собой снижение концентрации мочевины в 2,5 раза по сравнению с физиологическими показателями, установленными нами для данного кросса [4]. Содержание триглицеридов и холестерола у больных составило 0,89±0,04 и 1,36±0,12 ммоль/л соответственно, что не противоречит физиологическим данным при напольном содержании взрослого поголовья [4]. У кур очень высокий энергетический обмен, и концентрация глюкозы в крови значительно выше, чем у млекопитающих. Ее содержание варьирует в широких пределах и обусловлено условиями кормления, содержания, уровнем продуктивности, влиянием различных стрессоров и состоянием здоровья. При исследовании выявлена гипергликемия, достигающая 22,5±0,5 ммоль/л, (при норме 5,5–11,5 ммоль/л), что, по-видимому, связано с обезвоживанием и стрессовой реакцией при переводе кур на стационарное лечение, а также особенностями течения болезни. Низкая амилолитическая активность (370,7±4,8 ЕД/л), вероятно, носит адаптивный характер.
Напряженный минеральный обмен у птиц связан с яйцекладкой, поскольку с каждым яйцом выделяется до 2,0 г кальция и 0,1 фосфора [3]. У пациенток в среднем содержание кальция составило 3,79, фосфора – 1,99 ммоль/л, коэффициент соотношения кальций: фосфор 1,9. При условии отсутствия яйцекладки на момент исследования показатели минерального обмена находятся в пределах референтной величины. Однако энзиматическая активность щелочной фосфатазы превысила физиологически допустимый показатель, установленный нами при адекватных условиях, в 4,8 раза, что позволяет предположить развитие субклинических остеодистрофических процессов у кур [3, 4]. Повышение активности ряда ферментов, таких как АСТ до 178,1±0,8 и ЛДГ до 314,1±1,3 ЕД/л, практически в 2 раза, свидетельствует о системном воздействии токсических продуктов воспаления на желудочно-кишечный тракт, поджелудочную железу и печень птиц. Данные исследования помета птиц представлены в таблице.
Клинический анализ помета птиц
|
Показатель |
Содержание в пробе |
Показатель |
Содержание в пробе |
|
Цвет |
светло коричневый |
Клетчатка |
|
|
Запах |
резкий зловонный |
переваримая |
+ + |
|
Консистенция |
не оформленный, пенистый |
непереваримач |
+ |
|
рН, ед. |
6,5 |
Слизь |
+ + + |
|
Скрытая кровь |
+ + + + |
Билирубин |
- |
|
Крахмал |
|
Стеркобилин |
+ |
|
внутриклеточный |
+ |
Эритроциты |
до 20 в п/з |
|
внеклеточный |
+ + + |
Лейкоциты |
до 15 в п/з |
|
Жиры |
|
Эпителиальные клетки |
+ + + |
|
нейтральный |
+ + |
Простейшие |
ооцисты эймерий 8-10-10 в п/з |
|
мыла |
+ + |
Прочие микроорганизмы |
кокки++, палочки++, клостридии+ |
|
жирные кислоты |
- |
Яйца глист |
не обнаружены |
При исследовании помета выявлено наличие крови, эпителиальных клеток и слизи, непереваренных частиц корма, что характерно для геморрагического воспалительного процесса в кишечнике.
В экскрементах кур обнаружены ооцисты эймерий и клостридии, усугубившие течение основного заболевания (рис. 1). У взрослых кур эймериоз, как правило, имеет хроническое течение, что вместе с неудовлетворительным кормлением и качеством подстилки, ослабленной иммунной системой, повреждением слизистой оболочки кишечника, вызванным клоацитом, способствует заражению кур клостридиозом.
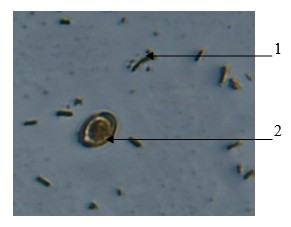
Рис.1. Микроскопия помета кур:
1. – клостридии,
2. – цисты эймерий
На основании анамнестических, клинических и лабораторных данных птицам назначили комплексное лечение, включающее диету, обогащенную тертой морковью и тыквой, дробленым чесноком, а также ежедневную смену подстилки, регулирование светового режима с 8–9-часовым ночным перерывом, ультрафиолетовое облучение в течение двух недель.
Для лечения эймериоза птице выпаивали 2,5%-ный раствор Байкокса (Bayer AG, Германия) из расчета 1 мл на 1 л воды двукратно в течение двух дней с пятидневным перерывом. В качестве средства, улучшающего аппетит и оперение, повышающего устойчивость организма к стрессам и инфекционным заболеваниям, назначен витаминно-аминокислотный препарат Чиктоник (INVESA, Испания) в дозе 1 мл на 1 л воды в течение 5 суток (в промежутке между циклами выпаивания препарата Байкокс).
Против клостридиоза курам задавали перорально Метронидазол (Биохимик, Россия) по 250 мг один раз в сутки по схеме, разработанной сотрудниками кафедры. Нитрогруппа молекулы этого препарата, являясь акцептором электронов, встраивается в дыхательную цепь простейших и анаэробов (конкурирует с электронтранспортирующими белками), вызывает нарушение дыхательных процессов, подавляет синтез ДНК, вызывает ее деградацию и приводит к гибели клеток. В терапии клоацита использовали обильное орошение 0,1%-ным раствором перманганата калия, обладающим обеззараживающим действием, околоклоачной области и клоачного кольца. После просушивания кожных покровов марлевыми тампонами вводили в клоаку одноразовым шприцем по 8–10 мл Левомеколя (Нижфарм, Россия). Левомеколь благодаря входящему в его состав антибиотику хлорамфениколу и производному пиримидина – метилурацилу обладает бактериостатическим и противовоспалительным действием, ускоряет процессы клеточной регенерации, стимулирует клеточные и гуморальные факторы защиты. Через 10 дней повторные исследования помета на наличие эймерий и клостридий дали отрицательный результат, признаков клоацита не наблюдали, гематологические и биохимические показатели крови соответствовали физиологическим нормам. Повторное исследование через трое суток подтвердило выздоровление птиц и улучшение обменных процессов.
Заключение. Проведенное комплексное исследование и терапия птиц позволяют заключить, что:
1) в основе клоацита кур, находящихся в приусадебных хозяйствах, лежит нарушение режима содержания и кормления;
2) отсутствие своевременной лечебной помощи способствует развитию осложнений, обусловленных присоединением условно патогенной и патогенной микрофлоры, отягчающей течение основной болезни;
3) энзиматические сдвиги и отклонение биохимических показателей от физиологических норм на ранних стадиях при клоаците кур носят обратимый характер и являются функционально-приспособительными ступенями при развитии патологического процесса;
4) комплексная терапия, базирующаяся на улучшении условий кормления и содержания, с применением Байкокса, Чиктоника, Метронидазола, Левомеколя позволяет восстановить здоровье и продуктивность кур.
Рецензенты:
Селезнев С.Б., д.вет.н., профессор кафедры клинической ветеринарии Российского университета дружбы народов Министерства образования РФ, г. Москва;
Здоорвинин В.А., д.вет.н., доцент, заведующий кафедрой морфологии и физиологии животных Мордовского государственного университета им. Н.П. Огарева Министерства образования РФ, г. Саранск.



