Наиболее распространенной причиной развития постменопаузального остеопороза (ПМО), сопровождающегося болью, снижением активности и качества жизни больных, что чаще всего является результатом остеопоротических переломов позвонков, проксимального отдела бедра, приводящих к инвалидизации и смерти больных, является дефицит эстрогенов. Кроме основного действия женских половых гормонов, связанного с развитием и функционированием женской репродуктивной системы, эстрогены, связываясь с рецепторами на клеточных элементах костной ткани, участвуют в регуляции костного метаболизма, формировании скелета и окостенении эпифизов трубчатых костей. В процессах ремоделирования половые стероиды регулируют совместную работу остеобластов и остеокластов, а дефицит эстрогенов приводит к активации остеокластов, нарушению минерального обмена костной ткани, снижению ее прочности [1; 2].
Основными целями лечения и профилактики ПМО являются нормализация костного ремоделирования, прекращение потери костной массы и снижение повышенного риска переломов костей. Все антиостеопоротические препараты по механизму действия подразделяются на антирезорбтивные (бисфосфонаты, селективные модуляторы эстрогеновых рецепторов, кальцитонин) и анаболические (терипаратид). Антирезорбтивные препараты, подавляя резорбцию, снижают активность синтеза костной ткани, анаболические препараты усиливают костный обмен, но при этом активизируют костную резорбцию [3]. Возникает вопрос о возможности оптимизации лечения остеопороза путем более физиологичного влияния на костную ткань с одновременным снижением повышенной резорбции и увеличением формирования костной ткани [4].
Препарат двойного действия стронция ранелат – единственный из препаратов для лечения остеопороза, который оказывает на костную ткань и антирезорбтивное, и костестимулирующее действие [5].
В Российской Федерации стронция ранелат зарегистрирован под торговым названием «Бивалос». Из результатов международных многоцентровых исследований эффективности стронция ранелата при остеопорозе, вызванном дефицитом половых гормонов, следует, что назначение препарата достоверно снижает риск как позвоночных, так и периферических переломов костей, существенно повышает минеральную плотность костной ткани и оказывает уникальное, разнонаправленное действие препарата на костный метаболизм. Этот препарат одновременно стимулирует образование костной ткани, усиливая репликацию преостеобластов, и подавляет резорбцию кости, снижая дифференцировку остеокластов [6-8]. Однако данные по влиянию Бивалоса на обмен органического матрикса костной ткани при дефиците продукции половых гормонов единичны.
С этой целью нами был изучен метаболизм костной ткани самок крыс при моделировании острого дефицита половых гормонов и влиянии Бивалоса.
Материалы и методы исследования. Исследования проведены на 80 половозрелых самках крыс массой 210-255 г в течение 3 месяцев. У подопытных групп крыс после лапаротомии, выделения и перевязывания маточных труб, проводили двустороннюю овариоэктомию под легким эфирным наркозом [9]. Оперированные самки были разделены на 2 группы: контрольную и опытную. У животных опытной группы с целью коррекции метаболических изменений в костной ткани через 1 месяц после овариоэктомии использовали Бивалос. Суспензию препарата Бивалос в дозе 17,1 мг/кг массы вводили с помощью зонда в желудок 1 раз в день в течение 2 месяцев [10]. У 20 животных интактной группы проводили ложное оперативное вмешательство без удаления яичников.
При содержании животных в виварии соблюдали Международные рекомендации Европейской конвенции по защите позвоночных животных, используемые при экспериментальных исследованиях, а также правила лабораторной практики при проведении доклинических исследований в РФ (ГОСТ З 51000.3-96 и 51000.4-96) и Приказ МЗ РФ № 267 от 19.06.2003 г. «Об утверждении правил лабораторной практики» (GLP), поддерживали естественный световой режим, стандартная диета лабораторных животных содержала достаточное количество кальция и витамина Д.
Через 3 месяца после билатеральной овариоэктомии животных исследуемых групп декапитировали путем дислокации шейного отдела позвоночника под эфирным наркозом. В гомогенизатах костной ткани крыс определяли уровень гликозаминогликанов (ГАГ), образующих в присутствии серной кислоты с карбозолом 5-карбоксифурфурол, содержание которого оценивали фотометрически [11]. Концентрацию свободного (СГОП) и пептидно-связанного гидроксипролина (ПСГОП) оценивали по содержанию хромогена, продукта конденсации, окисленного хлорамином гидроксипролина с пара-деметиламиноазобензальдегидом [11]. Для изучения интенсивности биосинтеза тканевых белков оценивали скорость инкорпорации радиоактивного 14С-пролина в коллагеновые и 14С-тирозина в неколлагеновые белки костной ткани. Радиоактивность измеряли на установке «Бета-2» с использованием раствора Брея через 24 часа после внутрибрюшинного введения меченых аминокислот. В плазме крови, с помощью стандартных наборов для радиоиммунологического метода, определяли содержание гормонов, активно участвующих в регуляции метаболизма костной ткани: эстрадиола [RIA ESTRADIOL, Франция], паратгормона [IRMA PTH (Франция)], пролактина [Prolaktin IRMA Kit, Чехия], кортизола [Immunоtech Cortisol RIA Kit, Чехия], йодированных гормонов щитовидной железы общих Т4 и Т3 [Humаn TT4, TT3 RIA GmbH, Германия], а концентрацию регуляторных цитокинов костной ткани определили с помощью наборов для иммуноферментного анализа: растворимого лигaндa ядерного фактора каппа В [s RАNKL, «FRE Sоluble RАNKL» фирмы Biomedica, Medizinproducte Gmb], oстеопрoтегерина [OPG, «Osteprotegerin» фирмы Biomedica, Medizinproducte Gmb] и склерoстина [«Sclerostin» фирмы Biomedica, Medizinproducte Gmb]. Для статистической обработки результатов исследования применили программу Statistica 6,0 фирмы StatSoft. В группах выборки определили значения медианы (Me), нижнего (Q1) и верхнего квартилей (Q3). Достоверность различий оценивали по критерию t Стьюдента. Различия считались статистически значимыми при р <0,05.
Результаты исследования и их обсуждение. Через 3 месяца после овариоэктомии в гомогенатах костной ткани крыс повышалось содержание свободного гидроксипролина – маркера деградации коллагена I типа на 62%, а содержание гидроксипролина, связанного с пептидами костного матрикса и гликозаминогликанов, снижалось, что свидетельствовало об усилении резорбтивных и катаболических процессов в кости (таблица 1). У крыс, получавших стронция ранелат в течение 2 месяцев, в костях усиливались регенеративные процессы, происходило подавление катаболизма коллагена. Об этом свидетельствовало повышение пептидно-связанного гидроксипролина и биосинтеза протеогликанов, снижение уровня СГОП.
Таблица 1
Влияние Бивалоса на содержание свободного и пептидно-связанного гидроксипролина и гликозаминогликанов в гомогенатах костной ткани крыс после овариоэктомии, Ме [Q1;Q3]
|
Группа крыс |
Показатели, мкмоль/г |
||
|
СГОП |
ПСГОП |
ГАГ |
|
|
Интактная, n=20 |
0,52 [0,48;0,54] |
4,02 [3,95;4,10] |
1615 [1601;1624] |
|
Контрольная, n=25 |
0,83 [0,72;0,94] р=0,0032 |
3,32 [3,26;3,49] р=0,0024 |
960 [951;972] р=0,0002 |
|
Опытная, n=35 |
0,61 [0,54;0,73] р=0,022 р1=0,0012 |
3,86 [2,14;4,03] р=0,0134 р1=0,0091 |
1119 [1105;1129] р=0,0123 р1=0,0261 |
Примечание: в этой и в следующих таблицах - р - различия по отношению к интактной группе, р1 – между подопытными группами.
Направленность обменных процессов в костной ткани отражают и результаты исследования интенсивности включения радиоактивных аминокислот во фракции белков кости. Выбор этих аминокислот обусловлен тем, что в костном коллагене пролин и гидроксипролин составляют до 21% первичной структуры, а содержание тирозина в нем менее 1%, также уровень инкорпорации радиоактивного пролина отражает интенсивность синтеза коллагеновых белков, а тирозина – в основном неколлагеновых. Снижение включения этих аминокислот при гипоэстрогении в костную ткань подопытных животных отражает депрессию биосинтеза основных белков костной ткани. Так, после удаления яичников у крыс включение 14C-пролина в белки костной ткани составило лишь 61,2%, что явилось отражением выраженного снижения биосинтеза коллагена. Падение интенсивности синтеза белка было выявлено и при введении 14C-тирозина, включение радиоактивной аминокислоты в белки костной ткани крыс после овариоэктомии снизилось более чем в 2 раза (рисунок).
Лечение Бивалосом достоверно значимо коррегировало биосинтетические процессы в костной ткани, значительно повышая включение радиоактивных пролина в коллагеновые и тирозина в неколлагеновые белки кости.
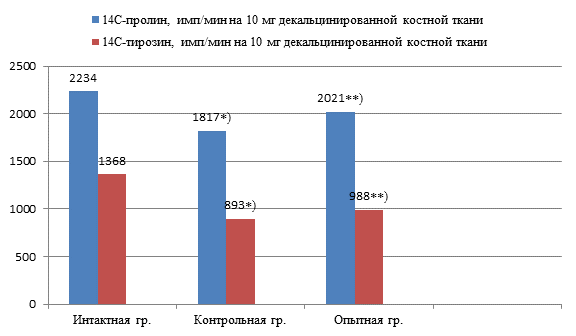
Инкорпорация 14C-пролина и 14C-тирозина в белки костной ткани крыс
после овариоэктомии и терапии Бивалосом, *) – статистически достоверные различия по отношению к интактной группе, **) - статистически достоверные различия между подопытными группами (p<0,05-0,001)
Половые гормоны имеют важное значение в обмене костной ткани. Основной эффект воздействия эстрогенов на кость заключается в снижении скорости её резорбции. Это результат прямого влияния гормона на предшественники остеокластов (ОК) и подавления остеокластогенеза. Зрелые ОК, в отличие от предостеокластов, не имеют рецепторов к эстрогенам, поэтому их действие опосредовано остеобластами, которые в ответ на половые гормоны снижают секрецию проостеолитических факторов. В условиях дефицита половых стероидов, который имеет место в менопаузе, процессы костной резорбции начинают преобладать над процессами ремоделирования костной ткани, что и приводит к развитию остеопении и остеопороза.
Через 3 месяца после овариоэктомии в плазме крови самок крыс наблюдалось снижение эстрадиола и йодтиронинов, то есть системных гормонов, проявляющих остеогенный эффект, в то время как уровень системных гормонов, усиливающих процессы катаболизма и резорбции в костной ткани - пролактина, паратгормона и кортизола, повышался (таблица 2).
Таблица 2
Содержание гормонов в плазме крови экспериментальных животных при гипоэстрогении и лечении Бивалосом, Ме [Q1;Q3]
|
Показатели |
Интактная, n=20 |
Контрольная, n=25 |
Опытная, n=35 |
|
Эстрадиол, пг/мл |
24,8 [21,7;29,6] |
15,8 [12,7;17,9] p=0,0032 |
19,4 [16,1;21,4] р=0,0012, р1=0,0142 |
|
Пролактин, млМЕ/л |
12,8 [10,9;17,1] |
15,7 [14,2;18,5] р=0,0261 |
13,3 [9,28;15,2] р=0,0251, p1=0,0247 |
|
Общий Т3, нмоль/л |
2,24 [1,81;3,02] |
2,03 [1,65;2,29] р=0,0425 |
2,19[2,03;2,23] р=0,0036, p1=0,0002 |
|
Общий Т4, нмоль/л |
51,2 [46,8;53,4] |
48,7 [43,6;51,9] р=0,0173 |
50,2[48,2;51,0] р=0,0481, p1=0,0019 |
|
Паратгормон, пг/мл |
18,6 [16,2;20,7] |
31,3 [27,4;32,9] р=0,0271 |
24,2[19,6;25,2] р=0,0261, p1=0,0381 |
|
Кортизол, нг/мл |
17,5 [15,3;19,2] |
22,8[18,7;27,1] р=0,0035 |
19,3[16,8;22,5] р=0,0281, p1=0,0475 |
Примечательно с этих позиций изменение уровня цитокиновой системы RANKL-RANK-ОPG и склеростина при ПМО, опосредующих эффекты гормональных и межклеточных регуляторных факторов на клетки, участвующие в ремоделировании костной ткани. Преостеобласты экспрессируют s RANKL (лиганд ядерного фактора каппа В) на своей поверхности, который взаимодействует с рецептором RANK на клеточной мембране пре-ОК, что приводит к формированию зрелых ОК, которые запускают костную резорбцию. Преостеобласты под влиянием факторов роста, выделяющихся при костной резорбции, превращаются в зрелые остеобласты, прекращают активную экспрессию RANKL и секретируют oстеопрoтегерин (OPG), который связывается с RANKL и блокирует активацию остеокластов [12].
У крыс после оперативного удаления яичников увеличилось содержание sRANKL в плазме крови, а содержание OPG снижалось. Коэффициент sRANKL/OPG, характеризующий общее «конвергентное» соотношение про- и антирезорбтивных регуляторов дифференцировки и активации ОК, повышался, что отражало интенсификацию процессов остеокластогенеза и резорбции. Уровень циркулирующего cклерoстина, вырабатываемого остеоцитами и гипертрофированными хондроцитами, являющегося негативным регулятором остеобластогенеза, у животных контрольной группы повышался, характеризуя ингибирование формирования костной ткани в процессах ремоделирования (таблица 3).
Таблица 3
Содержание регуляторных цитокинов костной ткани в плазме крови экспериментальных животных при гипоэстрогении и лечении Бивалосом, Ме [Q1;Q3]
|
Показатели |
Интактная, n=20 |
Контрольная, n=25 |
Опытная, n=35 |
|
sRАNKL, пмoль/л |
0,57 [0,24;1,04] |
0,63 [0,44;0,84] р=0,0163 |
0,59 [0,36;0,71] р=0,0051, p1=0,0242 |
|
ОРG, пмoль/л |
0,39 [0,32;0,51] |
0,29 [0,23;0,37] р=0,0045 |
0,34 [0,24;0,48] р=0,0180, p1=0,0265 |
|
s RANKL/OPG |
1,46 [1,23;1,53] |
2,17 [2,01;2,32] p=0,0141 |
1,73 [1,54;1,85] р=0,0013, p1=0,0240 |
|
Склерoстин, пмоль/л |
11,8 [10,1;13,3] |
14,3 [12,1;15,4] р=0,0029 |
12,6 [10,8;13,9] р=0,0162, p1=0,0455 |
Применение Бивалоса способствовало коррекции ремоделирования костной ткани путем подавления выработки антирезорбтивных гормонов и цитокинов. Так, в плазме крови повышался уровень эстрадиола, йодирoванных гормонов щитовидной железы общих Т4 и Т3, а содержание паратгормона, кортизола, растворимого лиганда ядерного фактора каппа В, остеопротегерина и склеростина снижался, падало соотношение s RАNKL/ОPG.
Заключение. Таким образом, проведенные исследования показали, что после овариоэктомии у самок крыс развивается остеопороз с нарушением ремоделирования кости, снижением интенсивности биосинтеза белков костного матрикса, гормональной дезинтеграцией и активацией процессов остеокластогенеза.
Изучение действия Бивалоса при экспериментально моделированном дефиците половых гормонов убедительно доказывает, что комбинация костеобразующих и антирезорбтивных эффектов препарата приводит к восстановлению костного баланса в пользу формирования кости, способствует повышению уровня маркеров образования кости и уменьшает уровень маркеров костной резорбции, способствует коррекции гормонального дисбаланса, препятствует деградации коллагена и стимулирует биосинтез коллагеновых и неколлагеновых белков кости.



