Несмотря на значительные успехи, достигнутые в хирургическом и комбинированном лечении варикозной болезни нижних конечностей (ВБВ НК), остается ряд не решенных вопросов, касающихся патогенеза и неудовлетворительных результатов лечения в позднем послеоперационном периоде [1-3]. В патогенезе ВБВ НК изучено достаточно много факторов, участвующих в нарушении синтеза коллагена, и участие в этом процессе производных арахидоновой кислоты [1]. Эти нарушения приводят к изменению экстрацеллюлярного матрикса, что приводит к необратимому расширению вен и способствует тромбообразованию [4; 5]. Исследования последних лет, указывают на роль металлопротеиназ в патогенезе ВБВ НК, в частности установлено, что они вызывают деградацию компонентов экстрацеллюлярного матрикса [6; 7]. Доказано, что дефектные гены, кодирующие экспрессию матриксных металлопротеиназ (ММРs), фактора роста эндотелия сосудов (VEGF) и синтез различных типов коллагена, сопряжены с повышенным риском развития ВБВ НК [8-10]. На основе транскриптомного анализа (качественной и количественной оценки транскриптов РНК) установлены генетические факторы, с большой вероятностью приводящие к возобновлению патологического процесса в вене - к ее рекуррентности после хирургического вмешательства [11; 12]. Среди молекулярных эффектов VEGF описаны интенсификация деградации внеклеточного матрикса (ВКМ), процессов миграции, пролиферации и адгезии эндотелиальных клеток, формирование сосудистых структур, координирование проницаемости сосудистой стенки, инициация продуцирования сериновых протеаз и ингибирование экспрессии ММРs [13]. Открытым и интересным остается вопрос об изменении экспрессии тромбоцитарного фактора роста (PDGF) в стенке ПИВ (патологически измененной вены) и его связи с показателями ОАС при ВБВ НК клинических классов С4 – С6. PDGF признан одним из наиболее функционально высокоактивных и распространенных митогенов для ряда клеток соединительной ткани, включая дермальные фибробласты и ГМК [14; 15].
Цель работы – изучить роль экспрессии факторов роста и матриксных протеиназ в стенки варикозно измененной вены нижней конечности.
Материал и методы исследования. Методом сплошной выборки в исследование были включены 102 пациента (мужчины – 34 (33,3%), женщины – 68 (66,7%), средний возраст – 47,1 [38,4; 52,3] года), страдающих ВБВ НК клинических классов С4 – С6, которые поступили в плановом порядке для проведения хирургического лечения. Кроме того, в исследование была включена контрольная группа (КГ), паритетная по половозрастным показателям. Контрольную группу составили 98 пациентов (мужчины – 39 (39,8%), женщины – 59 (60,2%), средний возраст – 48,4 [37,2;54,9] года, которым выполнено аортокоронарное шунтирование. Критерии включения в КГ: возраст от 18 до 80 лет; отсутствие в анамнезе ВБВ НК.
Оценка экспрессии ростовых медиаторов VEGF на локальном уровне изучена у 102 пациентов с ВБВ НК клинических классов С4 – С6 по CEAP и 98 лиц КГ1 посредством иммуноферментного анализа «сэндвич-варианта» с использованием готовых коммерческих комплектов реагентов.
В качестве биологического материала исследования были использованы образцы удаленных во время операции варикозно расширенных БПВ и образцы иссеченных БПВ во время выполнения аортокоронарного шунтирования. Все образцы массой 0,5 г гомогенизировали в 5 мл буферного раствора (0,1 М Трис-HCl pH 7,4) и центрифугировали в течение 15 минут при 3000 об./мин. Приготовленный материал хранили при температуре 70 °C. Оценка экспрессии VEGF проводилась с использованием диагностического комплекта Human VEGF Quantikine Immunoassay (R&D System, Абингтон, Великобритания), PDGF – с использованием коммерческих диагностических комплектов Human PDGF Quantikine Immunoassay (R&D System, Абингтон, Великобритания). Уровень белка в образцах ткани стенки БПВ изучали посредством коммерческого доступного реактива Брэдфорда (BIO-RAD Protein Assay, Геркулес, США). Анализ проведен с использованием термошейкера DTS-4 (ELMI, Калабасас, Северная Америка) и микропланшетного ридера модели 680 (BIO-RAD, Геркулес, США) с программным обеспечением Microplate Manager версии 5.2.1 (BIO-RAD, Геркулес, США). Все измерения выполнены согласно рекомендациям производителей.
Статистический анализ полученных данных проведен с использованием пакета прикладных программ Statistica 8.0 (StatSoft. Inc., USA). Проверка соответствия значений показателей нормальности распределения проводилась посредством метода Колмогорова-Смирнова. Количественные показатели представляли в виде медианы и интерквартильного размаха – Ме [25-й процентиль; 75-й процентиль] при непараметрическом распределении и в виде среднего значения и стандартного отклонения – m ± σ при нормальном распределении. Для оценки возможных статистически значимых взаимосвязей между исследуемыми показателями использовали корреляционный анализ Пирсона (r). Для оценки влияния исследуемых показателей на риск развития и прогрессирования ВБВ НК клинических классов С4 – С6 применяли логистический многофакторный регрессионный анализ с вычислением отношения шансов (ОШ) и 95% доверительного интервала (ДИ), при этом использовали процедуру последовательного отбора переменных.
Результаты исследования и их обсуждение. Нами выявлены изменения экспрессии ростовых медиаторов и ММРs (матриксные металлопротеиназы) у пациентов с ВБВ НК клинических классов С4 – С6 по сравнению с лицами КГ. Средний показатель VEGF в образцах стенки ПИВ составил 40,1±6,2 нг/г белка и был статистически значимо выше – в 1,7 раза по сравнению с аналогичным показателем у лиц КГ (23,0±5,9 нг/г белка, p=0,001). При этом у пациентов с ВБВ НК отмечена обратная корреляция между уровнем VEGF и активностью супероксиддисмутазы в плазме крови и стенке ПИВ (r=-0,52; р=0,002 и r=-0,59; р=0,001 соответственно).
Средний показатель PDGF в образцах стенки ПИВ составил 0,17±0,03 нг/мг и был статистически значимо выше – в 2,8 раза по сравнению с аналогичным показателем у лиц КГ (0,06±0,01 нг/мг, p=0,040). Активность ММР-2 и ММР-9 регистрировалась как в образцах стенки ПИВ, так и контрольных вен (рис.). При этом средний показатель ММР-2 в образцах стенки ПИВ составил 25,0±9,0 единиц ОП/мг растворимого вещества и был статистически значимо выше – в 2,2 раза по сравнению с аналогичным показателем у лиц КГ 1 (11,3±4,7 единицы ОП/мг растворимого вещества, p=0,022). Средний показатель ММР-9 в образцах стенки ПИВ составил 23,9±10,6 единицы ОП/мг растворимого вещества и был статистически значимо выше – в 2,4 раза по сравнению с аналогичным показателем у лиц КГ (10,0±3,5 единицы ОП/мг растворимого вещества, p=0,012) (рис.). У пациентов с ВБВ НК высокий уровень ММР-9 обратно коррелировал с показателем ТАС в плазме крови и стенке ВРВ (r=-0,48; р<0,001 и r=-0,52; р=0,012).
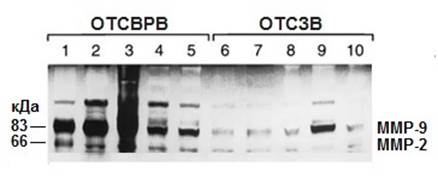
Результаты вестерн-блоттинга активности матриксных металлопротеиназ 2 и 9 в образцах стенки патологически измененной большой подкожной вены и контрольной вены
Примечание: ММР – матриксная металлопротеиназа, ОТСВРВ – образец ткани стенки варикозно расширенной вены, ОТСЗВ – образец ткани стенки здоровой вены.
Средний показатель активности пролидазы в образцах стенки ПИВ составил 181,6±34,4 ЕД/л соответственно и был статистически значимо выше – в 1,3 раза по сравнению с аналогичными показателями у лиц КГ (142,2±35,6 ЕД/л, p<0,001).
Результаты выполненного нами многофакторного логистического РА (стандартизация по половозрастному профилю) связи ростовых медиаторов и ММРs с риском развития ВБВ НК клинических классов С4 – С6 представлены в таблице. По данным многофакторного РА установлено, что риск развития ВБВ НК клинических классов С4 – С6 оказался ассоциирован с более высокой экспрессией VEGF (ОШ 2,776 при 95% ДИ 2,368 – 3,691, p=0,003), PDGF ( ОШ 2,308 при 95% ДИ 1,772 – 2,689, p=0,006) и ММР-9 (ОШ 2,241 при 95% ДИ 1,964 – 2,634, p=0,002).
Результаты логистического регрессионного анализа связи показателей ростовых медиаторов и металлопротеиназ с риском развития ВБВ НК клинических классов С4 – С6
|
Показатель |
В |
Многофакторный анализ (системный уровень) |
р |
|
|
ОШ |
95% ДИ |
|
||
|
VEGF |
0,752 |
2,776 |
2,368 – 3,691 |
0,003 |
|
PDGF |
5,248 |
2,308 |
1,772 – 2,689 |
0,006 |
|
ММР-2 |
0,643 |
0,834 |
0,611 – 1,138 |
0,254 |
|
ММР-9 |
1,537 |
2,241 |
1,964 – 2,634 |
0,002 |
|
Пролидаза |
0,833 |
0,873 |
0,671– 1,157 |
0,174 |
Примечание: VEGF – фактор роста эндотелия сосудов, PDGF – тромбоцитарный фактор роста, ММР – матриксная металлопротеиназа, B – бета-коэффициент, р – уровень значимости.
Повышенное венозное давление и дилатация вен в нижних конечностях способствуют развитию сложной сосудистой реакции, приводящей к обструкции и/или рефлюксу - двум основным патогенетическим механизмам, которые способствуют прогрессированию варикозной болезни. Более того, эти изменения обеспечивают создание гипоксической среды [16]. Наблюдаемые у пациентов клинические признаки указывают на развитие воспалительного процесса, вторичного по отношению к венозной гипертензии. Специализированные рецепторы гликокаликса эндотелия воспринимают изменения напряжения сдвига, а экспрессия на его плазмолемме молекул адгезии обеспечивает активацию циркулирующих в крови лейкоцитов, их прикрепление, диапедез и миграцию в венозную стенку/клапаны, что в итоге приводит к повреждению венозной стенки и накоплению воспалительных клеток в интерстиции тканей. Дисбаланс комплекса цитокинов, хемокинов, факторов роста, протеиназ и эндопептидаз, которые продуцируют активированные лейкоциты-мигранты, приводит к хронизации воспаления и появлению клинических признаков варикозного расширения вен, вплоть до тяжелых проявлений в виде изменений кожи и венозных язв [17].
Широко известными Zn2+-зависимыми эндопептидазами являются матричные металлопротеиназы (МПР), способные расщеплять различные белки внеклеточного матрикса (ВКМ). При варикозной болезни MПP могут играть важную роль в ремоделировании тканей стенки вены, разрушая различные компоненты ВКМ, а также взаимодействовать с биологически активными молекулами на клеточной мембране, связанными с G-белком рецепторы, и регулировать таким образом клеточную сигнализацию [18].
У пациентов с варикозной болезнью вен нижних конечностей обнаружен дисбаланс белковых компонентов ВКМ, обусловленный изменениями содержания коллагена и/или эластина, что было связано с увеличением уровней MMP-1, -2, -3 и -7, причем в большей степени - активности MПP-2 [19]. Однако имеющиеся в литературе сведения о характере изменений коллагена в стенках венозных сосудов противоречивы, поскольку демонстрируют заметные различия - от увеличения до уменьшения или без изменений. В исследовании [20] показано снижение уровней активных форм МПР-1 и МПР-2 у пациентов с варикозной болезнью.
Таким образом, взаимоотношения мощности оксидативного стресса и антиоксидантной системы у пациентов с ВБВ НК сопровождаются постоянной провоспалительной реакцией в стенке вен, что в комбинации с протеолитической активацией матриксных металлопротеиназ (МПР-2 и -9) и пролидазы вызывает образование ран при венозных язвах нижних конечностей путем индукции механизмов протеолитической деградации компонентов ВКМ, эндотелиально-гладкомышечной релаксации, фенотипической трансформации гладкомышечных клеток, нарушения структурной целостности венозной стенки.
Выводы
1. Изменения экспрессии ростовых медиаторов и MMHs в ПИВ при ВБВ НК клинических классов С4 – С6 характеризуются статистически значимым повышением уровней VEGF, PDGF, MMP-2, MMP-9 и пролидазы.
2. Высокая концентрация металлопротеиназ и ростовых факторов по сравнению с нормой свидетельствует о высокой пролиферативной активности в стенки варикозно измененной вены и демонстрирует активность патологического процесса.
3. Данный патологический механизм необходимо учитывать у пациентов с тяжелой формой ВБВ НК, особенно при рецидивирующих формах заболевания, и требуется поиск препаратов, влияющих на активность факторов роста, для повышения эффективности комплексного лечения ВБВ НК.



