Цереброваскулярные заболевания на сегодняшний день, пожалуй, занимают лидирующие места среди причин, приводящих к стойкой нетрудоспособности и инвалидизации, а как следствие – и к смерти. Доказанным фактом является то, что гипергликемия усугубляет неврологический дефицит в условиях ишемии головного мозга, о чем свидетельствуют многочисленные клинические наблюдения (у больных сахарным диабетом, перенесших инсульт, исходы значительно хуже, чем у аналогичных пациентов, не имеющих диабета) [1]. В условиях стационара гипергликемия, возникшая в результате экзогенного введения глюкозы, потенциально предотвратима, более сложная ситуация возникает при эндогенном повышении концентрации глюкозы в крови у пациентов с риском ишемического повреждения головного мозга. В современной клинической практике существенно недооцениваются неблагоприятные эффекты гипергликемии в условиях ишемии. Обычно считается, что гипергликемия от легкой до умеренной степени практически безвредна. Теоретически, инсулин можно использовать для поддержания концентрации глюкозы в крови в диапазоне от нормального до нижнего предела нормы и таким способом обеспечить защиту от гипергликемически опосредованных неврологических нарушений.
На сегодняшний день по-прежнему не до конца ясно, как влияет превентивное введение инсулина на неврологический дефицит в условиях церебральной ишемии, это и обусловило проведение данного исследования.
Цель исследования – оценить влияние на неврологический дефицит превентивного введения инсулина на модели церебральной ишемии у крыс в эксперименте.
Материалы и методы исследования
Эксперимент проводился на 64 животных (нелинейных белых крысах обоего пола массой 210–360 г). Все манипуляции с животными проводились в соответствии с Руководством по содержанию и использованию лабораторных животных [2]. Животным выполнено анестезиологическое пособие (наркоз), включающее интраперитонеальное введение (и/п) препаратов: «Ксилазин» (из расчета 0,5 мл/кг массы тела) и «Золетил 100» (из расчета 8 мг/кг массы тела). Выполнялась респираторная поддержка. На аппаратном комплексе «BIOPAC» в соответствии со стандартными методиками производился непрерывный мониторинг температуры тела, ЭЭГ, среднего артериального давления. Концентрацию глюкозы в крови определяли с помощью дополнительного модуля-анализатора Super GL сompact (Dr. Muller, Германия) по стандартной методике [3, 4]. Затем проводили взятие крови из хвостовой вены в объеме 0,3 мл для определения уровня гликемии перед окклюзией средней мозговой артерии (СМА). Животные были разделены на 4 группы:
1-я группа (n=16) – внутрибрюшинное введение (в/б) 1 мл 0,9%-ного раствора натрия хлорида за 60 минут до окклюзии СМА.
2-я группа (n=16) – внутрибрюшинное введение 0,4 ЕД (1,7 ЕД/кг массы тела) инсулина короткого действия («АктрапидНМ») за 60 минут до окклюзии СМА.
3-я группа (n=16) – внутрибрюшинное введение 0,5 ЕД (2,1 ЕД/кг массы тела) инсулина короткого действия («АктрапидНМ») за 60 минут до окклюзии СМА.
4-ая группа (n=16) – внутрибрюшинное введение 0,6 ЕД (2,5 ЕД/кг массы тела) инсулина короткого действия («АктрапидНМ») за 60 минут до окклюзии СМА.
Затем всем животным выполнялась 45-минутная окклюзия СМА по методике J. Koizumi (1986) [5] с последующей реперфузией. На следующем этапе оценивали неврологический дефицит, подвергая каждую крысу через 1, 4, 18, 24 часа после моделирования окклюзии СМА тестам «Бедерсон-тест» и «Открытое поле» [6, с. 68]. Общую выживаемость оценивали через 26 часов после окклюзии. Для статистической обработки были применены t-критерий Стьюдента и критерий Манна–Уитни. Результаты представлены следующим образом: М ± m (М – среднее, m – ошибка среднего). Данные принимались за статистически значимые при р<0,05.
Результаты исследования и их обсуждение
До начала эксперимента контрольный уровень среднего артериального давления во всех группах животных равен 112,24±10,68 мм рт. ст., статистически значимых различий между группами по данному показателю не выявлено. В группе № 1 зафиксировано увеличение концентрации глюкозы в крови непосредственно перед окклюзией СМА, предположительно это обусловлено дополнительным стрессом, связанным с выполнением анестезиологического пособия и операции интактным животным (табл. 1). У крыс в группе №2, получивших 0,4 ЕД инсулина короткого действия, концентрация глюкозы в крови была статистически значимо ниже – в 1,46 раза (р<0,05) – в сравнении с крысами из группы №1 на протяжении 4 часов с момента окклюзии. У одной крысы (6%) в группе животных №1 в период реперфузии отмечено прогрессирующее снижение артериального давления. Несмотря на проводимую респираторную поддержку, эта крыса умерла через 90 минут с момента окклюзии СМА.
Таблица 1
Концентрация глюкозы в крови и выживаемость у крыс на фоне церебральной ишемии
|
Группы животных
|
n |
Уровень глюкозы (ммоль/л) |
Выживаемость,% |
|||
|
Исходный уровень глюкозы крови до эксперимента |
Уровень глюкозы перед окклюзией СМА |
Уровень глюкозы через 1 час после окклюзии СМА |
Уровень глюкозы через 4 часа после окклюзии СМА |
|||
|
Группа № 1 (в/б 1 мл 0,9%-ного р-ра NACl за 60 минут до окклюзии СМА) |
16 |
8,06±0,8 |
11,21±0,41 |
8,38±0,57 |
8,69±0,57 |
39% |
|
Группа № 2 (в/б 0,4 ЕД (1,7 ЕД/кг массы тела) инсулина короткого действия за 60 минут до окклюзии СМА |
16 |
7,79±0,28 |
4,63±0,45* |
3,40±0,32* |
5,01±0,49* |
94% |
|
Группа № 3 (в/б 0,5 ЕД (2,1 ЕД/кг массы тела) инсулина короткого действия за 60 минут до окклюзии СМА |
16 |
7,89±0,41 |
3,34±0,34* |
2,47±0,35 |
5,28±1,74 |
75% |
|
Группа № 4 (в/б 0,6 ЕД (2,5 ЕД/кг массы тела) инсулина короткого действия за 60 минут до окклюзии СМА |
16 |
7,88±0,61 |
2,78±0,33* |
2,14±0,24* |
4,84±0,43* |
0% |
Примечание: * – статистическая значимость отличия по отношению к показателям группы № 1 при р<0,05.
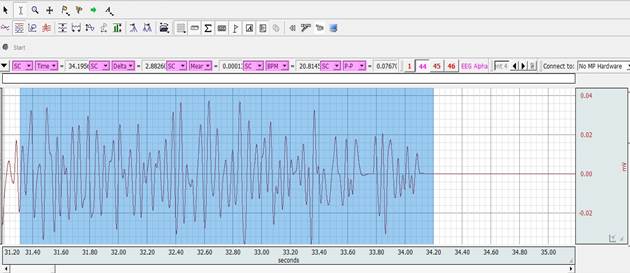
Время с момента окклюзии до появления изоэлектрической ЭЭГ колебалось от 20 до 40 секунд, и ЭЭГ оставалась изоэлектрической в течение всего периода окклюзии СМА (рис. 1).
Рис. 1. Пример записи ЭЭГ после окклюзии СМА
У всех 64 животных с момента начала ишемии головного мозга зафиксировано полное расширение зрачка, которое сохранялось на протяжении всего периода окклюзии СМА. Размер зрачка вернулся к норме в течение 1 минуты после снятия лигатуры; на ЭЭГ в период реперфузии не отмечалось никаких патологических «ЭЭГ паттернов». Общая выживаемость через 26 часов после окклюзии была статистически значимо выше у крыс в группе № 2 в сравнении с группой № 1 – в 1,41 раза (р<0,05). В группе животных № 1 количество умерших особей составило 61% (n=10, с учетом включения крысы, умершей спустя 90 минут с момента окклюзии СМА). Пять крыс из группы животных № 1, несмотря на проведение респираторной поддержки, умерли спустя 120 минут с момента окклюзии; еще 5 крыс из этой же группы скончались спустя 20 часов с момента окклюзии, смерть была обусловлена выраженным судорожным синдромом. Среди животных в группе № 2 у 12 особей из 16 отмечен судорожный синдром в периоде между 17 и 26 часами с момента окклюзии СМА, но ни одна из этих крыс не умерла. Судорожная активность состояла из пароксизмальных приступов генерализованных тонико-клонических судорог с выраженными беспокойными движениями конечностей. Стоит учесть и тот факт, что введение высоких доз инсулина может привести к чрезмерно низким концентрациям глюкозы в плазме, что, в свою очередь способно негативно сказаться на исходе. При анализе общей выживаемости в группах животных № 2, № 3, № 4 максимальная выживаемость отмечена в группе животных, получавших инсулин короткого действия в дозировке 1,7 ЕД/кг массы тела = 0,4 ЕД (группа № 2), затем она уменьшилась по мере увеличения дозы инсулина. Важным наблюдением является то, что степень гипогликемии во многом обусловливает исход. При увеличении дозы инсулина до 2,1 и 2,5 ЕД/кг массы тела выживаемость снижалась.
Наиболее выраженный неврологический дефицит был отмечен у животных в группе № 1. У животных в 1-й группе неврологический дефицит был обусловлен нарастанием расстройств преимущественно в моторной и рефлекторной сферах, а также расстройств чувствительности (табл. 2).
Таблица 2
Поведенческие показатели у крыс в тесте «Открытое поле» и оценка неврологического дефицита по «Бедерсон-тесту»
|
Показатель |
Спустя 24 часа с момента окклюзии СМА |
|||
|
Группа № 1 (в/б 1 мл 0,9%-ного р-ра NACl за 60 минут до окклюзии СМА) |
Группа № 2 (в/б 0,4 ЕД (1,7 ЕД/кг массы тела) инсулина короткого действия за 60 минут до окклюзии СМА |
Группа № 3 (в/б 0,5 ЕД (2,1 ЕД/кг массы тела) инсулина короткого действия за 60 минут до окклюзии СМА |
Группа № 4 (в/б 0,6 ЕД (2,5 ЕД/кг массы тела) инсулина короткого действия за 60 минут до окклюзии СМА |
|
|
Тест «Открытое поле» |
|
|
|
|
|
Время в центре, с |
1,1±0,3 |
3,02±0,2 |
2,99±0,4 |
3,01±0,4 |
|
Число пересеченных квадратов, шт. |
5,4±0,6 |
11,3±1,65* |
11,3±1,7 |
10,9±1,98 |
|
Время груминга, с |
2,1±0,87 |
3,4±1,4 |
2,98±0,97 |
3,02±1,16 |
|
Число вертикальных стоек, шт. |
1,9±0,9 |
3,87±0,5 |
3,99±0,48 |
3,77±0,41 |
|
Число заглядываний, шт. |
2,1±0,5 |
3,7±0,4* |
4,21±0,6 |
3,7±0,5 |
|
Время обнюхивания, с |
166,42±12,82 |
146,22±5,92* |
158,12±6,62 |
150,12±7,12 |
|
Число дефекаций, шт. |
2,9±0,6 |
1,6±0,7 |
1,73±0,7 |
1,6±0,7 |
|
Число уринаций, шт. |
0,5±0,2 |
0,4±0,6 |
0,4±0,45 |
0,6±0,31
|
|
Бедерсон-тест (баллы) |
|
|||
|
|
2,6±0,47 |
2,45±0,15* |
2,87±0,4 |
2,71±0,51 |
Примечание: * – статистическая значимость отличия по отношению к показателям группы № 1 при р<0,05.
Число пересеченных квадратов животными в группе № 2 была статистически значимо выше (на 91,5%) в сравнении с группой животных № 1 (р<0,05). При применении Бедерсон-теста наименее выраженные неврологические нарушения отмечены в группе животных № 2, так, показатели в этой группе были статистически значимо ниже (на 5,7%) в сравнении с группой № 1 (р<0,05). Тотальная церебральная ишемия, вызванная окклюзией СМА, носила временный характер, но, тем не менее, сопровождалась последующим стойким неврологическим дефицитом, который приводит к высокой смертности.
Гипергликемия является одним из факторов, который, как известно, усугубляет повреждение, но точный механизм повреждения, связанный с глюкозой, до конца не изучен. В результате расщепления основного субстрата-глюкозы в условиях гликолиза на фоне интенсивного метаболизма головного мозга происходит накопление лактата в тканях, что, пожалуй, сегодня рассматривается как ключевое метаболическое событие, отягчающее ишемически обусловленный неврологический дефицит. Теоретически гипогликемия легкой степени, вызванная инсулином, может уменьшить доступность глюкозы в качестве субстрата и, следовательно, уменьшить образование лактата, который будет накапливаться в анаэробных условиях ишемии. Несмотря на то что влияние инсулина на нервную ткань остается спорным (бытует точка зрения, что в условиях тотальной ишемии можно ожидать побочных эффектов от введения инсулина из-за локального накопления лактата в нервной ткани на фоне интенсивного расщепления глюкозы), в нашем эксперименте на модели церебральной ишемии инсулин в дозе 1,7 ЕД/кг массы тела оказывает нейропротективное воздействие. У крыс из группы № 2, которым вводили 0,4 ЕД инсулина (1,7 ЕД/кг массы тела), неврологический дефицит был менее выраженным в сравнении с крысами из группы № 1, получавшими раствор натрия хлорида 0,9%-ный 1 мл и/п (табл. 3).
Таблица 3
Сравнение компонентов оценки неврологического дефицита в модели церебральной ишемии у крыс
|
Компоненты
|
Через 1 час с момента окклюзии СМА |
Через 4 часа с момента окклюзии СМА |
Через 18 часов с момента окклюзии СМА |
Через 24 часа с момента окклюзии СМА |
||||
|
Группа № 1 (в/б 1 мл 0,9%-ного р-ра NACl за 60 минут до окклюзии СМА) |
Группа № 2 (в/б 0,4 ЕД (1,7 ЕД/кг массы тела инсулина короткого действия за 60 минут до окклюзии СМА) |
Группа № 1 (в/б 1 мл 0,9%-ного р-ра NACl за 60 минут до окклюзии СМА) |
Группа № 2 (в/б 0,4 ЕД (1,7 ЕД/кг массы тела) инсулина короткого действия за 60 минут до окклюзии |
Группа № 1 (в/б 1 мл 0,9%-ного р-ра NACl за 60 минут до окклюзии СМА) |
Группа № 2 (в/б 0,4 ЕД (1,7 ЕД/кг |
Группа № 1 (в/б 1 мл 0,9%-ного р-ра NACl за 60 минут до окклюзии СМА) |
Группа № 2 (в/б 0,4 ЕД (1,7 ЕД/кг |
|
|
Сознание |
7,7±0,51 |
6,0±0,48* |
6,0±0,71 |
2,4±0,45# |
4,0 ±0,97 |
0,4±0,21# |
4,2±1,2 |
0,1±0,13#
|
|
Двигательная функция |
14,7±0,21 |
14,0±0,41 |
11,2±0,9 |
7,6±0,87* |
10,3±0,99 |
4,9±0,41# |
9,7±1,1 |
3,6±0,42# |
|
Функция черепных нервов |
2,4±0,97 |
0,6±0,51 |
1,8 ±0,8 |
0±0* |
1,5 ± 0,81 |
0±0* |
1,8±0,91 |
0±0* |
|
Функция позвоночных нервов |
2,9±0,37 |
1,8±0,25* |
2,2±0,35 |
1,4±0,27
|
1,9 ± 0,39 |
0,5 ±0,24* |
2,3±0,53 |
0,4±0,21# |
|
Функция дыхания |
2,6±1,1 |
0,1±0,13* |
0,2±0,18 |
0±0 |
0,5 ±0,28 |
0±0* |
0,7±0,33 |
0±0* |
Примечание: * – статистическая значимость отличия по отношению к показателям группы № 1 при р<0,05.
# – статистическая значимость отличия по отношению к показателям группы № 1 при р<0,001.
Через 1 час после окклюзии в группе № 2, получавшей инсулин, по сравнению с группой, получавшей физиологический раствор натрия хлорида, количественные аспекты оценки нарушения сознания были менее выражены (табл. 3). Можно предположить, что отсутствие различий в двигательной функции, вероятнее всего, связано со снижением мотивации, поскольку данная закономерность наблюдалась у всех крыс, даже у которых не был отмечен визуально патологический уровень сознания, также снижение реакций может быть связано с остаточными эффектами компонентов наркоза.
Заключение
В нашем исследовании мы постарались показать, что умеренная гипогликемия в условиях церебральной ишемии оказывает нейропротективное действие. В настоящее время известно несколько механизмов, посредством которых инсулин может оказывать нейропротекцию. Инсулин снижает гликогенолиз и глюконеогенез в печени, а также снижает концентрацию глюкозы в плазме за счет усиления поглощения и усвоения тканями, следовательно, снижается и глюкоза, доступная для метаболизма в головном мозге. С определенной долей вероятности можно сказать, что увеличение выживаемости обусловлено анаболическими эффектами инсулина, которые инициируют гибернацию метаболических процессов в головном мозге, тем самым обеспечивается экономия пластических и питательных субстанций.



