Среди заболеваний, сопровождающихся билиарной непроходимостью, важное место занимают патологические изменения большого сосочка двенадцатиперстной кишки [1, 2]. Несмотря на совершенствование технологий визуализации, инструментальная диагностика патологии этой локализации все еще далека от совершенства. Топографо-анатомические и физиологические особенности БСДК, который является зоной функционального объединения всех органов гепатопанкреатодуоденальной зоны (ГПДЗ), детерминируют общность и неспецифичность клинических симптомов, инструментальной семиотики и данных лабораторных методов исследования [3].
Для инструментальной диагностики заболеваний БСДК традиционно используются эндоскопические и лучевые методы исследования. Однако небольшие размеры терминального отдела общего желчного протока и БСДК, содержащих незначительное количество жидкостного содержимого, малые размеры патологических образований этой локализации, воздушная среда двенадцатиперстной кишки (ДПК) создают определенные трудности для методов лучевой диагностики [3, 4, 5]. Современная инструментальная диагностика высокоэффективна в определении уровня и протяженности обструкции желчных протоков, однако наиболее актуальна и сложна дифференциация характера патологического процесса, а именно воспалительных и неопластических изменений на ранней стадии заболевания, что во многом определяет хирургическую тактику [6, 7].
Внедрение в клиническую практику эндоскопической ультрасонографии (ЭУС) повысило возможности объективной диагностики заболеваний БСДК [3, 4]. Эндосонография является уточняющим методом обследования пациентов с новообразованиями БСДК [7], а при внутриампулярном раке БСДК эндосонография обладает наибольшей эффективностью в сравнении с другими методами визуализации [4]. У пациентов с желчнокаменной болезнью, болевым синдромом в правом подреберье неясной этиологии, острым панкреатитом неизвестной этиологии ЭУС может использоваться уже на начальном этапе диагностики заболеваний ГПДЗ непосредственно после транскутанного ультразвукового исследования (УЗИ) [8, 9].
ЭУС обладает наибольшей чувствительностью в дифференциальной диагностике опухолевого и доброкачественного стеноза БСДК, микрохолелитиаза и сладжа желчных протоков, фиброза поджелудочной железы (ПЖ), небольших изменений панкреатических протоков, свидетельствующих о ранних стадиях хронического панкреатита [6, 9]. Однако в настоящее время не разработаны четко сформулированные эндосонографические критерии различных изменений БСДК (как неопластических, так и воспалительных), что вынуждает проводить диагностику ряда заболеваний, в том числе стеноза БСДК, методом исключения «от противного» [5].
В доступной литературе, проанализированной за последние 20 лет от начала широкого внедрения ЭУС в клиническую практику, отсутствуют систематизированные сведения о возможностях и месте эндосонографии в лечебно-диагностическом алгоритме у пациентов с патологией БСДК. Таким образом, несмотря на накопленный опыт инструментальной диагностики, дифференциация патологии БСДК, особенно внутриампулярной локализации, которая не доступна для прямого визуального осмотра, остается одной из актуальных проблем клинической медицины.
Цель исследования – совершенствование инструментальной диагностики заболеваний БСДК путем использования в лечебно-диагностическом алгоритме ЭУС.
Материалы и методы исследования
Объектом исследования являлись 189 пациентов с заболеваниями БСДК, лечившихся в отделениях общей хирургии, гнойной хирургии и гастроэнтерологии Курской областной многопрофильной клинической больницы с 2013 по 2023 годы, которым выполнялась ЭУС. Возраст больных варьировал от 24 до 82 лет, средний возраст составил 69±6,3 года, женщин было 119 (63,0%), мужчин – 70 (37%).
Для определения ЭУС-критериев дифференциальной диагностики заболеваний БСДК все пациенты были разделены на три группы: в первую группу вошли 134 (70,9%) пациента со стенозом БСДК, во вторую группу — 24 (12,7%) больных с одиночными доброкачественными образованиями БСДК, в третью – 31 (16,4%) пациент со злокачественными поражениями БСДК.
Основным показанием для выполнения эндосонографии было уточнение характера патологии БСДК (стенозирующий папиллит, парапапиллярный дивертикул, доброкачественные и злокачественные новообразования), которая была заподозрена или выявлена на предшествующем диагностическом этапе при выполнении фиброгастродуоденоскопии (ФГДС), компьютерной томографии, магнитно-резонансной томографии, эндоскопической ретроградной панкреатохолангиографии (ЭРПХГ). Показаниями к выполнению ЭУС были также: рецидивирующий болевой синдром билиарного или панкреатического типа в сочетании с лабораторными данными холестаза, проявляющимися в повышении уровня билирубина крови и ферментов – маркеров холестаза (щелочной фосфатазы, гамма-глутамилтранспептидазы), расширение общего желчного протока свыше 7 мм при условии отсутствия сведений об этиологии желчной гипертензии по результатам предшествующего диагностического этапа.
Критериями невключения явилась острая хирургическая патология, связанная с острым нарушением оттока желчи (вклиненный конкремент БСДК, тяжелый острый холангит, механическая желтуха класса В, С по Э.И. Гальперину).
Критериями исключения явились патология, связанная с невозможностью проведения эхоэндоскопа в ДПК, а также периампулярная обструкция, связанная с хроническим обструктивным панкреатитом, раком головки ПЖ, обструктивной патологией внепеченочных желчных протоков, холедохолитиазом.
ЭУС и транспапиллярные вмешательства выполнялись с использованием видеоинформационной системы EVIS EXERA II фирмы «Olympus» (Япония) c ультразвуковым процессором EU-ME1 с изменяемой частотой сканирования 7, 5, 12 и 20 МГц, оснащенной видеогастроскопами с датчиками радиального и конвексного ультразвукового сканирования GF UM160 и GF UC140P–AL5. Методика исследования принципиально не отличалась от стандартных приемов эндосонографии органов панкреатобилиарной зоны [9].
Статистическая оценка аналитической надежности методов исследования включала показатели информативности теста: чувствительность, специфичность, точность, являющиеся общепринятыми компонентами технологий доказательной медицины. Оценку информативности эндосонографии проводили на основании сравнения результатов диагностики с результатами морфологического метода исследования, дополненного комплексом достоверных клинико-лабораторных методов, принятых в литературе за золотой стандарт [10]. Окончательный диагноз основывался на данных дооперационной щипковой, перкутанной аспирационной биопсии, ЭУС-контролируемой тонкоигольной пункционной, а также интраоперационной биопсии. Морфологические исследования выполнены 52 (38,8%) больным со стенозом БСДК и всем пациентам с новообразованиями БСДК (55 человек), при этом 96,4% биоптатов были информативны, что связано с использованием внутривенной седации и забором материала после эндоскопической папиллосфинктеротомии (ЭПСТ), если вмешательство выполнялось.
Результаты исследования и их обсуждение
В группе пациентов со стенозом БСДК на основании анализа результатов обследования этих больных, многократного изучения и детализации видеоматериалов ЭУС в рамках настоящего исследования авторами предложены прямые эндосонографические критерии стеноза БСДК, основанные на непосредственном наблюдении зоны патологического сужения терминального отдела общего желчного протока. Авторы считают целесообразным разделять стенозирующие папиллиты на склерозирующие и гиперпластические, поскольку их эндосонографические признаки кардинально отличаются друг от друга.
Прямым критерием склерозирующего стенозирующего папиллита является визуализируемый нитевидный сегмент терминального отдела общего желчного протока, следующий за супрастенотическим расширением (рис. 1). Прямые эндосонографические критерии склерозирующего стенозирующего папиллита выявлены у 41 (30,6%) больного.
Гиперпластический стенозирующий папиллит сонографически характеризуется утолщением стенок ампулярного отдела БСДК с формированием подчеркнутой слоистой структуры смешанной эхогенности (рис. 2).
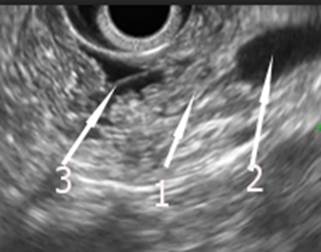
Рис. 1. Эндосонограмма. Склерозирующий стенозирующий папиллит: 1 – нитевидный сегмент терминального отдела общего желчного протока, 2 – общий желчный проток выше сужения, 3 – просвет ДПК
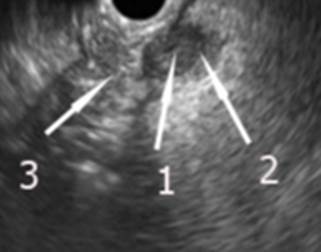
Рис. 2. Эндосонограмма. Гиперпластический стенозирующий папиллит: 1 – БСДК, 2 – утолщенная стенка БСДК, 3 – просвет ДПК
Указанные прямые эндосонографические критерии гиперпластического стенозирующего папиллита с увеличением БСДК в размерах выявлены в 20 (14,9%) случаях. В остальных 73 (54,5%) случаях стеноз диагностирован с учетом совокупности эндосонографических критериев по разработанному в клинике диагностическому алгоритму. Информативными дополнительными критериями стеноза БСДК являются: снижение эластичности терминального отдела общего желчного протока, патологическое уменьшение сосочка в размерах с деформацией продольной складки, увеличение БСДК в размерах с формированием однородной гипоэхогенной структуры.
С учетом сформулированных авторами ЭУС-критериев первоначально диагноз стенозирующего папиллита был установлен у 138 больных, при этом ошибочно стеноз заподозрен у 10 пациентов (ложноположительный результат (ЛП) при отсутствии прямых эхопризнаков и формировании заключения с учетом совокупности косвенных эндосонографических признаков стеноза, сопутствующих желчной гипертензии с умеренным расширением общего желчного протока (в пределах 12 мм). При выполнении ЭРПХГ у четырех из десяти пациентов канюляция холедоха была свободной, без технических трудностей, отток контрастного вещества замедлен не был, от выполнения ЭПСТ у этих пациентов воздержались. Еще у двух больных на фоне консервативной терапии отмечался регресс клинико-лабораторных симптомов билиарной обструкции, а в двух случаях отмечалось уменьшение диаметра общего желчного протока в течение периода госпитализации. Такая клиническая картина была расценена как следствие транзиторного микрохоледохолитиаза. У двух пациентов была гипердиагностика гиперпластического папиллита, при ЭПСТ выявлено внутриампулярное доброкачественное образование.
В шести случаях при эндосонографии стеноз БСДК диагностирован не был, что было расценено как ложноотрицательный результат (ЛО). У двух пациентов отмечался стойкий болевой синдром билиарного характера с характерными лабораторными изменениями, потребовавшими повторной госпитализации. У четырех пациентов стенозирующая патология БСДК манифестировала после выполнения лапароскопической холецистэктомии, в том числе в одном случае в послеоперационном периоде отмечалась гипербилирубинемия до 58 мкмоль/л с расширением общего желчного протока до 10 мм; у одного пациента в первые сутки после выполнения лапароскопической холецистэктомии отмечались миграция клипсы с культи пузырного протока и желчеистечение в свободную брюшную полость; в двух случаях отмечался повышенный дебит желчи по наружным дренажам желчных протоков (свыше 200 мл в сутки).
Таким образом, по результатам эндосонографической диагностики стеноза БСДК истинно положительный результат (ИПП) был у 128 пациентов, в шести случаях имела место ложноотрицательная диагностика, а в десяти – ложноположительная.
При оценке статистических показателей информативности ЭУС в диагностике стеноза БСДК получены следующие результаты: показатель диагностической чувствительности (ДЧ) ЭУС для стеноза БСДК составил 0,95, диагностической специфичности (ДС) – 0,84, диагностической эффективности (ДЭ) – 0,92.
Всего по результатам эндосонографии показания к ЭПСТ в связи с изолированным стенозом БСДК определены у 59 (44,0%) больных, а еще у 75 (56,0%) показанием к транспапиллярным вмешательствам явилось сочетание стеноза и холедохолитиаза, включая конкременты с рыхлой эхографической структурой.
Группа больных с одиночными доброкачественными образованиями БСДК включала 24 (12,7%) пациента. В 11 случаях (45,8%) опухоли располагались внутриампулярно. Средний размер образований составил 0,98±0,11 см. При ЭУС доброкачественное новообразование визуализируется как однородное образование различной эхогенности, чаще изоэхогенное, правильной формы, с ровными контурами, связанное с одной из стенок интраампулярной части терминального отдела холедоха. При этом размеры опухолевидного образования, как правило, небольшие (не более 2 см), сохраняется многослойность БСДК, окружающие анатомические структуры интактны, лимфаденопатия без признаков злокачественности (рис. 3).
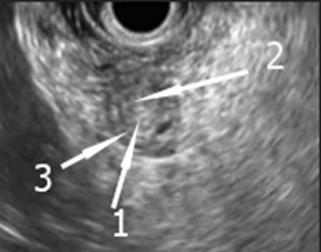
Рис. 3. Эндосонограмма. Аденома БСДК: 1 – БСДК, 2 – аденома, 3 – стенка БСДК
Наиболее частым гистологическим заключением в этой группе пациентов являлся гиперплазиогенный полип, выявленный у 9 (37,5%) больных. Аденоматоз БСДК, представляющий собой гиперплазиогенные аденоматозные разрастания, являющиеся следствием хронического воспаления, обнаружен у 5 (20,8%) больных, папиллярная аденома БСДК выявлена также в 5 (20,8%) случаях. Среди других гистологических заключений встречались: аденомиоматозная гиперплазия – у двух больных, тубулярная аденома – у одного больного, аденофиброзный полип – у одного больного, образование со строением ворсинчатой аденомы – в одном случае.
При диагностике доброкачественных образований БСДК наибольшие сложности возникли при их внутриампулярной локализации и размерах менее 5 мм в диаметре. У двух пациентов диагноз гиперпластического стенозирующего папиллита по результатам ЭПСТ был скорректирован на внутриампулярное доброкачественное образование. В одном случае это была аденома, в другом – гиперплазиогенный полип, размерами до 5 мм. В обоих случаях БСДК сонографически визуализировался в виде однородной гипоэхогенной массы. Скорректированный диагноз подтвержден при выполнении щипковой биопсии после ЭПСТ. В одном случае внутриампулярное образование БСДК размерами 4 мм диагностировано не было. Эти результаты были расценены как ЛО. В трех случаях имели место ЛП, среди которых у двух пациентов заподозренное при ЭУС внутриампулярное образование результатами ЭПСТ подтверждено не было, а изменения БСДК соответствовали гиперпластическому стенозирующему папиллиту. Еще у одного пациента с диагностированной аденомой БСДК по результатам гистологического исследования выявлена высокодифференцированная аденокарцинома. Таким образом, ИП ЭУС в группе был у 21 пациента. Показатели качества диагностики доброкачественных новообразований БСДК при ЭУС были следующими: ДЧ – 0,87, ДС – 0,98, ДЭ – 0,97.
У 18 (75,0%) больных с доброкачественными новообразованиями БСДК выполнялось оперативное лечение, в остальных случаях проводилось динамическое наблюдение. Структура выполненных оперативных вмешательств при доброкачественных новообразованиях БСДК выглядела следующим образом. У 11 (61,1%) больных выполнена ЭПСТ с целью забора материала для гистологического исследования, а также для декомпрессии и нормализации оттока желчи. У трех пациентов с аденомами БСДК, размеры которых не превышали 2,0 см, выполнена ампулэктомия с профилактическим бистентированием желчных и панкреатических протоков. В одном случае выполнена аденомэктомия. У трех больных с образованиями, превышающими 2,5 см, определены показания к лапаротомным вмешательствам.
Злокачественные опухоли БСДК в наблюдаемой группе пациентов были у 31 больного (16,4%), из них у 16 больных (51,6%) диагностированы признаки инфильтративного роста с распространением на стенку ДПК, общего желчного протока, ПЖ. Средний размер образований составил 2,0±0,13 см. Рак БСДК без инфильтрации окружающих тканей характеризуется наличием гипоэхогенного образования с неровными контурами, которое формирует асимметричное резкое сужение типа «обрыв протока», при этом слоистая структура стенок сохранена, образование связано со стенкой БСДК, перихоледохеальные структуры не изменены. Рак БСДК с инфильтрацией окружающих тканей выглядит как гипоэхогенное образование с неровными нечеткими контурами, образующее асимметричное резкое сужение типа «обрыв протока», слоистая структура стенок не просматривается, отмечается гипоэхогенная инфильтрация окружающих тканей, размеры опухоли более 2 см, имеются признаки инвазии в сосудистые структуры, симптом «двух протоков», лимфаденопатия с признаками злокачественности (рис. 4).
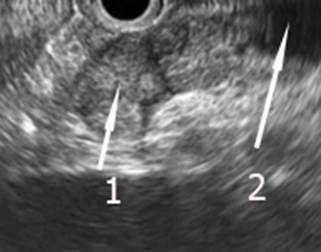
Рис. 4. Эндосонограмма. Рак БСДК: 1 – рак БСДК с прорастанием в общий желчный проток, 2 – терминальный отдел общего желчного проток (обрыв протока)
Частота выявления злокачественных ампулярных опухолей при ЭУС составила 96,8% (30 из 31). Сонографические критерии, характеризующие опухолевые поражения, локализующиеся в небольших по объему полых органах (БСДК, ДПК, терминальный отдел общего желчного протока), особенно с инфильтрацией окружающих тканей, дополненные прямым визуальным осмотром и биопсией, обеспечивают высокую эффективность диагностики. В одном случае имел место ложноотрицательный результат: при ЭУС не диагностирована экстраампулярная аденокарцинома T1N0М0, а сонографическая картина образования, учитывая размеры в 15 мм и расширение общего желчного протока не более 10 мм, расценивалась как аденома БСДК. По результатам первичного морфологического исследования биоптата – ворсинчатая аденома. Трудности дифференциальной диагностики возникали при опухолях БСДК размерами более 3 см с инфильтрацией головки или крючковидного отростка ПЖ, стенки ДПК и терминального отдела общего желчного протока. У 5 (16,1%) пациентов со злокачественными образованиями БСДК диагноз установлен по результатам выполненных тонкоигольных пункций под контролем ЭУС, когда при повторных щипковых биопсиях гистологической верификации получено не было.
В выявлении злокачественных новообразований ЭУС оказалась наиболее информативна, ее ДЭ составила 0,99.
Основные результаты диагностики и доля выполненных оперативных вмешательств пациентов с заболеваниями БСДК отражены в таблице.
Результаты ЭУС-диагностики и лечения пациентов с заболеваниями БСДК
|
Группы наблюдения |
Истинно положительный результат |
Ложноотрицательный результат |
Ложноположительный результат |
Чувствительность |
Специфичность |
Эффективность |
Доля выполненных оперативных вмешательств (%) |
|
Стеноз БСДК (n=134) |
128 |
6 |
10 |
0,95 |
0,84 |
0,92 |
44,0 |
|
Доброкачественные новообразования БСДК (n=24) |
21 |
3 |
3 |
0,87 |
0,98 |
0,97 |
75,0 |
|
Злокачественные опухоли БСДК (n=31) |
30 |
1 |
–- |
0,97 |
0,97 |
0,99 |
16,1 |
Выводы
1. ЭУС является высокоинформативным методом диагностики патологии БСДК, диагностическая эффективность при стенозах БСДК, доброкачественных и злокачественных новообразованиях составляет 0,92, 0,97 и 0,99 соответственно.
2. При патологии БСДК ЭУС можно рекомендовать в качестве основного метода диагностики.
3. При стенозе БСДК эндосонография является методом диагностики, позволяющим непосредственно визуализировать прямые признаки этой патологии.
4. Результаты эндосонографии являются основанием для выбора тактики лечения и определения показаний к транспапиллярным малоинвазивным вмешательствам.



