Достижение благоприятного исхода лечения переломов костей остается одной из важных задач оказания медицинской помощи как в стационарных, так и в поликлинических условиях. Анализ литературных источников, результатов исследования с применением новых технологий лечения показывает, что в основе лечения лежит способ фиксации и консолидации костных отломков с перспективой образования в зоне первичной мозоли пластинчатой кости.
Научные убеждения, основанные на анализе устаревших взглядов на подходы к выполнению оперативного вмешательства при остеосинтезе, предполагают кризис, так как результаты оценки качества медицинской помощи для медицинских организаций, предоставляющих медицинские услуги, остаются на низком уровне, что находит отражение в исках, направленных в следственный комитет, прокурату и суды. Наиболее частыми причинами исков являются высокая частота осложнений в ходе предоставления медицинских услуг, среди которых – несросшийся перелом костей, формирование ложных суставов, деформации, тугоподвижность суставов в зоне перелома, развитие остеомиелита, а также трудность лечения и высокий уровень инвалидизации со стойкой утратой общей трудоспособности той или иной степени в процентном отношении [1]. Частота неблагоприятных исходов порой достигает, по данным разных авторов, 50%. Указанные причины обусловили актуальность нашего исследования.
На сегодняшний день нет установленной классификации осложнений, определения этапов и соответствующих им последствий лечения переломов костей. Нередко не учитывается и фоновая патология костной системы. А ведь именно остеопороз наиболее часто провоцирует значительное расхождение костных отломков, разрыв мягких тканей, развитие внутрикостных кровоизлияний с выраженным лимфоцитарно-пролиферативными изменениями, затяжным воспалительным процессом. Все это замедляет образование костной мозоли, концы отломков резорбируются с образованием ложного сустава или псевдоартроза, признаком которого является закрытие костномозгового канала пластинкой компактного вещества.
Цель исследования – установить морфологические критерии осложнений при заживлении перелома на фоне остеопороза, позволяющие использовать их в производстве экспертизы качества медицинской помощи.
Материалы и методы исследования
Перспективное исследование проведено в травматологическом отделении БУЗОО «ГКБ № 1 им. А.Н. Кабанова» (г. Омск, Омская область, Российская Федерация) в период с 01.02.2022 года по 11.02.2023 года. Были отобраны 119 пациентов с диагностированным согласно клиническим критериям остеопорозом в возрасте от 29 до 59 лет с травмами различных областей тела: закрытыми травмами груди с переломами ребер по различным анатомическим линиям и закрытыми травмами тазового кольца (плоские кости), закрытыми травмами верхних и нижних конечностей с переломами длинных трубчатых костей и различными травмами позвоночного столба. Контроль исследования проведен в группе из 43 пациентов в возрасте от 21 до 39 лет без остеопороза (рентгенография и МСКТ-исследование). Распределение пациентов по половому признаку представлено в таблице 1. Материал был получен в ходе оперативного лечения, во время операции проводилась резекция кости в зоне перелома в различные сроки посттравматического периода (в зависимости от времени обращения, показаний для оперативного лечения, характера осложнений). Резецированную кость промывали проточной водой и помещали во флаконы с 10%-ным раствором нейтрального формалина, который выполнял функцию фиксатора. Перед окраской обязательно проводили обезвоживание этиловым спиртом по восходящей возгонке путем погружения фрагментов костной ткани в спирты увеличивающейся концентрации, с последующим помещением в ксилол-парафин. Остывший и затвердевший материал устанавливали в микротом с изготовлением срезов. Перед помещением на предметное стекло костная ткань подвергается дополнительной декальцинации. Для окрашивания костной ткани использовали краситель – гематоксилин-эозин и раствор тионина. Из каждого фрагмента костной ткани изготавливали 3 среза, которые помещали на одно предметное стекло. Обработка полученного материала, изготовление микропрепаратов гистологического материала, окраска костной ткани осуществлялись в патологоанатомическим отделении БУЗОО ГКБ № 1 им. Кабанова А.Н. Микросрезы просмотрены под большим и малым увеличением микроскопа «Zeiss PrimoStar» (Китай) и «Микмед – 6 ЛОМО» (Россия). Таким способом было исследовано 162 объекта (486 гистологических препаратов).
Таблица 1
Распределение пациентов по половому признаку
|
|
Исследуемая группа |
Группа контроля |
||
|
Количество |
% |
Количество |
% |
|
|
Мужчины |
62 |
52,1 |
28 |
65,2 |
|
Женщины |
57 |
47,9 |
15 |
34,8 |
|
Итого |
119 |
100 |
43 |
100 |
Результаты исследования и их обсуждение
При световой микроскопии установлены принципиально важные особенности переломов. В обеих группах в зоне перелома – деформация костных балок, участки размозжения костного мозга, разрывы кровеносных сосудов с выходом эритроцитов в периваскулярное пространство, с последующим формированием кровоизлияния без клеточной реакции между отломками. В исследуемой группе отличительный признак – массивное, большее по размеру, площади и объему в сравнении с группой контроля, кровоизлияние с инфильтрацией окружающих мягких тканей, расслоением соединительно-тканных структур надкостницы, наличием поднадкостничной гематомы, инфильтрацией гемолизированными эритроцитами костного мозга. При расслоении и отслоении надкостницы массивными гематомами отмечается значительное, более 3 мм смещение отломков. В зоне «комоционных изменений», прилежащей к зоне перелома, как в исследуемой группе, так и в группе контроля, в равной степени наблюдается инфильтрация гемолизированными эритроцитами костномозговых пространств, при которой происходит деструкция гистоархитектоники костной ткани [2, 3]. Все это как в отдельности, так и в совокупности замедляет паранеопластические процессы в зоне перелома, с одной стороны, а с другой – является субстратом для формирования внутрикостных переломов за счет деструкции костных балок, лизиса остеоцитов, снижения количества остеобластов, размозжения кровеносных сосудов [2, 3]. Внутрикостные переломы, фиксированные при микроскопическом исследовании, долгое время сохраняются в окружении массивных кровоизлияний. Помимо гемолизированных эритроцитов, отмечаются лимфоцитарно-пролиферативные процессы, при которых долгое время большинство остеоцитов разрушены или находятся в состоянии пикноза [3].
В ряде случаев видно скопление лейкоцитов в центре зоны травмы, что говорит о сохраняющихся явлениях воспаления, что является основой для развития осложнений в виде остеомиелита. В зоне повреждения развивается серозное воспаление. К концу третьих суток отмечается серозная, серозно-десквамативная и серозно-гнойная инфильтрация различными клетками воспалительного ряда с нарушением гистоархитектоники костного мозга, нарушением соотношения жировых клеток и зоны кроветворения, инфильтрацией эритроцитами, нейтрофилами, лимфоцитами, моноцитами и макрофагами окружающих мягких тканей. По костномозговому каналу воспалительный процесс быстро переходит с метафиза к диафизу. Через гаверсовы каналы гной распространяется в пространство между костью и надкостницей с отслоением последней. Это в совокупности с тромбозом сосудов в гаверсовых каналах усиливает дистрофические процессы в кости, увеличивается количество остеокластов, и, как следствие, наблюдается резорбция костной ткани с формированием обширных участков некроза кости и надкостницы (рис. 1).
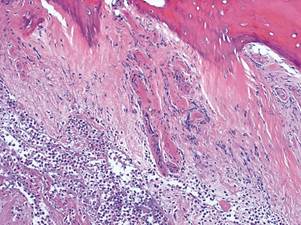
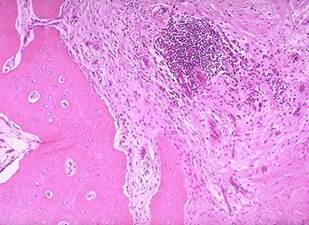
Рис. 1, 2. Продуктивное воспаление низкой активности в фиброзной оболочке очага при хроническом травматическом остеомиелите. Неполный секвестр. Окраска гематоксилин-эозином. Увеличение х200
Гистологические структуры костной ткани, подверженные деструкции и распаду, постепенно отторгаются и, отграничиваясь от сохранной костной ткани, образуют полости – секвестры со скоплением остеоцитов и остеокластов на границе со здоровой костной тканью с разрастанием грануляционной ткани в пограничной зоне секвестра [4]. Демаркация, которая начинается в острой стадии, может занимать неопределенно долгий период и завершаться уже при полном формировании фиброзной капсулы в окружении зоны воспаления (рис. 2). Соединительная ткань, разрастающаяся в зоне перелома, со временем приобретает структуру грубоволокнистой и в будущем является фундаментом для формирования костной микроскопической мозоли. При ненарушенном остеогенезе клеточно-волокнистая мозоль замещается пластинчатыми костными структурами. В группе исследования, когда фоновая патология извращает репаративные процессы, нарушая остеогенез за счет массивных гематом с ярко выраженными лимфоцитарно-пролиферативными воспалительными процессами, отломки костей соединялись клеточноволокнистой тканью с преобладанием коллагеновой структуры над остеогенной [5].
Лимфоцитарно-пролиферативный процесс, персистирующий в костной ткани и окружающих мягких тканях, может продолжаться месяцы и годы [6]. При этом на фоне низкоактивного пролиферативного процесса могут возникать эпизоды усиления и активации воспалительного процесса в зоне остеомиелитического очага, обозначая рецидив экссудативного воспаления [6]. Комплекс патологических изменений наиболее часто характеризует серозно-десквамативный с умеренно выраженной полиморфно-ядерной инфильтрацией из нейтрофильных лейкоцитов, лимфоцитов, макрофагов с увеличением сосудистой проницаемости, часто – с отложением фибрина, окрашенного эозином, как отражение фибринозно-гнойного воспаления – период обострения хронического остеомиелита [6-8].
На фоне извращения остеогенеза в процессе нарушенных процессов резорбции и репарации костной ткани при остеопорозе, хронизации воспалительных процессов в зоне перелома в 15% случаев спустя три года после оперативных вмешательств было отмечено значительное образование костной мозоли в зоне перелома. Первоначальный диагноз, как правило, выставляется «периохондрит». При клинических исследованиях (рентгенологическое и МСКТ-исследование) отчетливо выражены участки очагового остеолиза, реактивное периостальное костеобразование в виде остеофитов, разрушение кортикального слоя [9, 10]. В пограничной зоне между хрящевой частью и костными структурами наблюдаются признаки эндохондральной оссификации [10]. При нативном исследовании макроскопическим признаком в таком случае является дольчатое разрастание соединительной ткани, располагающееся на тонкой ножке или на широком основании (за счет прорастания) [10]. При гистологическом исследовании отмечаются клеточный полиморфизм хрящевой ткани, миксоматоз стромы, нарушение структуры с деструкцией лакунарности хондроцитами [10].
Анализируя составляющие морфологического субстрата остеомиелитических очагов, а именно скопления воспалительного экссудата, нарушение гистоархитектоники за счет некротизированных тканей, клеточного полиморфизма в зоне перелома предсуществующей костной ткани и жизнеспособной регенерирующей ткани кости, авторы пришли к следующим результатам.
В группе исследования фоновая патология в виде остеопороза преобладает деструктивная форма, отличительным признаком которой является наличие зоны деструкции с образованием полости распада с полиметрическими характеристиками с ярко выраженным высокоактивным воспалительным (экссудативным или продуктивным) процессом и фиброзирующим микроабсцедированием костной ткани (рис. 3, 4) [6].
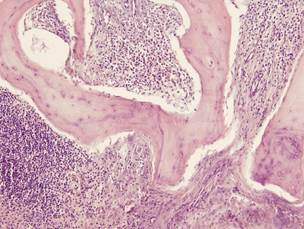
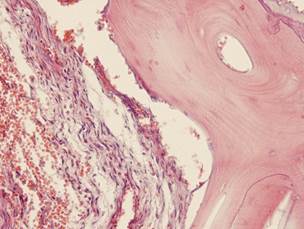
Рис. 3, 4. Массивный рост грануляционной ткани в зоне гнойного расплавления костного мозга; рассасывание и секвестрация участков кости, подвергнувшихся некрозу Окраска гематоксилин-эозином. Увеличение х200 [6]
В контрольной группе преобладала фиброзирующе-остеосклерозирующая форма. Отличительным признаком является продуктивное воспаление с образованием грануляционной ткани с отсутствием в зоне поражения гнойного расплавления с образованием полостной деструкции костной ткани (рис. 5) [6].
При анализе результатов рентгенологического исследования, данных МСКТ у пациентов с остеопорозом необходимо правильно оценить зону перехода деструктивного очага на окружающие мягкие ткани, надкостницу и интактную кость [11, 12, 13]. Нами установлены 2 фундаментальных критерия, которые необходимо фиксировать при рентгенологическом исследовании:
1) граница деструктивного очага четкая, мягкие ткани отграничены, а сам очаг плотный;
2) границы деструкции размыты с широкой переходной остеолитической зоной [3, 6, 13].
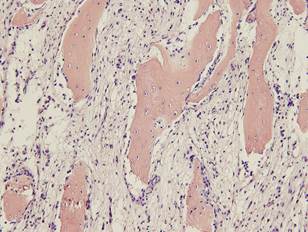
Рис. 5. Разрастания рыхлой соединительной ткани в зоне перелома с признаками вялотекущего воспалительного процесса в межтрабекулярных пространствах с клеточным полиморфизмом. Субпериостально – остеогенез реактивного характера. Окраска гематоксилин-эозином. Увеличение х200
Помимо этого, для каждой группы характерны свои исходы. В исследуемой группе с остеопорозом нередко наблюдаются поствоспалительные кисты кости, укорочения и деформации кости. В контрольной группе часто наблюдается фиброз костного мозга и костной ткани.
Длительное обездвиживание конечности, связанное с увеличением сроков репаративных процессов в зоне перелома на фоне остеопороза, приводит к образованию приобретенных контрактур [3, 14]. Воспалительные изменения сухожилий, а также распространение воспалительного процесса лежат в основе тендогенных контрактур, при которых суставы принимают стойкое вынужденное положение вследствие развития рубцов и спаек, фиксирующих сухожилия [3]. Остеопороз является исходной точкой запуска широкого каскада патологических процессов с ярким полиморфизмом извращенного репаративного процесса с трансформацией хондрогенных клеток в остеогенные, что в конечном итоге приводит к формированию грубоволокнистой соединительной ткани на месте должной хрящевой с разрастанием перихондрального кольца и образованием костной манжеты прямо в месте диафиза [3, 15]. Количество кровеносных сосудов резко снижается, что обусловливает развитие патологических процессов с приумножением дистрофических процессов в хрящевой ткани, расплавлением хондроцитов. Некроз хондроцитов, в свою очередь, запускает процесс перемещения остеобластов и остеогенных клеток по каналам [3, 16]. Окостенение по типу эндохондрального со временем переходит в эпифизарное, с формированием грубых артрогенных контрактур [3, 6].
Выводы
Остеопороз как фоновая патология нарушает репаративные процессы в зоне перелома, извращает остеогенез, что приводит к огромному каскаду осложнений, изменяя сроки лечения и реабилитации в сторону увеличения периода временной нетрудоспособности. Посттравматический остеомиелит с развитием гнойно-септических состояний представляет угрозу жизни и соответствует тяжкому вреду здоровью, вызвавшему расстройство жизненно важных функций организма человека, которое не может быть компенсировано организмом самостоятельно и обычно заканчивается смертью (п. 6.2 «медицинских критериев, установленных приказом МЗ и СР России от 24.04.2008 г. № 194н «Об утверждении медицинских критериев определения степени тяжести вреда, причиненного здоровью человека»). Последствия осложненных переломов приводят к стойкой утрате общей трудоспособности в соответствии с таблицей процентов стойкой утраты общей трудоспособности в результате различных травм, отравлений и других последствий внешних причин, прилагаемой к медицинским критериям. В ходе производства экспертизы качества медицинской помощи все это негативно отражается на выводах эксперта, снижая уровень качества оказанных услуг.
Таким образом, остеопороз может не только быть истинной первопричиной переломов при незначительном травматическом воздействии, но и способен привести к развитию различной вариации осложнений и их последствий. Именно эти обстоятельства должны быть глубоко исследованы при производстве экспертизы качества медицинской помощи с целью определения уровня качества медицинской помощи. Осложнения переломов, возникших на фоне остеопороза, не должны расцениваться как дефект оказания медицинской помощи в соответствии с п. 25 Медицинских критериев, установленных приказом МЗ и СР России от 24.04.2008 г. № 194н «Об утверждении медицинских критериев определения степени тяжести вреда, причиненного здоровью человека» и в соответствии с приказом МЗ РФ от 10.05.2017 г. об утверждении критериев оценки качества медицинской помощи.



