Экстренное оперативное лечение больных с осложненными большими и гигантскими послеоперационными вентральными грыжами (ПОВГ) всегда сопряжено с тактическими и техническими трудностями. Несмотря на постоянный поиск и обновление методов хирургического лечения больших и гигантских ПОВГ, проблема выбора оптимального способа операции сохраняет свою актуальность и в настоящее время [1,2]. В течение многих лет частота развития вентральной грыжи после лапаротомии составляет от 10 до 20% и не имеет тенденции к снижению [2,3,4]. Ущемление больших и гигантских ПОВГ встречается редко, это связано с большими размерами грыжевых ворот. Чаще приходится встречаться с острой спаечной тонкокишечной непроходимостью в грыжевом мешке. У таких пациентов часто развиваются тяжелые гнойно-септические осложнения в виде флегмоны грыжевого мешка или кишечных свищей, что значительно ухудшает течение и прогноз заболевания [5].Больные с большими и гигантскими ПОВГ являются, как правило, представителями старших возрастных групп, страдают ожирением разной степени выраженности и разнообразной коморбидной патологией [6]. Экстренная ситуация, возникающая при ущемлении ПОВГ или при развитии острой кишечной непроходимости в грыжевом мешке, не позволяет провести адекватную предоперационную коррекцию имеющихся соматических нарушений, что в значительной степени повышает риски развития осложнений [6,7]. Внутрибрюшная гипертензия, которая имеет место у большинства больных с большими и гигантскими ПОВГ до операции [3,8], приобретает критический характер при развитии кишечной непроходимости в грыжевом мешке и паралитической кишечной непроходимости в раннем послеоперационном периоде. Риск развития синдрома абдоминальной компрессии после экстренной герниопластики вынуждает отказываться от применения классических видов пластики в пользу технологий «bridge», после которых значительно возрастает частота рецидивов и местных раневых осложнений [3,9,10].
Материалы и методы исследования
Изучены непосредственные и отдаленные результаты хирургического лечения 57 больных с осложненными большими и гигантскими ПОВГ, находившихся на лечении в хирургических отделениях ГБУЗ «ККБСМП г. Краснодара» МЗ КК за период с 2010 по 2022 гг. Все они были разделены на 2 группы. В основную группу вошли 25 (43,9%) пациентов, которые были оперированы с использованием предложенного авторами метода (патент РФ № 2685636 от 19.04.2018 г. «Способ герниопластикиобширных и гигантских послеоперационных вентральных грыж»). Группу контроля составили 32 (56,1%) больных, оперированных с применением других методов пластики грыжевого дефекта. Для обеспечения репрезентативности сформированных групп и рандомизации пациентов в настоящей работе использовали классификацию вентральных грыж (SWR) Европейского герниологического общества (EHS).Определение степени тяжести состояния больных при поступлении и при проведении динамического наблюдения в послеоперационном периоде проводилось с помощью интегральных шкал APACHE II (Acute Physiology and Chronic Health Evaluation II) и SOFA (Sequential Organ Failure Assessment).
Всемпациентам при поступлении в клинику выполнялось ультразвуковое исследование брюшной полости с использованием аппаратов Aloka 2500 и Toshiba Aplio 300 с конвексными мультичастотными датчиками 3,5–12 Mhz. По данным УЗИ определяли площадь (S) грыжевого дефекта в см2. При круглой форме грыжевого дефекта его площадь определяли по формуле:
S=πR2,
где R – радиус окружности.
При эллипсоидной форме грыжевого дефекта для определения его площади использовали формулу:
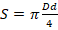 ,
,
где D и d – длинная и короткая оси эллипса.
В случае наличия множественных дефектов апоневроза вычисляли их общую площадь.
Кроме этого, всем пациентам была выполнена компьютерная томография (КТ) органов брюшной полости и передней брюшной стенки с использованием аппаратов Philips Brilliance 64, Siemens SOMATOM Emotion 6 в режимах «Abdomen W300 C40» (мягкотканный протокол) или с контрастированием (Ультравист 300/350/370, Омнипак, Омнискан, Изипак), а после получения данных КТ вычисляли площадные и объемные показатели грыжи.
Объем грыжевого мешка и брюшной полости определялся по формуле:
V=A×B×C×0,52,
где A – фронтальный размер, B – сагиттальный размер и C – краниокаудальный размер.
Отношение объемов грыжевого мешка и брюшной полости или VR (volumeratio) определяли по формуле:
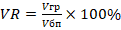 ,
,
где Vгр – объем грыжевого мешка, Vбп – объем брюшной полости.
Критическими считали значения VR>25%.
Всем больным основной группы и 47 (55,3%) пациентам в контрольной группе проводили периоперационный мониторинг внутрибрюшного давления (ВБД) в соответствии с рекомендациями WSACS. Использовали стандартную методику измерения через мочевой катетер с помощью устройства «Abdo Pressure Uno Meter»™. с помощью аппарата «Uno Meter Abdo Pressure®Kit» (ЗАО «Уномедикал», РФ). Первое измерение ВБД проводили непосредственно перед оперативным вмешательством, затем в процессе проведения герниопластики и ежедневно в течение первых 5 суток послеоперационного периода. При оценке результатов использовали классификацию WSACS.
Результаты обследования больных, включенных в исследование, фиксировались в интерактивной карте пациента. Все числовые данные представлены в виде M±m. При условии сопоставимости объемов выборки и нормального распределения данных в группах наблюдения для оценки достоверности различий средних арифметических показателей проводили дисперсионный анализ путем примененияt-критерия Стьюдента.
В случаях отсутствия нормального распределения данных в группах наблюдения межгрупповые различия оценивали с помощью непараметрического двустороннего критерия Манна–Уитни. Для повторных измерений некоторых показателей использовали критерий Вилкоксона. Различия считали достоверными при р<0,05. Для оценки статистической значимости различий двух или нескольких показателей в группах наблюдения определяли критерий согласия Пирсона.Для упрощения некоторых расчетов использовали online-калькуляторы, имеющиеся в свободном доступе в Интернете. В работе применяли PCAMD Ryzen 5 3500X 6-Core Processor 3.59 GHz с установленным лицензионным программным обеспечением, текстовым редактором и графическим диспетчером Microsoft Office.
Результаты исследования и их обсуждение
Подавляющее число пациентов в обеих группах наблюдения, согласно классификации EHS, относились к классу М; W3-W4; R0; Группы были сопоставимы по морфометрическим показателям. Средний диаметр грыжевых ворот составил в основной группе 98,4±18,5 см2, в контрольной группе – 90,6±23,1 см2, при объеме грыжевого мешка 937,4±116,6см3 и 897,8±94,8 см3соответственно. Показатель VR (volumeratio) составил для пациентов основной группы 23,6±4,7%, для больных в группе контроля – 21,9±5,5. Также не обнаружено статистически достоверной разницы между группами наблюдений по показателю CCI (индекс коморбидностиM.E.Charlson) – 2,3±1,2 балла в основной и 2,5±1,3 балла в контрольной группе (табл.1). У большинства пациентов, помимо сопутствующей соматической патологии, диагностировано ожирение 2–3-й степени. Средний ИМТ в основной группе составил 32,4±2,6 балла, в контрольной – 33,1±1,8 балла. В подавляющем большинстве случаев и в основной, и в контрольной группе больных в качестве показаний к экстренному оперативному лечению выступала клиническая картина острой спаечной тонкокишечной непроходимости в грыжевом мешке. Истинное ущемление грыжи диагностировано только у 2 (3,5%) пациентов в основной группе и у 1 (3,1%) больного в контрольной. Указанные обстоятельства обусловливали предоперационное повышение внутрибрюшного давления до значительных величин. У всех больных, оперированных в экстренном порядке, показатели ВБД до операции соответствовали 1–2-й степени тяжести абдоминальной гипертензии. Средние показатели ВБД у экстренных больных основной группы составили 12,2±3,6 ммрт.ст.У 11 (44%) из них по данным обследования выявлены признаки полиорганной дисфункции. Средний балл по шкалам APACHEII и SOFA составили 11,2±1,7 и 3,3±0,04 соответственно. В контрольной группе средние показатели ВБД составили 13,1±4,1 ммрт.ст., а средний балл по шкалам APACHE II и SOFA – 12,0±1,3 и 3,2±0,5 соответственно.
Таблица1
Характеристикабольных с послеоперационными вентральными грыжамив основной и контрольной группе
|
Показатель
|
Группы |
Уровень достоверности по критерию ꭓ2 |
ВСЕГО |
||
|
Основная (n=25) |
Контрольная (n=32) |
||||
|
S |
M |
23 (92%) |
32 (100%) |
р>0,05 |
55 (96,5%) |
|
L |
2 (8%) |
– |
р>0,05* |
2 (3,5%) |
|
|
W |
W3 |
14 (56%) |
17 (53,1%) |
р>0,05 |
31(54,4%) |
|
W4 |
11(44%) |
15 (46,9%) |
р>0,05 |
26 (45,6%) |
|
|
R |
R0 |
18 (72%) |
21 (65,6%) |
р>0,05 |
39 (68,4%) |
|
R1 |
4 (16%) |
6 (18,8%) |
р>0,05 |
10 (17,5%) |
|
|
R2 |
3 (12%) |
5 (15,6%) |
р>0,05 |
8 (14,1%) |
|
|
ИТОГО: |
25 (100%) |
32 (100%) |
– |
57 (100%) |
|
|
S грыжевых ворот (см2) |
98,4±18,5 |
90,6±23,1 |
р>0,05 |
– |
|
|
V грыжи (см3) |
937,4±116 |
897,8±94 |
р>0,05 |
– |
|
|
VR (volume ratio) (%) |
23,6±4,7% |
21,9±5,5 |
р>0,05 |
– |
|
|
CCI(индекс коморбидности) |
2,3±1,2 |
2,5±1,3 |
р>0,05 |
– |
|
|
ВБД (мм Hg) |
12,2±3,6 |
13,1±4,1 |
р>0,05 |
– |
|
|
APACHE II |
11,2±1,7 |
12,0±1,3 |
р>0,05 |
– |
|
|
SOFA |
3,3±0,04 |
3,2±0,5 |
р>0,05 |
– |
|
Примечание: * – оценка по точному критерию Фишера
В контрольной группе пациентов пластика «on-lay» выполнена у 19 (59,4%) больных, пластика in-lay (bridge) – у 9 (28,1%) пациентов и предбрюшинная пластика «sublay» – в 4 (12,5%) случаях.
У всех больных основной группы выполнена герниопластика по оригинальному методу, суть которого заключалась в следующем: после выделения грыжевого мешка и подготовки участка неизмененного апоневроза, отступая 4–5 см от грыжевых ворот, грыжевой мешок вскрывают. При этом брюшина грыжевого мешка делится на 2 неравных лоскута. Меньший лоскут должен быть не менее диаметра грыжевых ворот, а больший на 4–5 см выходить за периметр грыжевых ворот (рис. 1). После устранения причины кишечной непроходимости в грыжевом мешке или ущемления петель кишечника содержимое мешка вправляется в брюшную полость.
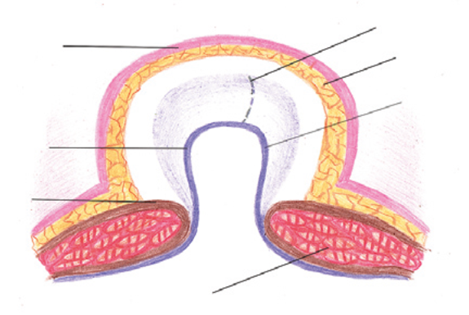
Рис. 1.Грыжевой мешок, разделенный на два неравных лоскута.
1 – кожа; 2 – подкожная жировая клетчатка; 3 – апоневроз; 4 – мышечная ткань; 5 – лоскут грыжевого мешка бóльшего размера; 6 – лоскут грыжевого мешка мéньшего размера; 7 – линия рассечения грыжевого мешка
Лоскутом грыжевого мешка меньшего размера укрывают грыжевые ворота, фиксируя его к краю апоневроза, тем самым полностью изолируя брюшную полость. Сетчатый имплантат выкраивают так, чтобы он не менее чем на 2–3 см выходил за пределы грыжевых ворот, фиксируют узловыми швами по периметру к неизмененному апоневрозу. Далее большим лоскутом грыжевого мешка укрывают сетчатый имплантат и фиксируют его к неизмененному апоневрозу узловыми швами, полностью перекрывая эндопротез по его периметру на 1–2 см, тем самым исключают его контакт с подкожно-жировой клетчаткой (рис. 2).
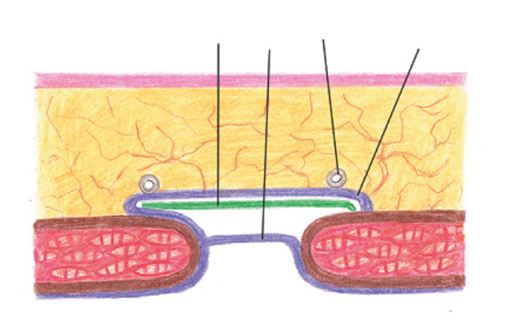
Рис. 2.Окончательный вид пластики.
1 – лоскут грыжевого мешка мéньшего размера; 2 – лоскут грыжевого мешка бóльшего размера; 3 – сетчатый имплантат; 4 – дренажная трубка
При изучении динамики ВБД в раннем послеоперационном периоде у больных с большими и гигантскими ПОВГ удалось выявить некоторые закономерности. Во всех случаях контрольной группы в первые сутки после операции наблюдалось достоверное (р<0,01) и значительное увеличение показателей ВБД по сравнению с исходными (табл. 1). Наибольший прирост показателей ВБД отмечен у пациентов контрольной группы, которым выполнялась «on-lay» и «sublay» пластики, на 88,1% и 84,6% соответственно. У больных с пластикой in-lay (bridge) прирост показателей ВБД был достоверно ниже и составил 42,9%.
В основной группе пациентов в первые сутки после операции средние показатели ВБД составили 18,9±2,7 ммрт.ст., что на 54,9% выше исходных, и были сопоставимы с данными, полученными у больных контрольной группы после проведения пластики in-lay (bridge). Высокие показатели ВБД устойчиво сохранялись до конца вторых суток послеоперационного периода и их изменения носили статистически не достоверный характер в большинстве случаев. Начиная с третьих суток послеоперационного периода у всех пациентов в группах наблюдения отмечено снижение показателей ВБД, однако даже на пятые сутки после операции средний уровень ВБД соответствовал 1-й степени тяжести внутрибрюшной гипертензии и составлял около 10 ммрт.ст.
Таблица 2
Динамика показателей ВБД в раннем послеоперационном периоде у больных основной и контрольной групп в зависимости от вида пластики грыжевого дефекта
|
Сутки наблюдения |
Показатели |
Вид пластики |
|||
|
«on-lay» (n=19) |
in-lay (bridge) (n=9) |
«sublay» (n=4) |
Оригинальный метод (n=25)
|
||
|
ВБД перед операцией |
12,6±2,4 |
14,1±2,8 |
13,5±2,5 |
12,2±3,6 |
|
|
1 |
ВБД* |
23,7±3,3 |
20,1±2,1 |
24,5±2,0 |
18,9±2,7 |
|
ΔВБД |
+11,7 |
+6,0 |
+11,0 |
+6,7 |
|
|
Тср (%) |
188,1 |
142,9 |
184,6 |
154,9 |
|
|
Т-критерий |
0,5 |
2,5 |
0,5 |
0,5 |
|
|
р |
р<0,01 |
р<0,05 |
р<0,01 |
р<0,01 |
|
|
2 |
ВБД |
25,6±2,2 |
20,4±1,7 |
23,8±2,3 |
20,2±2,5 |
|
ΔВБД |
+1,9 |
+0,3 |
–0,7 |
+1,6 |
|
|
Тср (%) |
108,0 |
101,5 |
109,7 |
6,9 |
|
|
Т-критерий |
15,5 |
34,5 |
12,5 |
14,5 |
|
|
р |
р>0,05 |
р>0,05 |
р>0,05 |
р>0,05 |
|
|
3 |
ВБД |
19,2±1,3 |
16,9±2,6 |
17,5±2,8 |
14,2±2,3 |
|
ΔВБД |
–6,4 |
–3,5 |
–6,3 |
–6,0 |
|
|
Тср (%) |
75,0 |
82,8 |
74,2 |
70,3% |
|
|
Т-критерий |
4,5 |
6,0 |
3,5 |
2,5 |
|
|
р |
р=0,05 |
р>0,05 |
р<0,05 |
р<0,05 |
|
|
5 |
ВБД |
11,8±2,2 |
9,3±1,2 |
10,7±2,2 |
8,5±1,8 |
|
ΔВБД |
–7,4 |
–7,6 |
–6,8 |
–5,7 |
|
|
Тср (%) |
61,5 |
55,0 |
61,1 |
59,9% |
|
|
Т-критерий |
0,5 |
0,5 |
1,5 |
0,5 |
|
|
р |
р<0,01 |
р<0,01 |
р<0,05 |
р<0,01 |
|
В раннем послеоперационном периоде у 2 (6,3%) пациентов из 32 из контрольной группы развился абдоминальный компартмент синдром с явлениями прогрессирующей полиорганной недостаточности – в 1(25%) случае после пластики «sublay» и в 1 (5,3%) наблюдении после пластики «on-lay». У одного из этих пациентов потребовалось проведение повторного декомпрессивного оперативного вмешательства с удалением сетчатого эндопротеза. Нагноение операционной раны, которое не потребовало удаления эндопротеза, зарегистрировано в 1 (11,1%) случае после «in-lay» (bridge) пластики. Серомыв подкожные клетчатки формировались у 3 (9,4%) пациентов контрольной группы, из них у 2 (10,5%) больных – после пластики «on-lay» и у 1 (11,1%) – после «in-lay» (bridge) пластики. Образования сером в подкожной жировой клетчатке после пластики «sublay» у больных контрольной группы не выявлено. Послеоперационная пневмония диагностирована у 2 (6,3%) больных контрольной группы. Общая частота осложнений раннего послеоперационного периода в контрольной группе пациентов составила 28,1% (9 случаев). В раннем послеоперационном периоде в контрольной группе умерли 2 больных с выраженной сопутствующей соматической патологией, летальность в группе составила 6,3%.
В основной группе пациентов после проведения герниопластики по предложенной авторами оригинальной методике удалось добиться снижения частоты ранних послеоперационных осложнений до 8%, в основном за счет уменьшения количества нагноений операционной раны, формирования сером и гематом в подкожной жировой клетчатке (табл. 3).
Таблица 3
Распределение осложнений в группах наблюдения
|
ОСЛОЖНЕНИЯ |
Группы наблюдения |
|||||
|
Контрольная (n=32) |
Основная |
|||||
|
«on-lay» (n=19) |
In-lay (bridge) (n=9) |
«sublay» (n=4) |
Всего |
Оригинальный метод(n=25) |
|
|
|
Ранние |
5 (26,3%) |
2 (22,2%) |
2 (50,0%) |
9 (28,1%) |
2 (8,0%) |
|
|
АКС |
1 (5,3%) |
– |
1 (25,0%) |
2 (6,3%) |
– |
|
|
Пневмония |
1 (5,3%) |
|
1 (25,0%) |
2 (6,3%) |
1 (4,0%) |
|
|
Нагноение раны |
– |
1 (11,1%) |
– |
1 (3,1%) |
– |
|
|
Серома п/к клетчатки |
2 (10,5%) |
1 (11,1%) |
– |
3 (9,4%) |
1 (4,0%) |
|
|
Гематома |
1 (5,3%) |
– |
– |
1 (3,1%) |
– |
|
|
Поздние |
4 (21,1%) |
4 (44,4%) |
2 (50,0%) |
10 (31,3%) |
4 (16,0%) |
|
|
Рецидив грыжи |
1 (5,3%) |
– |
1* (25,0%) |
2 |
– |
|
|
Болевой синдром |
– |
– |
1** (25,0%) |
1 |
– |
|
|
Ограничение подвижности |
2 (10,5%) |
– |
1** (25,0%) |
3 |
– |
|
|
Ощущение инородного тела |
1 (5,3%) |
– |
1** (25,0%) |
2 |
2 (8,0%) |
|
|
Свищи |
– |
1 (11,1%) |
– |
1 |
– |
|
|
Косметические дефекты |
– |
3 (33,3%) |
– |
3 |
2 (8,0%) |
|
Примечания: * – рецидив грыжи возник у больного с развившимся АКС, который потребовал декомпрессивных мероприятий в виде повторного оперативного вмешательства и удаления сетчатого эндопротеза; ** – все 3 осложнения диагностированы у 1 пациента.
Образование серомы отмечено только у 1 (4%) пациента. Умер 1 (4,0%) больной от двусторонней пневмонии и острого нарушения мозгового кровообращения в бассейне средней мозговой артерии.
За всеми больными обеих групп осуществлялось наблюдение в течение 1 года после операции. В контрольной группе у 1 (3,1%) пациента, которому в раннем послеоперационном периоде было выполнено вынужденное удаление сетчатого аллотрансплантата, отмечено закономерное формирование грыжи, еще у 1 (5,3%) после пластики «on-lay» диагностирован рецидив грыжи на фоне смещения и сморщивания эндопротеза. Общая частота рецидивов грыжи в контрольной группе через год после операции составила 6,3%. У больных основной группы в течение года наблюдения после операции рецидив грыжи отмечен в 1 (1,8%) случае.
Выполнение герниолапаротомии и пластики дефекта мышечно-апоневротического каркаса передней брюшной стенки в экстренном порядке у больных сбольшими и гигантскими ПОВГпредставляется сложной тактической и технической задачей. Такие операции выполняются по поводу острой спаечной кишечной непроходимости в грыжевом мешке или ущемления грыжи и должны преследовать достижение двух целей. Первая из них – это спасение жизни пациента в ургентной ситуации, вторая – надежное устранение грыжевого дефекта.
Наличие у большинства пациентов с большими и гигантскими ПОВГ ситуации «потери домена», сопутствующего ожирения и выраженной коморбидностиопределяет повышение уровня внутрибрюшного давления даже при отсутствии острой абдоминальной хирургической патологии. Развивающаяся непроходимость в грыжевом мешке или ущемление грыжи, а также паралитическая послеоперационная кишечная непроходимость значительно усугубляют ситуацию и могут привести к развитию синдрома абдоминальной компрессии, полиорганной недостаточности и смерти больного в раннем послеоперационном периоде. Проведение сепарационных видов пластик и пластик типа «sublay» и «on-lay» приводит к значительному приросту показателей внутрибрюшного давления более чем на 80% от исходных. Именно у этих пациентов в раннем послеоперационном периоде отмечались такие осложнения, как пневмония и развитие синдрома абдоминальной компрессии с полиорганной недостаточностью. Наиболее выгодной в плане профилактики послеоперационной внутрибрюшной гипертензией выглядит пластика типа «bridge», но она, также как и пластика «on-lay», предполагает поверхностное расположение сетчатого эндопротезаи его контакт с подкожной жировой клетчаткой. В этих случаях закономерно повышается частота ранних раневых осложнений в виде образования сером в подкожной клетчатке и нагноений послеоперационной раны.
Предложенный авторами метод по своей сути является пластикой типа «bridge», но он лишен недостатка в виде контакта эндопротеза с подкожной жировой клетчаткой. При сопоставимых уровнях повышения внутрибрюшного давления совместно с другими способами пластики типа «bridge» и «on-lay» применение данного метода позволило достоверно снизить частоту раневых осложнений в раннем послеоперационном периоде.
Заключение
Вопросы выбора оптимального метода экстренной герниопластики у больных с большими и гигантскими ПОВГ в настоящее время окончательно не решены. Наибольшую проблему представляет внутрибрюшная гипертензия, которая имеет место до операции, увеличивается при кишечной непроходимости и в ответ на хирургическую агрессию. Применение предложенного способа герниопластикибольших и гигантских ПОВГ в экстренном порядке у больных с ущемлениями грыж и спаечной кишечной непроходимостью в грыжевом мешке позволило добиться приемлемых показателей внутрибрюшного давления в раннем послеоперационном периоде, уменьшения выраженности болевого синдрома и предотвращения развития синдрома абдоминальной компрессии за счет полного отсутствия натяжения, а также снижения частоты раневых осложнений из-за отсутствия контакта эндопротеза с подкожной жировой клетчаткой.



