Основным методом лечения пациентов с послеожоговыми рубцовыми стриктурами пищевода является бужирование пищевода по струне-направителю, что способствует улучшению непосредственных результатов и снижению числа осложнений при выполнении данной процедуры щевода составляет от 20 до 40%, что заставляет задуматься об усовершенствовании хирургической тактики или иных методах лечения [5].
Стоит отметить, что открытая хирургия у данной группы пациентов отличается значительной трудоемкостью и высоким риском осложнений. Несостоятельность швов отмечается в 12–54,6% случаев, развитие рубцовых стриктур пищеводно-кишечных анастомозов – в 9–19,6% случаев после завершенного лечения [6]. Методика интрамурального введения стероидов при лечении послеожоговых рубцовых стриктур пищевода для улучшения результатов лечения и снижения послеоперационных рестенозов применяется более 30 лет [7].
Для внутристеночного введения используют преднизолон, метилпреднизолон, триамцинолон, кеналог и другие препараты. Отечественные авторы свидетельствуют о высокой эффективности внутристеночных инъекций триамцинолона при бужировании сложных рестнозирующих, рецидивирующих и рефрактерных стриктур пищевода. Осложнений при терапии стероидами авторы не наблюдали, а побочные явления были незначительными и не влияли на работу пищевода [8, 9].
Согласно проведенному систематическому обзору, состоявшему из 4 рандомизированных и 2 когортных исследований, 6 серий случаев, включавших в себя 341 больного с доброкачественными стриктурами пищевода, отмечены преимущества добавления внутристеночной инъекции стероидов с последующим бужированием [10]. Эндоскопические способы лечения стриктур пищевода остаются методом первой линии при оказании помощи пациентам указанной группы, отмечаются их высокая эффективность и безопасность. При использовании бужирования пищевода с внутристеночным введением стероидов осложнения были редкими и имели низкую степень тяжести [10].
Цель исследования: ретроспективно проанализировать собственный опыт применения внутристеночных инъекций бетаметазона при лечении пациентов с рубцовыми послеожоговыми стриктурами пищевода
Материалы и методы исследования
Временной период исследования составил 15 лет (с 2007 по 2022 гг.). Все пациенты проходили лечение в отделении торакальной хирургии ГОБУЗ «Новгородская областная клиническая больница», всего методикой комбинированного лечения (внутристеночное введение бетаметазона с последующим бужированием пищевода) были пролечены 36 человек с рубцовыми стриктурами пищевода.
Основным методом при лечении пациентов с доброкачественными послеожоговыми стриктурами пищевода, применяемым в ГОБУЗ «Новгородская областная клиническая больница» (клиническая база кафедры госпитальной хирургии Новгородского государственного университета имени Ярослава Мудрого (ФГБОУ ВО НовГУ им. Ярослава Мудрого)), является бужирование по струне-направителю.
Осуществлен ретроспективный анализ медицинских карт пациентов, которым в дополнение к проведению бужирования пищевода осуществлялось внутристеночное введение препарата бетаметазон.
Исследование одобрено локальным этическим комитетом (протокол заседания локального этического комитета ФГБОУ ВО НовГУ им. Ярослава Мудрого № 2 от 28.02.2023 г.). Все пациенты перед проведением манипуляции подписывали добровольное медицинское согласие.
Критерии включения в исследование:
- согласие пациента на внутристеночное введение бетаметазона с последующим бужированием пищевода бужами типа Savary как основным методом лечения;
- подтвержденный рестеноз пищевода после ранее проведенного бужирования (бужирований);
- наличие стеноза пищевода III (3–5 мм) и IV (0–2 мм) степени по классификации Ю.И.Галлингера и Э.А. Годжелло.
Для исследования из 36 человек были отобраны 30 пациентов. Исключены 6 больных с пептическими стриктурами на фоне протекающего рефлюкс-эзофагита. Всем пациентам перед проведением бужирования выполнялась рентгеноскопия и/или рентгенография пищевода с использованием жидкой бариевой взвеси.
Тактика бужирования пищевода с предшествующим выполнением внутристеночных инъекций бетаметазона в нашем стационаре стандартна: пациенту проводится интраоперационная фиброгастродуоденоскопия (ФГДС), по ходу пищевода под контролем эндоскопа устанавливается струна-проводник. После позиционирования эндоскопа и визуализации участка максимального стеноза выполняются подслизистые инъекции бетаметазона 1,0 мл. Игла вводилась по каналу эндоскопа. Инъекции осуществляются через 2 вкола на 12 и 6 часов или 3 и 9 часов по циферблату соответственно. Выполняется эндоскопический контроль области вколов с целью выявления возможных осложнений (кровотечения и перфорации). После инъекций далее по струне-направителю проводится бужирование пищевода бужами типа Savary от № 12 до 40 Fr. По окончании манипуляций производится визуальная оценка при помощи эндоскопа, также исключались осложнения (перфорации и значимые кровотечения). Визуализация пищевода и послеоперационный контроль бужирования выполняются с использованием видеогастроскопа «Pentax-2990К» (Pentax Medical, Япония).
Количество мужчин и женщин в исследуемой группе составляло 70% (n=21) и 30% (n=9) соответственно. Минимальный возраст пациентов – 22 года, максимальный – 77 лет. Средний возраст 51,92±13,03 года. Средний срок возникновения рестеноза – 8 месяцев.
Все пациенты при госпитализации предъявляли жалобы на дисфагию.
Стеноз пищевода III степени присутствовал у 27 пациентов (90%), IV степени выявлен у 3 пациентов (10%).
Всем пациентам в исследуемой группе ранее уже был выполнен как минимум один сеанс бужирования пищевода, и больные повторно обратились с клинической картиной рестеноза.
Основными химическими агентами, прием которых привел к формированию стриктуры пищевода, являлись неизвестная жидкость (n=11), уксусная кислота (n=6), суррогаты алкоголя (n=6), щелочи (n=3), у 4 человек причинами ожогов явились иные жидкости (бензин, нашатырный спирт, ацетон).
При обследовании пациентов перед проведением планового оперативного лечения были выявлены различная сопутствующая патология (табл. 1) и отклонения в лабораторных показателях и на ЭКГ (табл. 2).
Таблица 1
Сопутствующая патология у пациентов в исследуемой группе (n=30)
|
Нозологическая форма |
Абс. |
% |
|
Язвенная болезнь желудка и/или 12-перстной кишки |
6 |
20 |
|
Гипертоническая болезнь |
4 |
13,3 |
|
Хронический гепатит / цирроз печени |
2 |
6,7 |
|
Ишемическая болезнь сердца (ИБС), постинфарктный кардиосклероз (ПИКС), нарушения ритма сердца |
5 |
16,7 |
|
Сахарный диабет |
2 |
6,7 |
Среди сопутствующих заболеваний превалировала кардиальная патология (гипертоническая болезнь и различные формы ИБС), которая была выявлена у 30% больных, что является предсказуемым, учитывая возраст исследуемых. Патология желудочно-кишечного тракта обнаружена у 26,7% пациентов, что часто объяснялось злоупотреблением алкоголем и его суррогатами.
Таблица 2
Отклонения лабораторных показателей и ЭКГ в исследуемой группе (n=30)
|
Лабораторный показатель |
Абс. |
% |
|
Протеинурия |
6 |
20 |
|
Железодефицитная анемия |
7 |
23,3 |
|
Гипербилирубинемия |
3 |
10 |
|
Гипопротеинемия |
9 |
30 |
|
Повышение уровня АЛТ, АСТ |
12 |
40 |
|
Лейкоцитоз, повышение уровня СОЭ |
4 |
13,3 |
|
Нарушения ритма и проводимости (ФП, АВ-блокада, СССУ) |
5 |
16,7 |
|
Гепатит С (HCV) |
1 |
3,3 |
Таким образом, у 9 пациентов (30%) наблюдалось присутствие в биохимическом анализе крови гипопротеинемии, признаки железодефицитной анемии – у 7 человек (23,3%), что свидетельствует о белково-энергетической недостаточности в указанной группе. У 16 больных (53,3%) выявлены показатели, указывающие на патологию желудочно-кишечного тракта (гипербилирубинемия, повышение уровня трансаминаз, гепатит С).
Результаты исследования и их обсуждение
Средняя длительность госпитализации больных составила 8,62±3,21 дня.
Локализация уровня сужений пищевода (верхняя треть (в/3), средняя треть (с/3), нижняя треть (н/3) и протяженность стриктур (одиночные, множественные) указана в таблице 3.
Таблица 3
Характеристика пациентов по степени стеноза пищевода и уровню поражения
|
Общее число наблюдений (n=30) |
||||
|
Уровень поражения и количество стриктур |
Стеноз пищевода III степени (n=27) |
Стеноз пищевода IV степени (n=3) |
||
|
|
Абс. |
% |
Абс. |
% |
|
Стриктура пищевода в в/3 |
12 |
44,4 |
2 |
66,7 |
|
Стриктура пищевода в с/3 |
11 |
40,7 |
1 |
33,3 |
|
Стриктура пищевода в н/3 |
4 |
14,8 |
0 |
0 |
|
Одиночные стриктуры |
23 |
85,2 |
3 |
100 |
|
Множественные стриктуры |
4 |
14,8 |
0 |
0 |
В большинстве случаев (90%) наблюдалась обращаемость пациентов со стенозом пищевода III степени. Чаще встречались пациенты с локальными (одиночными) стриктурами, захватывающими верхнюю и среднюю трети пищевода.
Среднее время проведения оперативного лечения (инъекции бетаметазона и последующее бужирование) составило 32±11,3 минуты.
У 12 пациентов (40%) до проведения комбинированной методики лечения уже имела место однократная госпитализация с проведенным бужированием по струне-направителю, 12 больных (40%) ранее проходили лечение не менее трех раз, 6 пациентов (20%) были госпитализированы 4 раза и более до момента прохождения комбинированной методики лечения.
Результаты основных этапов комбинированного метода лечения послеожоговых стриктур пищевода представлены на рисунке.
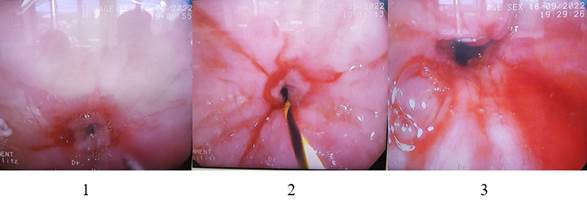
Одиночная стриктура с/3 пищевода IV степени: 1 – эндоскопическая картина до лечения; 2 – установлена струна-проводник, выполнены интрамуральные инъекции бетаметазона; 3 – просвет пищевода после проведенного бужирования
Сроки возникновения рестеноза до госпитализации с целью проведения комбинированной методики лечения, потребовавшего повторной госпитализации, варьировались в пределах от 20 дней до 6 лет (средний срок 8 месяцев). Частота повторных госпитализаций составляла от 1 до 6 в год (в среднем 2,6 в год).
Летальных исходов за время стационарного лечения не наблюдалось.
Эрозивный эзофагит после проведенного бужирования был выявлен у 4 (14,8%) пациентов в группе со стенозом пищевода III степени и у 1 (33,3%) больного со стенозом пищевода IV степени. Перфорация пищевода струной подтверждена у 1 (3,7%) пациента со стенозом пищевода III степени. Перфорации (разрывы) пищевода бужом, формирование «ложного хода», кровотечения, микоз пищевода в исследуемых группах не зарегистрированы.
Перфорация пищевода струной (n=1) не потребовала хирургического лечения, на контрольном осмотре через 3 дня выявлен формирующийся точечный рубец в месте перфорации, на контрольной ФГДС через 7 дней дефекта в пищеводе не обнаружено.
Клиническая картина эрозивного эзофагита купирована у всех больных, на контрольных ФГДС признаков эрозий не зарегистрировано.
У 5 пациентов (16,7%) было отмечено формирование умеренных подслизистых гематом в месте проведения инъекций. Всем указанным пациентам была выполнена контрольная ФГДС спустя 5–7 дней. Эндоскопическая картина соответствовала гематоме в стадии обратного развития (лизиса).
У 3 (10%) пациентов, которые были госпитализированы повторно с клинической картиной рестеноза, на ФГДС наблюдались локальные точечные или линейные рубцы в местах ранее выполненных инъекций бетаметазона с последующим бужированием. Все послеинъекционные рубцы являлись локальными, не стенозировали просвет пищевода.
Оценка результатов лечения комбинированным методом проведена по двум критериям: отсутствие явлений дисфагии и восстановление проходимости пищевода, которое оценивалось по его диаметру после бужирования. В исследуемой группе диаметр пищевода после завершенного лечения составлял от 9 мм до 22 мм (в среднем 15 мм).
У одного пациента с множественными стриктурами в с/3 и н/3 пищевода удалось добиться дилатации пищевода до 9 мм (буж 28 Fr), однако в последующем потребовались повторные госпитализации. В общей сложности выполнено 9 сеансов бужирования, первый из которых был проведен спустя 34 дня после оконченного случая лечения комбинированным методом. Еще у одного пациента, имевшего протяженную одиночную стриктуру со стенозом пищевода IV степени, удалось добиться дилатации пищевода до 10 мм, однако из-за рестеноза потребовались повторные госпитализации для проведения сеансов бужирования. Всего было выполнено 6 сеансов бужирования, первый из которых был выполнен спустя 23 дня после оконченного случая лечения комбинированным методом.
У 28 пациентов (93,3%) диаметр пищевода после проведенного бужирования составлял от 11 до 22 мм (30–36 Fr соответственно). После завершения лечения комбинированным методом самый ранний срок обращения за выполнением повторного бужирования составил 6 месяцев.
После завершенного курса лечения комбинированным методом (интрамуральные инъекции бетаметазона + бужирование пищевода) 26,7% (n=8) больным не понадобилась повторная госпитализация с целью бужирования, указанные пациенты после выписки из стационара за медицинской помощью не обращались. После оконченного комбинированного лечения 33,3% (n=10) больным потребовалась однократная госпитализация, 26,7% (n=8) проводилось 2 госпитализации, 13,3% (n=4) трижды и более были госпитализированы с целью повторного бужирования пищевода по поводу его рестеноза.
Тактика лечения больных с доброкачественными послеожоговыми рубцовыми стриктурами пищевода достаточно четко отработана при лечении их в стационарных условиях ГОБУЗ «Новгородская областная клиническая больница». При наличии у пациента протяженных или рефрактерных стенозов перспективной является методика внутристеночных инъекций гормональных препаратов. Для введения используют преднизолон, метилпреднизолон, дексаметазон, триамцинолон. Согласно исследованиям, данные препараты за счет своего механизма действия (противовоспалительный и противоотечный) оказывают влияние на рубцовую ткань, делая стриктуру менее ригидной и плотной, облегчая процесс бужирования [11, 12]. Отечественные авторы при бужировании сложных рестнозирующих, рецидивирующих стриктур пищевода используют дексаметазон или триамцинолон [7-9].
В клинической практике авторы статьи активно используют препарат бетаметазон (Дипроспан). Препарат является глюкокортикостероидом, подавляет функции лейкоцитов (адгезия, активность) и тканевых макрофагов, снижает концентрацию протеолитических ферментов в области воспаления, угнетает активность фибробластов и образование коллагена. Терапевтическая активность бетаметазона обусловлена противовоспалительным, противоаллергическим и антиэкссудативным действием, сопоставимыми с действием дексаметазона и триамцинолона. По противовоспалительной активности дипроспан превышает гидрокортизон в 30 раз, однако при этом не обладает минералокортикоидной активностью. При повторном бужировании стриктур пищевода у пациентов, которым ранее было проведено лечение комбинированной методикой, авторами статьи было отмечено, что рубец становится менее ригидным (выраженный противовоспалительный и противоотечный механизм действия бетаметазона). Это проявляется в облегчении процесса бужирования, ощущении меньшего сопротивления при проведении бужа (в том числе большего диаметра), более быстром прохождении участка стеноза и уменьшении продолжительности операции.
По мнению авторов статьи, использование комбинированной методики лечения (внутристеночное введение бетаметазона с последующим бужированием пищевода) позволяет уменьшить количество бужирований и повторных госпитализаций у конкретного пациента, ускорить время проведения операции за счет влияния дипроспана на рубцовую ткань (снижение плотности и ригидности стриктуры).
Заключение
Показанный авторский 15-летний опыт лечения пациентов комбинированной методикой при наличии у пациента послеожоговых рубцовых стенозов пищевода является перспективным. Стоит учитывать тот факт, что для лечения были отобраны больные с рецидивирующими или рефрактерными стенозами, что говорит о необходимости длительной терапии указанным пациентам, наличии технических сложностей при их лечении. Однако при оказании помощи таким пациентам авторы статьи придерживаются тактики «самый плохой собственный пищевод лучше любого искусственного», тем самым максимально пролонгируются малоинвазивные методы лечения. Стоит отметить, что количество осложнений при выполнении комбинированной методики является минимальным, а также отсутствуют системные изменения и случаи летального исхода, что может говорить о перспективах дальнейшего развития данного варианта лечения в дополнение к стандартному бужированию пищевода по классическим способам и внедрения его в общую клиническую практику.



