Лечение заболеваний слизистой оболочки рта, в частности стоматитов различной этиологии, продолжает оставаться одним из наиболее сложных и важных разделов современной стоматологии. Высокая и неуклонно растущая заболеваемость населения страны острым (первичным) стоматитом является актуальной проблемой современной медицины, несмотря на многочисленные исследования в этой области. По данным Рыбакова А.И., в 1978 г. распространенность стоматита среди населения нашей страны составляла 5% от всех воспалительных заболеваний слизистой оболочки полости рта, а в настоящее время доля стоматита занимает около 53% [1; 2]. Понятие «стоматит» достаточно широкое. Из стоматологических заболеваний, наверное, ни одно не имеет столь разнообразного проявления и такого обширного количества причин, как стоматит. В зависимости от повреждающего фактора различают около 10 видов стоматитов, имеющих как общие, так и специфические симптомы. Однако причины возникновения стоматита могут быть объединены в следующие группы: травмы, инфекционные агенты, аллергия, системные заболевания. Сложность лечения заключается как в разнообразии факторов, вызывающих развитие данного заболевания, так и в возможности сочетания нескольких факторов, что ведет к изменению вида заболевания или хронизации процесса. Применяемые в настоящее время медикаментозные средства в лечении стоматита не дают желаемый результат, следовательно, необходимо искать и апробировать новые и эффективные препараты.
Наиболее сложно поддаются лечению бактериальные стоматиты. Они вызваны травмами слизистой оболочки рта, наличием кариозных полостей в зубах, нарушением правил асептики и антисептики во время стоматологических манипуляций и хирургических вмешательств. Золотистый стафилококк – основной представитель данной группы, вызывающий стоматиты бактериальной природы. Благодаря высокой резистентности микроба к антибактериальным препаратам, заболевания стафилококковой этиологии занимают ведущее место среди всей гнойно-воспалительной патологии. Известно, что многие штаммы Staphylococcus aureus обладают сниженной чувствительностью к метициллину и ванкомицину, это делает терапию стафилококковых инфекций в некоторых ситуациях достаточно проблематичной [3]. Увеличение числа больных с инфекционными заболеваниями полости рта повысило интерес к пробиотическим препаратам, которые, в отличие от лекарственных средств, восстанавливают собственную микрофлору, не нанося ей вреда. Лактобациллы обладают наибольшей антагонистической активностью по отношению к патогенной и условно-патогенной микрофлоре, обеспечивая устойчивость слизистых оболочек организма к колонизации аллохтонной микрофлорой в желудочно-кишечном тракте. В связи с этим является актуальным создание и внедрение в медицину высококачественных пробиотиков на основе региональных биовариантов лактобацилл, выделенных от здоровых людей [4]. Экспериментальные модели, в частности бактериальных стоматитов, позволяют оценить эффективность применения новых способов лечения инфекционно-воспалительных процессов ротовой полости различной этиологии.
Цель работы: охарактеризовать гистологическую картину стоматита в эксперименте на белых крысах и оценить эффективность использования высокоактивных культур лактобацилл для его лечения.
Материал и методы. Эксперимент проводился на 32 самках беспородных белых крыс массой 230 г, в течение 12 дней в 3 этапа. Содержание, питание, уход за животными и выведение их из эксперимента осуществляли в соответствии с требованиями «Правил проведения работ с использованием экспериментальных животных» (Приложение к Приказу МЗ СССР от 12.08.1977 № 755). Все животные содержались при сходных условиях в отношении температуры, влажности и освещения, а также рациона питания (комбикорм ПК-120-1, Россия). На проведение экспериментов получено разрешение этического комитета ГБОУ ВПО «Тверская ГМА» Минздрава РФ (протокол от 14 октября 2013 г.). Первый этап эксперимента: создание химической модели стоматита у всех животных путём ежедневной на протяжении 3 дней обработки ротовой полости 9%-ной уксусной кислотой (УК) [5]. Второй этап: на четвёртые сутки создание биологической модели стоматита на базе химической на всех крысах путём однократной обработки ротовой полости культурой Staphylococcus aureus, выделенной от клинически здоровых детей и подростков г. Твери и Тверской области. Третий этап: спустя сутки лечение стоматита, отягощённого бактериальной инфекцией, путём двукратной в течение 7 дней обработки ротовой полости опытных крыс культурами 3 видов Lactobacillus (Lactobacillus 11 зв., Lactobacillus 2 п. рта, Lactobacillus 24 д. ст. и их комбинации). Эти штаммы лактобацилл, выделенные из полости рта здоровых людей, обладают высокими показателями адаптационного и пробиотического потенциала, в том числе активностью по отношению к патогенным и условно-патогенным микроорганизмам в экспериментах in vitro [6]. На третьем этапе все крысы были разделены на 5 серий: 1 – без лечения (контрольная), 2 – лечение Lactobacillus 11 зв. (опытная № 1), 3 – лечение Lactobacillus 2 п. рта (опытная № 2), 4 – лечение Lactobacillus 24 д. ст. (опытная № 3), 5 - лечение комбинацией всех трех культур лактобацилл (опытная № 4).
На 1, 3, 5, 6, 9 и 12-й день эксперимента под общим ингаляционным эфирным наркозом проводили забор биоптатов (десна) для гистологического исследования. После этого животные выводились из эксперимента передозировкой паров эфира. Изготовление гистологических препаратов проводилось по стандартной методике, включающей фиксацию небольших кусочков материала в 12%-ном фосфатно-буферном растворе формалина на протяжении 24 ч., промывание в воде в течение суток и заливку в парафин. Парафиновые срезы, полученные на микротоме HESTION ERM 3100 (HESTION, Австралия - Китай), обрабатывали в три этапа: депарафинирование, окрашивание гематоксилин-эозином и обезвоживание срезов с последующим заключением в бальзам [7]. Полученные срезы исследовали с использованием светового микроскопа Olympus CX21 (Olympus Corporation, Китай) c встроенной фотокамерой МС 10 (АО «ЛОМО», Россия) и комплекса визуализации МС (система фото- и видеодокументирования на базе цифровой видеокамеры). Обработка данных осуществлялась на компьютерной программе MCview (базовое программное обеспечение фотокамеры).
Результаты исследования и их обсуждение. До начала эксперимента были осмотрены слизистые оболочки ротовой полости всех животных, никаких признаков воспаления обнаружено не было. Слизистая оболочка без видимых патологических изменений, не кровоточащая, влажная, бледно-розового цвета. На гистологических микропрепаратах слизистой оболочки десны интактных крыс картина соответствует норме: эпителий без признаков повреждения, в рыхлой волокнистой соединительной ткани собственной пластинки слизистой встречаются отдельные лимфоциты, плазматические клетки и редкие макрофаги, очаги воспаления не выявлены (рис. 1а).
На 4-е сутки эксперимента (после 3 дней применения кислоты) у всех крыс в ротовой полости была отмечена выраженная гиперемия, отёк слизистой оболочки десны. На микропрепаратах - стаз крови в некоторых сосудах микроциркулярного русла, инфильтрация собственной пластинки слизистой нейтрофильными лейкоцитами (рис. 1б). Примерно у половины опытных животных зафиксировано наличие очаговых поражений полости рта в виде афт и язв, а также петехий, вследствие разрушения поверхностных слоёв слизистой оболочки. У отдельных крыс на фоне указанных изменений появились признаки ангулярного хейлита, начали формироваться гнойные очаги [8].
Спустя сутки после обработки ротовой полости крыс культурой Staphylococcus aureus (на 5-е сутки эксперимента) развился бактериальный стоматит. Об этом свидетельствуют как внешние признаки воспалительного процесса, так и микроскопические [9]. При осмотре десен у всех крыс было выявлено нарастание признаков воспаления слизистых покровов: выраженная гиперемия и отёк, петехии, сформированные гнойные очаги. У многих животных значительно увеличивается объём лейкоцитарного инфильтрата, который трансформируется в гнойный мешок в виде валика в области резцовой части десны нижней челюсти, также стаз крови в сосудах микроциркулярного русла. На гистологических микропрепаратах визуализируются разрозненные клетки поверхностного слоя эпителия и более глубоко лежащих его слоёв, а также разрушение клеток, лейкоцитарная инфильтрация подлежащих тканей и кровоизлияния (рис. 1в).
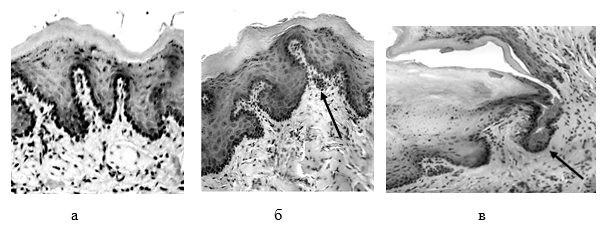
Рис.1 Десна крысы. Окраска гематоксилин – эозином. Ув. х 400
А — интактная; Б – после воздействия уксусной кислоты; скопление макрофагов, нейтрофилов, тучных клеток под базальной мембраной (стрелка);
В – после обработки культурой Staphylococcus aureus, разрыхление и нарушение целостности эпителия (стрелка)
На 6-е сутки (через день после обработки культурами Lactobacillus) и вплоть до окончания эксперимента наблюдалась картина постепенного «возвращения» слизистых покровов десен большинства крыс к интактному состоянию. При визуальном осмотре обнаруживалось уменьшение отечности мягких тканей десны и объема гнойных валиков, снижение числа гнойных очагов и язв в полости рта до полного их исчезновения. Выявлено постепенное восстановление поверхностного эпителиального слоя, а также более глубоко расположенных его слоёв, снижение концентрации нейтрофилов, плазматических клеток, макрофагов под базальной мембраной до отдельно встречающихся клеток (рис. 2а).
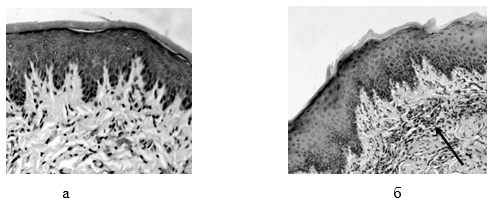
Рис. 2 Десна крысы на 12 – й день эксперимента. Окраска гематоксилин – эозином. Ув. х 400. А – 7-е сутки лечения культурой Lactobacillus 11 зв., отдельные макрофаги и нейтрофилы под базальной мембраной; Б – контроль, нейтрофильная инфильтрация (стрелка)
У крыс контрольной серии, которые были обработаны УК и Staphylococcus aureus, но не подвергались лечению культурами Lactobacillus, воспалительный процесс слизистой оболочки рта имел те же проявления, что и у животных опытных серий. Однако, в отличие от них, клиническая картина была ярче: на гистологических препаратах отмечалось разрыхление и нарушение целостности эпителиального слоя. По времени воспалительный процесс длился дольше, и к 12-му дню у половины животных фиксировались его признаки, на микропрепаратах – нейтрофильная инфильтрация (рис. 2б). В опытных сериях к окончанию эксперимента, напротив, в 100% случаев признаки воспаления ни визуально, ни на микропрепаратах обнаружены не были.
На базе созданной нами биологической модели стоматита были получены данные, которые позволяют оценить эффективность его лечения у крыс высокоактивными штаммами лактобацилл. Культуры лактобацилл прежде всего оказывают влияние на Staphylococcus aureus, как основную причину развития бактериального стоматита.
Анализ литературы показывает, что, несмотря на различные инициальные моменты развития стоматита, гистологические изменения в слизистой оболочке полости рта при эрозивно-язвенной стадии заболевания схожи (А.А. Спасов, 2006 г.; А.А. Ярцева, 2014 г.; И.В. Ковач, 2015 г.; А.Ю. Нассонов, 2016 г.) [10-13]. В своей работе А.А. Спасов воспроизводил термический ожог слизистой оболочки полости рта в области верхних резцов кроликов породы шиншилла путем нанесения раскаленного докрасна штопфера. Через сутки объективно отмечали нарастание воспалительной реакции - отечности, гиперемии, инфильтрации окружающих тканей, нагноения ран. Обращало на себя внимание наличие воспалительного инфильтрированного краевого валика. На 11-13-е сутки эксперимента клинически отмечали снижение отечности, гиперемии, инфильтрации окружающих тканей [10]. В нашем эксперименте мы наблюдали те же признаки воспаления с образованием гнойных мешков в виде валика в области резцовой части десны. В эксперименте А.Ю. Нассонова показана гистологическая картина при травматическом стоматите у белых крыс. Травма наносилась путем поверхностного линейного разреза на десневой поверхности. На 3-и сутки в очаге поражения в подэпителиальном слое десны определялись плотные воспалительные инфильтраты, представленные лимфоцитами, гистиоцитами и нейтрофилами, единичными тучными клетками и эозинофилами, стаз эритроцитов в некоторых сосудах микроциркулярного русла. На 5-е сутки эксперимента гистологическая картина биоптатов свидетельствовала о том, что в тканях сохранялись экссудативно-некротические процессы. Определялись отек, нарушения кровообращения в виде полнокровия, стаза, присутствовали кровоизлияния. На 10-е сутки исследования определялись регенераторные процессы, но воспалительный инфильтрат сохранялся. К 14-му дню эксперимента эпителизация была завершена [13].
Заключение. Таким образом, полученные нами результаты согласуются с данными других авторов. А.А. Спасов и А.Ю. Нассонов описали такие же изменения клинической и гистологической картины слизистой оболочки десны в соответствующие сроки. Однако в доступной литературе описаны травматические модели стоматита. В нашем эксперименте воздействие УК на слизистую десны было усилено культурой Staphylococcus aureus. Объективно проявления стоматита были выражены ярче, что максимально приблизило модель к реальной клинической картине, так как данное заболевание нередко сопровождается бактериальной инфекцией.
Исследования, связанные с моделированием стоматита, ведутся давно, но изучение морфогенеза экспериментального стоматита остается актуальной проблемой и в настоящее время. В результате работы многих авторов были созданы различные лекарственные препараты, разработаны методики, успешно применяемые для лечения данного заболевания, однако поиски более эффективных средств продолжаются.
Библиографическая ссылка
Ганина Е.Б., Червинец Ю.В., Шестакова В.Г., Грудинин Н.В., Кузнецова В.С., Прутенская Е.А. ГИСТОЛОГИЧЕСКАЯ КАРТИНА СТОМАТИТА В ЭКСПЕРИМЕНТЕ НА КРЫСАХ // Современные проблемы науки и образования. 2017. № 5. ;URL: https://science-education.ru/ru/article/view?id=26783 (дата обращения: 22.03.2026).



