Трудности лечения посттравматических деформаций пальцев, нередко сопровождающихся развитием фиброзных анкилозов в проксимальных межфаланговых суставах, определяются необходимостью одновременного устранения деформации пальца и восстановления подвижности суставов для осуществления функции кисти. С этой целью в настоящее время широко используется подход, когда на первом этапе осуществляется наложение чрескостного аппарата и проводится постепенное расширение суставной щели, а затем, после снятия аппарата, выполняется артропластика с удалением внутрисуставных образований, препятствующих движению. Однако при выполнении артропластики возникают определенные технические трудности, обусловленные особенностями анатомического строения сустава (небольшие размеры суставных концов, малый объем суставной полости, незначительная толщина жировой клетчатки), что повышает риск развития осложнений. У многих больных в послеоперационном периоде наблюдается «потеря» активных движений в суставе.
Развитие и внедрение в практику клеточных технологий открывает новые перспективы в использовании сочетанного применения метода дистракции и клеточных субстанций, обладающих хондрогенной и остеогенной активностью у пострадавших с последствиями травм кисти. О первых обнадеживающих результатах подобной методики сообщают А.А. Богов с соавторами [1].
Цель исследования – предложить вариант использования клеточных технологий в лечении фиброзных анкилозов проксимального межфалангового сустава пальцев кисти.
Материал и методы исследования
В исследование включено 46 пациентов (16 женщин и 30 мужчин), поступивших на оперативное лечение с диагнозом фиброзный анкилоз проксимального межфалангового сустава. Наличие фиброзного анкилоза подтверждалось данными клинического (отсутствие активных и пассивных движений в суставе) и рентгенологического (отсутствие или резкое снижение суставной щели) обследований. В анамнезе у девяти больных были выявлены переломы (в том числе внутрисуставные) фаланг пальцев, у трех – вывихи средней фаланги, у одного – подкожный разрыв сухожилия разгибателя. Открытые сочетанные травмы нескольких структур кисти имели место у пяти пациентов. У 23 больных были диагностированы ушибы пальцев. Анкилоз проксимального межфалангового сустава только одного пальца были выявлен у 40 человек, двух пальцев – у пяти, четырех – у одного. По частоте поражения пальцев распределение было следующее: II палец – 9 случаев, III – 15, IV – 19, V – 11. Преимущественно страдала правая кисть (29 человек). Причиной обращения в специализированное отделение хирургии кисти была деформация травмированного пальца, которая приводила к нарушению функции кисти и не позволяла пациенту выполнять свои профессиональные или бытовые обязанности. Все пациенты были трудоспособного возраста (от 18 до 55 лет, средний – 37,4).
Всем пациентам на первом этапе был наложен чрескостный аппарат «Ellis Mini-Fixateur» с целью расширения суставной щели до 10–12 мм и выведения пальца в функционально выгодное положение (темп дистракции – 0,5 мм в сутки). На втором этапе производили снятие чрескостного аппарата и мобилизацию сустава. Восстановление полного объема пассивных движений в суставе проверялось на операционном столе и было достигнуто во всех случаях.
Состояние функции кисти оценивали, используя DASH-опросник и авторский [2].
Для проверки выдвигаемых гипотез использовали методы непараметрической статистики. Уровень статистической значимости принят равным 0,05. Описание данных приведено средним и стандартным отклонением.
Результаты и обсуждение
При обследовании до операции средние значения по DASH-опроснику составили 38,0±3,2 балла, по авторскому опроснику – 66,2±3,0 балла, что объективно подтверждало нарушение функции кисти. Степень функциональных нарушений зависела от количества поврежденных пальцев. При повреждении одного пальца суммы баллов по опросникам составили соответственно 35,2±3,3 и 68,0±3,1, а при повреждении нескольких пальцев – 53,5±7,0 и 56,3±8,5 (p<0,05).
При контрольном осмотре 35 пациентов через три месяца после артропластики установлено, что ни у одного из них не было полного восстановления амплитуды активных движений в проксимальном межфаланговом суставе. Дефицит активного разгибания составлял в среднем 40,0±12,5°. Данные DASH-опросника – 26,4±3,5 баллов и нашего опросника – 82,0±3,5 балла, что свидетельствовало о положительной динамике, но не о полном восстановлении функции.
После выписки из стационара реабилитационные мероприятия в условиях поликлиники не проводились. Лишь 18 пациентов регулярно занимались гимнастикой самостоятельно.
Таким образом, применение дистракционного метода с последующей артропластикой «в чистом виде» не решает в полной мере проблему восстановления функции в проксимальном межфаланговом суставе, что, на наш взгляд, в первую очередь связано с состоянием суставного хряща и сухожильно-капсульного аппарата, а также отсутствием реабилитационных мероприятий.
Двухэтапное лечение, включающее плавную дистракцию и артопластику с введением мультипотентных мезенхимальных стромальных клеток (ММСК) жировой ткани в полость сустава на втором этапе, может существенно улучшить результаты лечения и имеет ряд предпосылок.
Дозируемая дистракция позволяет восстановить анатомическую ось пораженного пальца (если фиброзный анкилоз был в порочном положении), создать структурную основу для оперативного доступа к внутрисуставным формированиям, наблюдать в ряде случаев феномен роста внутрисуставного костного регенерата. Постоянная нарастающая (но дозируемая!) дистракция сустава вызывает временную ишемию дистрагируемых тканей и, как следствие, локальную гипоксию.
Именно дефицит кислорода способствует сохранению гомогенности активно пролиферирующей менее коммитированной популяции мезенхимальных клеток, сохраняющих высокий уровень жизнеспособности. Это сопровождается изменением экспрессии генов структурных и регуляторных белков цитоскелета, регуляторов клеточного цикла, а также регуляции экспрессии некоторых про- и антиапоптотических белков [3]. Доказано, что гипоксическая нагрузка активирует хемокины, секретируемые клетками поврежденной ткани, градиент концентрации которых определяет способность стромальных клеток к миграции [4]. В условиях гипоксии повышается экспрессия фактора роста ММСК (SDF-1), стимулирующего пролиферацию, и его рецептора (CXCR4), что приводит к усиленной миграции клеток-предшественниц в зоны повреждения [5].
Снижение в условиях гипоксии синтеза макроэргических соединений (аденозинтрифосфорная, пиро- поли- и креатинфосфорная кислоты и др.) активирует синтез нуклеиновых кислот и белков, в том числе хемоаттрактантов, стимулирующих миграцию ММСК жировой ткани.
Миграция стромальных клеток по градиенту концентрации хемоаттрактанта является необходимым компонентом хоуминга, обеспечивающим их доставку в пораженный участок ткани, что имеет решающее значение для эффективности клеточной терапии [6]. Этот процесс обусловлен наличием на мигрирующих клетках рецепторов, избирательно взаимодействующих с цитокинами и/или хемокинами, вырабатываемыми клетками поврежденной ткани.
Таким образом, дискретное растяжение тканей с помощью аппарата внешней фиксации можно рассматривать как ишемический стимул, потенцирующий фибриллогенез, пролиферацию и дифференцировку клеток.
Можно предположить, что дополнительное введение в полость патологически измененного сустава культивированных аутологичных ММСК будет служить не только «механической подушкой», облегчающей движения, но мощным катализатором репаративных процессов.
Для достижения максимального успеха в послеоперационном периоде необходимо проведение полноценного курса реабилитационных мероприятий.
С учетом анатомических особенностей сустава наиболее целесообразным в комплексе реабилитационных мероприятий считаем использование лечебной гимнастики в виде активных и пассивных упражнений для оперированного пальца, бегущего импульсного магнитного поля и ультразвука низкой интенсивности.
В эксперименте in vitro нами было доказано, что воздействие магнитным полем в терапевтических дозировках не оказывает цитотоксического эффекта на морфологию ММСК жировой ткани, не влияет на иммунофенотип, жизнеспособность, пролиферативную и секреторную активность клеток [7, 8].
Воздействие ультразвуком низкой интенсивности в терапевтических дозировках на культуру ММСК жировой ткани in vitro также не оказывало влияния на жизнеспособность, фенотип и морфологию ММСК в культуре. Под воздействием ультразвука, независимо от особенностей культуры ММСК и её генеза, отмечалась отчетливая тенденция к увеличению пролиферативной активности клеток и активации синтеза фибронектина.
Полученные экспериментальные данные подтверждают безопасность воздействия этих физиофакторов на сустав, в полость которого могут быть имплантированы ММСК.
Лечебную физкультуру, равно как и ультразвук, мы рассматривали как одни из действующих факторов поля механического напряжения, которые могут влиять на пролиферацию, миграцию и адгезию клеток [9]. Установлено, что мультипотентные клетки могут быть чувствительны к изменению напряженности механического и гравитационного поля в моделируемых условиях, а циклические нагрузки могут стимулировать хондрогенную дифференцировку ММСК [10, 11].
Сгибание-разгибание (активное или пассивное) в проксимальном межфаланговом суставе можно условно рассматривать как действие помпы с меняющимся давлением в суставе (циклическая нагрузка).
Физиологические механизмы воздействия поля механического напряжения на клетки сложны и до конца не изучены. Проведенный нами анализ литературных данных позволил разработать упрощенный вариант схемы этого взаимодействия (рисунок).
Механическая нагрузка индуцирует синтез трансформирующего фактора роста – TGFβ, который может стимулировать ММСК к дифференцировке в хондроциты [11].
В ответ на действие факторов роста происходит активация экспрессии индуцибельной простагландин-синтазы (Cox-2) и продукции простогландина Е2, что необходимо для перехода клеток из G1-фазы в S-фазу репликации ДНК и последующей активной пролиферации [12].
О переходе клеток из одной фазы в другую свидетельствуют изменения в уровнях экспрессии матричной РНК (mRNA) маркеров генов специфических белков хондроцитов под действием ультразвука и механической нагрузки [13, 14]. Кроме того, увеличение продукции простогландина Е2 (PGE2), который оказывает сосудорасширяющее действие на большинство сосудов, ведет к усилению микроциркуляции [10].
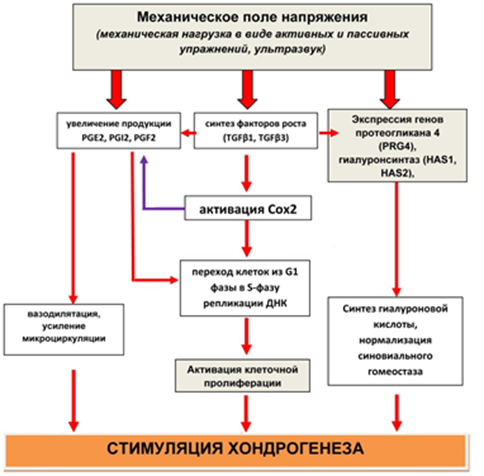
Схема влияния механического поля напряжения на хондрогенез
Механическая нагрузка стойко модулирует экспрессию генов специфических белков хондроцитов [15]. Экспрессия под влиянием нагрузки генов протеогликана 4 (PRG4) и гиалуронсинтаз (HAS1, HAS2) стимулирует синтез гиалуроновой кислоты, нормализует синовиальный гомеостаз [13]. Все эти процессы приводят к усиленной пролиферации клеток, и, как следствие, стимуляции хондрогенеза.
Таким образом, поле механического напряжения играет важную роль в репарации хрящевой ткани, а применение ультразвука и кинезотерапии после введения в сустав ММСК вполне оправдано.
Заключение
Поскольку применение дистракционного метода с последующей артропластикой «в чистом виде» не решает в полной мере проблему восстановления функции в проксимальном межфаланговом суставе у пациентов с фиброзными анкилозами, считаем целесообразным дополнить его введением в полость сустава на этапе артропластики культуры ММСК. Они могут играть роль не только «механической подушки», облегчающей движения, но и являться мощным катализатором репаративных процессов. Для достижения хороших результатов лечения необходимо проведение в послеоперационном периоде реабилитационных мероприятий, включающих магнитотерапию, ультразвук, активные и пассивные упражнения для суставов пальцев, которые не оказывают отрицательного воздействия на культуру введенных клеток и стимулируют регенераторные процессы.
Библиографическая ссылка
Новиков А.В., Щедрина М.А., Петров С.В. К ВОПРОСУ ОБ ИСПОЛЬЗОВАНИИ КЛЕТОЧНЫХ ТЕХНОЛОГИЙ В ЛЕЧЕНИИ ФИБРОЗНЫХ АНКИЛОЗОВ ПРОКСИМАЛЬНОГО МЕЖФАЛАНГОВОГО СУСТАВА ПАЛЬЦЕВ КИСТИ // Современные проблемы науки и образования. – 2017. – № 5. ;URL: https://science-education.ru/ru/article/view?id=26845 (дата обращения: 27.04.2024).



