В настоящее время лечение патологий крупных суставов зачастую принято решать при помощи методик эндопротезирования. Данный вид операций позволяет в короткие сроки восстановить функциональность и опороспособность конечности, сокращает сроки пребывания пациентов в стационаре, а, следовательно, на сегодняшний день этот метод занимает лидирующее место среди всех методик оперативного лечения патологии суставов. Несмотря на постоянное совершенствование техники эндопротезирования суставов при патологии различного генеза, число ревизионных вмешательств, по литературным данным, составляет от 15 до 45% [1; 2]. Среди наиболее частых причин, ведущих к повторному оперативному вмешательству, отмечают перипротезную инфекцию (от 27,4 до 53%) и асептическую нестабильность (расшатывание) компонентов эндопротеза (от 16 до 39,9%) [3; 4]. Поэтому выявление факторов риска развития инфекции для каждого конкретного пациента остается одной из ключевых задач научных исследований. Определение ведущих причин нестабильности компонентов эндопротеза обуславливает тактику ревизионного вмешательства. Для определения причин нестабильности эндопротеза на первом этапе большое значение имеет лабораторное исследование показателей крови. После проведения оперативного вмешательства по поводу тотального эндопротезирования в биологических жидкостях организма повышается уровень биохимических маркеров костного метаболизма, что указывает на интенсификацию процессов костного ремоделирования и является одним из проявлений адаптивно-компенсаторной реакции. Большое значение в развитии нестабильности эндопротезов имеет коморбидная патология и разные виды нарушений метаболизма. Выявление факторов риска развития нестабильности компонентов эндопротеза на догоспитальном этапе для каждого конкретного пациента остается одной из ключевых задач научных исследований.
Цель исследования: проведение анализа результатов гематологических и биохимических показателей крови в группах пациентов с первичным и ревизионным эндопротезированием тазобедренного сустава в дооперационном периоде.
Материалы и методы исследования. Результаты гематологических и биохимических исследований проанализированы у 58 пациентов с эндопротезированием тазобедренного сустава, пролеченных в ФГБУ «НМИЦ ТО им. академика Г.А. Илизарова» Минздрава РФ в 2022 году. Критериями исключения были несоответствие пациентов возрастной группе и недостаточные сведения в медицинской карте, а также наличие онкологических или сопутствующих хронических заболеваний. Заболевание диагностировалось на основании данных клинического осмотра и лабораторного исследования. Пациенты, проходившие обследование, оформили информированное согласие на публикацию данных, полученных в результате исследований. На проведение клинического исследования получено разрешение комитета по этике ФГБУ «НМИЦ ТО имени академика Г.А. Илизарова» Минздрава России.
Средний возраст обследованных пациентов составил 62,7±1,2 года (Ме - 64,0; МКИ 60,3-67,0). 60% (n=35) пациентов составили женщины, 40% (n=23) – мужчины. В 1-ю группу вошли 30 пациентов с первичным эндопротезированием тазобедренного сустава в возрасте 64,5±0,6 года (Ме - 64,0; МКИ 62,3-67,0), из них 17 женщин и 13 мужчин. Во 2-й группе 28 пациентам (18 женщин и 10 мужчин) было проведено ревизионное эндопротезирование тазобедренного сустава. Возраст данных пациентов составил 60,8±2,3 года (Ме 62,5; МКИ 52,8-69,5).
Всем пациентам при поступлении и в процессе лечения с целью контроля динамики заболевания проводили скрининг гематологических показателей крови: общеклинических показателей красной крови, лейкоцитарной формулы, СОЭ. Также проводилось исследование биохимических показателей сыворотки крови пациентов: определение концентрации общего белка, СРБ, альбуминов, глюкозы, АСТ, АЛТ, креатинина и мочевины. В ходе исследования использовалось следующее оборудование: Hitachi/BM 902 (Япония) (регистрационный № МЗ РФ 2000/564); Paragon (Beckman, США) (регистрационный № 2005/282); StatFax (регистрационный № 2004/1258). В качестве нормы были взяты референтные интервалы, установленные производителем реагентов.
В соответствии с требованиями, предъявляемыми к исследованиям в медицине, статистическая обработка проводилась на основе сформированной электронной базы данных, полученных в результате исследования, с использованием интеграторного модуля AtteStat 1.0 для программы Microsoft Excel. Полученные данные были обработаны методами непараметрической статистики, статистическую значимость различий в группах сравнения оценивали с помощью критерия Вилкоксона. Выборки были проверены на нормальность распределения, различия считались статистически значимыми при р<0,05.
Результаты исследования и их обсуждение. Лабораторными тестами, играющими весомую роль в интерпретации результатов анализов, являлись клинически значимые показатели воспаления и послеоперационной кровопотери. На рисунке представлены показатели красной крови: уровень эритроцитов, гемоглобина и гематокрита.
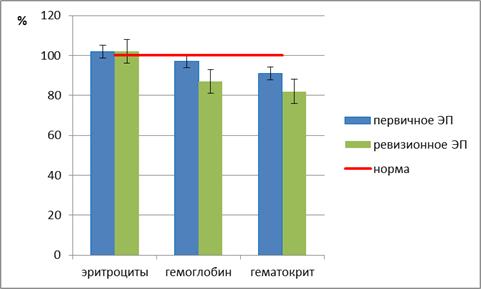
Гематологические показатели крови в группах пациентов с первичным и ревизионным эндопротезированием тазобедренного сустава
Показатели белой крови были в пределах референтных значений, и в данной работе они не приводятся.
Было отмечено, что общеклинические показатели красной крови пациентов обеих исследуемых групп в дооперационном периоде находились в пределах нормальных значений. Количество эритроцитов соответствовало референтной норме и не отличалось в обеих группах. Однако у пациентов с ревизионным эндопротезированием показатели гематокрита и гемоглобина были статистически значимо ниже, чем у пациентов с первичным эндопротезированием (Me гемоглобина в 1-й группе 139 г/л, МКИ 132–148; Me во 2-й группе 127 г/л, МКИ 113–139; Me гематокрита в 1-й группе 41,2%, МКИ 38,3–43,2; Me во 2-й группе 37,6%, МКИ 33,2-41,2).
В пределах допустимых значений находились общеклинические показатели белой крови пациентов обеих групп: уровень лейкоцитов, палочкоядерных и сегментоядерных нейтрофилов, лимфоцитов (табл. 1).
Таблица 1
Гематологические показатели сыворотки крови пациентов с первичным и ревизионным эндопротезированием тазобедренного сустава
|
Показатель |
Норма |
Первичное э/пр |
Ревизия |
|
Лейкоциты, 109/л |
4-9 |
6,9 (5,7;8,2) |
6,6 (5,2;8,4) |
|
Нейтрофилы, % |
47-72 |
60,0 (54,9;65,7) |
61,8 (52,0;64,8) |
|
Эозинофилы, % |
0-5 |
2,0 (1,3;3,2)* |
3,4 (2,35;4,1) |
|
Базофилы, % |
0-1 |
0,8 (0,4;1,0) |
0,8 (0,5;0,9) |
|
Моноциты, % |
3-11 |
7,9 (6,0;9,3) |
8,0 (6,6;9,7) |
|
Лимфоциты, % |
19-45 |
29,8 (25,3;34,6) |
30,0 (23,6;41,4) |
Примечание: * - показатели, имеющие статистически значимые различия между группами при уровне значимости р <0,05.
Биохимические показатели сыворотки крови пациентов обеих групп в дооперационном периоде представлены в таблице 2. Существенных различий в показателях сыворотки крови в группах сравнения не обнаружено. Данные показатели также не отличались от референтных значений.
Таблица 2
Биохимические показатели сыворотки крови пациентов с первичным и ревизионным эндопротезированием тазобедренного сустава
|
Показатель |
Норма |
Первичное э/пр |
Ревизия |
|
Общий белок, г/л |
64,0-83,0 |
75,0 (72,9-78,1) |
72,5 (69,0;79,0) |
|
Альбумины |
35,0-50,0 |
44,8 (42,6;49,3) |
44,0 (39,9;47,1) |
|
Глюкоза |
4,0-6,1 |
5,7 (5,1;6,2) |
5,5 (5,2;5,9) |
|
АСТ |
0-40,0 |
21,0 (18,0;27,0) |
19,0 (15,2;24,6) |
|
АЛТ |
0-41,0 |
22,0 (15,0-26,9) |
15,0 (11,0;22,0) |
|
Креатинин |
71,0-115,0 |
80,0 (72,8;88,3) |
85,9 (74,8;96,3) |
|
Мочевина |
2,5-8,3 |
5,6 (5,2-6,4) |
5,9 (4,8;6,8) |
|
СРБ, мг/л |
0-5,0 |
4,2 (2,3;6,2) |
2,9 (1,6;8,4) |
Поиски критериев прогноза результатов эндопротезирования крупных суставов приводятся в целом ряде исследований [2; 3; 5]. Основным стандартом диагностики развития септической нестабильности является микробиологическое исследование. Наличие воспалительного процесса находит отражение в изменении клинического анализа крови, что позволяет сделать выбор в пользу антибактериальной терапии в самом начале процесса. По данным зарубежных исследований, в частности Guide Line AAOS (2010), лабораторными критериями септической нестабильности считается сочетание показателей СОЭ и СРБ [6]. У пациентов с асептической нестабильностью эндопротеза в проведенных исследованиях авторы не обнаружили изменения показателей, связанных с воспалительным процессом.
В настоящий момент для оценки риска развития асептической нестабильности эндопротеза наиболее убедительным считается использование в лабораторной практике показателей деградации межклеточного матрикса костной ткани, таких как дезоксипиридинолин (DPYR), остеопротегерин (OPG), N-концевой телопептид коллагена I типа (NTx), С-концевой телопептид коллагена I типа (CTX-I). Однако эти тесты являются достаточно дорогостоящими, а их клиническая эффективность на данный момент не доказана. Использование маркеров метаболизма костной ткани, подразумевающее определение клинически обоснованных показателей кислой и тартратрезистентной щелочной фосфатазы, может применяться для оценки риска развития асептической нестабильности, но требует проверки на большом количестве клинического материала.
Известно, что эндопротезирование крупных суставов сопровождается большой кровопотерей, высокой частотой послеоперационной анемии и гемотрансфузий [7]. В литературе отмечено, что даже незначительная предоперационная анемия влияет на исход оперативного вмешательства [8]. Кроме того, известно, что существует взаимосвязь между особенностями остеогенеза и количественными изменениями состава периферической крови [9]. В ходе работы авторами были обнаружены статистически значимые различия в показателях красной крови, они оказались снижены у пациентов с ревизионным эндопротезированием. В то же время наблюдаемые изменения являются умеренными. Регистрируемые у пациентов с ревизионным эндопротезированием некоторые признаки сниженного эритропоэза носят нормохромный характер и, возможно, обусловлены наличием изменений в активности эритропоэза, связанных с костным ремоделированием. Известно, что строма, которая обеспечивает кроветворение, происходит из той же линии, что и клетки хряща и кости, и включает иерархию скелетных стволовых клеток и предшественников, которые дают начало различным видам скелетных клеток, а также способствуют росту скелета, поддерживают скелетную массу и передают значительный потенциал для восстановления и регенерации [10], которыми наделена кость. Механизмы, которые регулируют развитие гемопоэтического костного мозга в кости, формирование стромальных стволовых клеток остаются в значительной степени неисследованными. Их взаимодействие с процессами, которые определяют форму, структуру, размер и массу костей, также еще предстоит выяснить.
В настоящее время ведущее представление о развитии асептической нестабильности эндопротеза основано на роли нарушений в процессах костного ремоделирования. Исходя из этого и данных литературных источников, наиболее диагностически значимым в прогнозе оперативного вмешательства является определение тестов, отражающих ремоделирование костной ткани. В достаточном числе литературных источников решается клинически важная задача - попытка прогноза результатов эндопротезирования тазобедренного сустава, которая осуществляется с помощью лабораторных тестов [11; 12], выполняемых в биологических жидкостях пациента (кровь, моча). Наиболее информативными лабораторными показателями являются определение активности щелочной фосфатазы (ее костной фракции), расчет соотношений активности кислой и щелочной фосфатаз, определение содержания кальция и гидроксипролина. Все варианты изменений этих показателей чаще всего указывают на замедленное течение процессов костеобразования [13; 14].
В то же время ни у кого не вызывает сомнения, что коморбидность является фактором риска развития осложнений [11], что находит отражение в изменении биохимических показателей сыворотки крови. Нарушения отдельных звеньев метаболизма значительно влияют на отдаленные результаты эндопротезирования крупных суставов и на развитие нестабильности компонентов эндопротеза [15], а, следовательно, требуют наблюдения за лабораторными показателями пациентов на амбулаторном этапе.
Заключение. Стратегия дальнейшего улучшения результатов эндопротезирования крупных суставов, по всей видимости, должна базироваться на совершенствовании диагностических алгоритмов комплексного обследования пациентов, нуждающихся в операции первичного эндопротезирования, что позволит своевременно выявлять или исключать риски ревизионного эндопротезирования и корректировать при необходимости тактику лечения.
Авторами показано, что все гематологические и биохимические показатели крови пациентов с первичным эндопротезированием тазобедренного сустава и асептической нестабильностью эндопротеза находятся в пределах референтных значений, что, очевидно, обусловлено клиническим отбором пациентов. В рамках стандартного обследования нет лабораторных тестов, позволяющих выявить группу риска пациентов, которым грозит развитие асептической нестабильности компонентов эндопротеза тазобедренного сустава.
Оценка достоверности различий в гематологических показателях обнаружила статистически значимое снижение показателей гемоглобина и гематокрита у пациентов с асептической нестабильностью эндопротеза, а также повышенный уровень эозинофилов в лейкоформуле крови.
Современные клинико-лабораторные алгоритмы обследования обладают хорошей диагностической ценностью в выявлении развития нестабильности эндопротезов после первичного эндопротезирования, однако чувствительность и специфичность ряда методов диагностики не позволяет оценить риски перед первичным эндопротезированием тазобедренного сустава.
Библиографическая ссылка
Матвеева Е.Л., Гасанова А.Г., Чегуров О.К. РЕЗУЛЬТАТЫ ГЕМАТОЛОГИЧЕСКОГО ИССЛЕДОВАНИЯ И БИОХИМИЧЕСКОГО АНАЛИЗА СЫВОРОТКИ КРОВИ ПАЦИЕНТОВ С ПЕРВИЧНЫМ И РЕВИЗИОННЫМ ЭНДОПРОТЕЗИРОВАНИЕМ ТАЗОБЕДРЕННОГО СУСТАВА // Современные проблемы науки и образования. – 2023. – № 5. ;URL: https://science-education.ru/ru/article/view?id=32992 (дата обращения: 10.05.2024).



