Введение
Воздействие непрерывного электромагнитного излучения на биологические молекулы и сопровождающие этот процесс структурные изменения представляют собой важную задачу в рамках фундаментальных проблем взаимодействия излучения с веществом и трансформации энергии света в биологических молекулах. Такие исследования важны для практических приложений в микроинженерии (возможностью контроля и управления состоянием вещества на молекулярном уровне) и в практической медицине (возможностью создания более эффективных схем лечения). Особый интерес представляет изучение межмолекулярных взаимодействий в водных растворах аминокислот в условиях непрерывного освещения видимым светом низкой интенсивности. Эти исследования представляют интерес для изучения межмолекулярных взаимодействий внутри белков, понимания роли нелинейных эффектов в динамике первичных фотореакций внутри сложных фоточувствительных биосистем. Аминокислоты (АК), как известно, являются основными строительными блоками белков и непосредственно участвуют в донорно-акцепторных взаимодействиях в фотоиндуцированных процессах переноса заряда через биологические мембраны. Лизин является основной аминокислотой и имеет самую длинную боковую цепь с концевой NH2 группой, которая является наиболее важной для его функциональной активности. Эта аминогруппа имеет рКа (рКа ~ 10,5) значительно выше, чем в a-аминогруппе (рКа ~ 9). Боковая NH2- группа высоко реактивна и часто участвует в реакциях в активных центрах белков и ферментов. Глицин является самой простой аминокислотой и обязательно присутствует в составе соединительных полипептидных цепей в белках.
Целью данной работы было исследование с помощью адсорбционной спектроскопии в УФ-видимой области, спектрофлуориметрии и оптической микроскопии влияния низкоинтенсивного оптического излучения на структуру и свойства L-лизина и L-глицина в водной фазе.
Материалы и методы
Образцы L-лизина моногидрохлорида и L–глицина Sigma-Aldrich растворяли в деионизованной воде при рН ~ 6.8 и фильтровали через фильтр (Millex”CV с размером пор 0,22 мк). Для предотвращения попадания глицериновой смазки с фильтра последний перед заполнением рабочим раствором несколько раз ополаскивали деионизованной водой. Деионизованная вода была получена на системе (Nanopure Diamond ultrapure). Чистота воды сертифицирована величиной проводимости в 18 mQ.
Флуоресценция чрезвычайно чувствительна к присутствию примесей, поэтому, для предотвращения появления артефактного свечения, в отношении используемых кювет соблюдали особую предосторожность по отношению к загрязнению и как контроль использовали образец с деионизованной водой. Спектрофотометрические измерения в УФ-видимой области были выполнены на спектрофотометре модели UV/VIS Evolution 600 (Thermo Scientific, США). Флуориметрические измерения были выполнены на спектрофлуориметре Lumina Fluorescence (Thermo Scientific, США). Данные обрабатывали с помощью программы Origin, версии 6.0 и компьютерных программ, входящих в программное обеспечение каждого прибора. Полученные спектры усредняли по пяти экспериментам.
Визуальные наблюдения с 20-кратным увеличением и временным разрешением выполняли с помощью лабораторного устройства, сконструированного на основе скоростной видеокамеры, увеличительной оптики, светового источника и персонального компьютера. В качестве источника света использовали непрерывный лазер (Nd:YaG, λ=532 нм, 18 мВт или He-Ne, 633 нм, 4 мВт). Мощность излучения регулировалась набором нейтральных светофильтров в пределах 1.8–18 мВт для длины волны 532 нм и 1.4-4 мВт для длины волны 633 нм. Все эксперименты проводились при комнатной температуре.
Результаты исследования и их обсуждение
На рис. 1 представлены спектры поглощения водных растворов L-глицина и L-лизина в УФ-видимой области. Отличительной особенностью этих спектров является появление
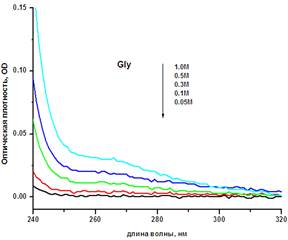
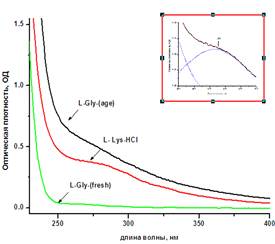
Рис. 1. Спектры поглощения: (слева) - L-глицина (fresh) при концентрациях 0.05, 0.1, 0.3, 0.5 и 1.0 М; (справа) – 1М растворов: (красная кривая) - L-лизина HCl, (зеленая кривая ) L- глицина - свежеприготовленный (fresh), (черная кривая) выдержанный > 1 месяца (age). На вставке: аппроксимация кривой Lys HCl разложением на компоненты с помощью лоренцевых кривых 230 и 273 нм.
нового пика возле 270 нм. Амплитуда этого пика при концентрациях (0.3-1.0 М) в лизине была выше, чем в глицине, если раствор последнего использовался сразу после приготовления. Однако при «старении», т.е. при выстаивании (более месяца) раствора в закрытой посуде при комнатной температуре, спектр поглощения глицина имел более высокую по сравнению с лизином амплитуду возле 270 нм. Тенденция к увеличению оптического поглощения глицина возле 270 нм также наблюдалась при повторном облучении свежеприготовленного образца глицина.
Появление новых свойств возле 270 нм в спектрах поглощения исследуемых растворов АК является достаточно неожиданным, поскольку оба этих образца известны тем, что они имеют широкую область прозрачности в диапазоне 230-900 нм и их структура не содержит конъюгированных связей. Из всех аминокислот, как известно, в УФ-области между 250-300 нм поглощают только три ароматические аминокислоты (фенилаланин, тирозин и триптофан), содержащие в своей структуре кольцо из сопряженных С=С связей. Максимум длины волны триптофана и тирозина находится возле 280 нм, и они имеют более высокий по сравнению с фенилаланином коэффициент поглощения, который поглощает на длине волны 260 нм. По этой причине считают, что триптофан и тирозин вносят основной вклад в поглощение белков в этой области. Между тем появление подобного пика в спектре поглощения L-лизина или L-глицина не является случайным. Аналогичный результат был получен ранее в работах [1; 3-4]. Согласно интерпретации авторов работ [3-4], впервые наблюдавших это свойство в растворе моногидрохлорида L-лизина, поглощение при 270 нм обусловлено образованием агрегатов при взаимодействии молекул лизина с молекулами воды. Агрегация происходит за счет образования связи, которая посредством молекулы воды объединяет N-H группы пары взаимодействующих молекул лизина. Позже в работе [1] было показано, что пик возле 270 нм проявляется в спектрах растворов как органических веществ (L-лизин, L-аланин, D-глюкоза, сахароза) так и неорганических солей (NaCl, KCl и LiCl). Это привело авторов к заключению о том, что это свойство является не столько особенностью лизина, как это утверждалось в [3], или других биологических молекул, сколько уникальной характеристикой воды, взаимодействующей с растворенными ионами или заряженными молекулами. Учитывая результаты вышеупомянутых [1; 3-4] и теоретических работ [2; 5], мы полагаем, что в наших условиях имеют место оба типа межмолекулярных взаимодействий - аминокислота-аминокислота и аминокислота-вода, которые играют важную роль не только в появлении адсорбционного пика возле 270 нм, но и в образовании флуоресцентных состояний и структур. На рис. 2А представлены спектры флуоресценции лизина, записанные при разных длинах волн возбуждения. Каждый спектр представляет собой сложную по форме широкую полосу, расположенную в области между 310 и 500 нм. Изменение длины волны возбуждающего света приводило к изменению формы, интенсивности и сдвигу максимума спектральной кривой. Так, при возбуждении светом с длиной волны 290 нм максимум флуоресценции наблюдался около 426 нм, тогда как при возбуждении 310 или 410 нм максимум располагался при 410 и 476 нм, соответственно.
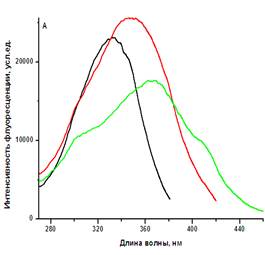
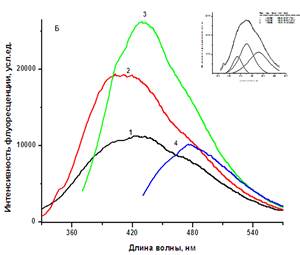
Рис. 2: А – 1М L-лизин моногидрохлорид. Спектры возбуждения – кривые: черная ( lэмис = 435 нм), красная (lэмис = 455 нм) и зеленая (lэмис = 471.нм); Б - спектры флуоресценции – кривые: 1(lвозб = 290 нм), 2 – (lвозб = 310нм), 3 (lвозб = 355нм) и 4 -(lвозб = 410нм). На вставке аппроксимация спектра флуоресценции (lвоз = 355 нм) с компонентами в разложении с помощью приближения Лоренца.
Аналогичные изменения наблюдались в спектрах возбуждения L-лизина при варьировании длины волны испускания (рис. 2Б). Наличие множественных полос в спектрах действия и спектрах флуоресценции свидетельствует об образовании гетерогенных состояний или структур в исходно оптически однородном растворе исследуемого образца. Разложение спектральных кривых L-лизина HCl позволило определить как минимум три разных состояния с положением максимумов при 383, 426 и 475 нм в спектрах флуоресценции и при 320, 345, 374 нм в спектрах возбуждения. Эти результаты находятся в полном соответствии с данными, опубликованными ранее [1; 3-4]. Аналогичные свойства были выявлены в растворе глицина. Впервые было показало, что в растворе глицина, как и в лизине, образуются множественные флуоресцентные состояния и/или структуры. В спектрах возбуждения максимумы полос наблюдались при 280, 335 или 354-369 нм, а спектрах эмиссии - возле 410 и 456 нм (lвозб = 290, 326 или 355 нм) и 478 нм (lвозб = 410 нм). Интенсивность спектров глицина была слабее по сравнению с лизином, однако интенсивность могла увеличиваться (иногда даже в несколько раз) при «старении» или повторном облучении раствора. Флуоресценция АК при 450-470 нм проявлялась в прозрачном объеме жидкости в виде ярко окрашенной протяженной структуры. В отсутствие поглощения эта структура имела окраску входящего излучения. Наиболее контрастная картина получалась при использовании лазерного излучения с диаметром пучка ~1.5-2 мм. Эту необычную структуру в жидкости исследовали с 20-кратным увеличением и временным разрешением с помощью лабораторного устройства, сконструированного на основе видеокамеры и увеличительной оптики при двух длинах волн 532 или 633 нм. На рис. 3 представлено увеличенное изображение этой структуры при лазерном возбуждении.
А  Б
Б
Рис. 3: А – увеличенное изображение (20х) структуры жидкости внутри светящегося «трэка»; Б – образование аморфных форм АК на поверхности кюветы в месте светового пятна.
Хорошо видно, что ее изображение представляет собой подобие спекл-картины - диффузной структуры, состоящей из темных и светлых пятен различной формы и величины и распределенных в пространстве случайным образом. Такое распределение интенсивности обычно формируется из-за вариаций в показателе преломления, обусловленных наличием в среде неоднородностей, которые по своим макроскопическим параметрам (структуре, плотности и т.п.) существенно отличаются от жидкости в целом. Чаще всего центрами образования таких неоднородностей являются кластеры – ассоциированные молекулы, которые могут включать в себя макроскопическое количество молекул. Таким образом, спекл-картина (результат интерференции света, рассеянного ансамблем многих оптических неоднородностей в среде) однозначно свидетельствует о кластеризации вещества, инициируемой низко интенсивным светом в ненасыщенном растворе аминокислот при комнатной температуре. Было показано, что так называемая спекл-картина обладает динамической неустойчивостью в пространственно-временном масштабе. Например, в течение времени наблюдения (5-60 минут) было заметно движение диффузных пятен - изменялись их форма и размер - пятна поочередно появлялись и исчезали без какого-либо заметного перемещения в пространстве. Эти изменения имели осциллирующий характер. Вместе с мерцанием среды наблюдали также другой тип движения, который по сложным траекториям внутри трека совершали различные по размеру и форме твердые структуры. Эти плотные структуры высаживались на боковые стенки кюветы, образуя непрозрачные области внутри освещенного пятна (рис. 3Б). Вместе с аморфными формами в треке происходило образование наноразмерных кристаллических форм аминокислотных образцов. Как подтверждение на рис. 4 А и Б представлено фото микрокристаллов лизина и глицина, образовавшихся после медленного выпаривания облученных образцов при комнатной температуре. На рис. 4 видно множество разных по форме и размеру кристаллических форм АК. В другой серии экспериментов было показано, что фазовые переходы (образование агрегатов и кристаллических форм) в каждом из образцов происходили в интервале 1,4-18 мВт без порога. Мощность действующего света влияла на число образующихся твердых
А  Б
Б 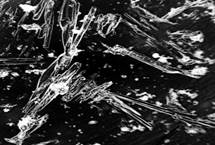
Рис. 4. Изображение микрокристаллов лизина (А) и глицина (Б), образовавшихся после выпаривания облученных растворов при комнатной температуре. Снимки получены с помощью камеры Webbers 320M на микроскопе OptiTech c увеличением 400х
частиц, интенсивность свечения протяженной структуры и характер распределения в ней диффузных пятен. Температура и концентрация вещества также влияли на число, размеры и подвижность частиц. Эти результаты показали, что образование зародышей кристаллов в растворе АК, обычно наблюдаемое только при использовании мощных лазеров [6], может происходить также при использовании источников света низкой интенсивности. Лазером индуцированное образование зародышей кристаллов происходит за счет ряда механизмов, некоторые из них включают кавитацию, другие нет. В последнем случае индуцированные процессы описываются эффектом Керра, в котором поляризованный электромагнитный луч, взаимодействуя с зарядами молекул, инициирует упорядочивание молекул и тем самым индуцирует кристаллизацию вещества. Очевидно, что кавитация исключается при использовании непрерывных источников с низкой интенсивностью света. Происходит ли кристаллизация в наших экспериментальных условиях по второму типу механизма или этот процесс обусловлен другим(и) механизмом(ами), помогут прояснить дальнейшие эксперименты. Очевидным фактом является то, что в данных экспериментальных условиях заряженные формы аминокислот вступают в тесное взаимодействие с молекулами воды, образуя межмолекулярные соединения или сольваты определенного стехиометрического состава, каждый из которых может дать спектр, смещенный относительно главного на определенный небольшой интервал частот. Вода, как растворитель, содержит ОН-группу, которая способна вступать в водородную связь с концевыми имино-, амино- и карбонильными группами аминокислот, образуя различные по составу и ориентации межмолекулярные соединения. Очевидно также, что вода входит в качестве структурного элемента в кристаллическую или агрегированную фазу аминокислот.
Заключение
Обобщая полученные результаты, можно выделить главные моменты.
УФ-спектрофотометрия L-лизина моногидрохлорида и L-глицина выявила наличие новой полосы возле 270 нм, которая характерна для ароматических аминокислот (триптофана и фенилаланина) в растворе и белках. Этот результат свидетельствует о том, что изменения в белках, наблюдаемые на этой полосе, могут быть связаны не только и не столько с триптофановым или фенилаланиновым аминокислотными остатками, сколько с изменением межмолекулярных взаимодействий – аминокислота-аминокислота и аминокислота-вода-, или, как полагают авторы работы [1], с кластеризацией воды.
Другой важный вывод, который следует из проведенных экспериментов, заключается в том, что видимый свет низкой интенсивности способен влиять на характер гидрофобных и/или полярных взаимодействий и вызывать большие изменения в структуре и свойствах биологических молекул в жидкой фазе. Влияние низкоинтенсивного света происходит по механизму не прямого фотохимического или теплового воздействия излучения на биомолекулу, а посредством нелинейных взаимодействий, природу которых еще предстоит установить. Этот факт представляется принципиально важным с точки зрения выявления основных закономерностей взаимодействия низкоинтенсивного излучения с биологическими объектами на молекулярном уровне, а также для понимания донорно-акцепторных взаимодействий при фотоиндуцированном транспорте зарядов внутри сложных биологических систем.
Авторы выражают благодарность Центру коллективного пользования ИТЭБ РАН и особенно проф. В.С. Акатову и Ю. Шаталину за микрофотосъемку и подготовку фотографий микрокристаллов.
Рецензенты:
Полозов Р.В., д.ф.-м.н., ведущий научный сотрудник, Лаборатория физической биохимии, Федеральное государственное учреждение науки «Институт теоретической и экспериментальной биофизики Российской академии наук» (ИТЭБ РАН), г. Пущино.
Новоселова Е.Г,, д.б.н., профессор, главный научный сотрудник, Лаборатория механизмов рецепции, Федеральное государственное учреждение науки «Институт биофизики клетки Российской академии наук» (ИБК РАН), г. Пущино.



