Введение. В настоящее время бисфосфонаты используются в качестве химиотерапевтического лечения злокачественных заболеваний, препараты вводят внутривенно для профилактики костных метастазов и их осложнений [2]. Бисфосфонаты также используют при патологии метаболических процессов и лечении остеопороза, болезни Педжета, педиатрического несовершенного остеогенеза, в качестве средства, препятствующего несбалансированной работе остеокластов, расщепляющих минеральные структуры кости [2, 4]. В последние годы отмечен рост числа пациентов с остеонекрозом костей лицевого скелета у лиц с наркотической зависимостью от дезоморфина и первитина, при изготовлении которых используется красный фосфор. На территории Российской Федерации в последние годы отмечается тенденция к росту и распространению в различных регионах употребления кустарно изготовленного дезоморфина: с 16 регионов в 2006 году до 60 регионов в 2009 году [4]. В первом квартале 2010 года изъято 150 миллионов среднеразовых доз дезоморфина, что, по оценкам Федеральной службы Российской Федерации по контролю за оборотом наркотиков, соответствует годовой потребности в дезоморфине 300 000 человек [9, 10].
Наиболее частым симптомом метастазов в костях является боль. К механическим факторам болевого синдрома относят повышение внутрикостного давления, сдавление мягких тканей и механическую компрессию кости. К химическим фактором относят простагландин Е, ацидоз, сопровождающий остеолиз и факторы, продуцируемые или активируемые опухолью [5]. На ранних стадиях развития метастаза боль обусловлена раздражением внутрикостных и периостальных нервных окончаний за счет выделения цитокинов и увеличения внутрикостного кальция.
Патогенентические особенности взаимодействия фосфора, содержащегося в препаратах для лечения онкобольных и препаратах используемых при изготовлении синтетических наркотических веществ, с клеточными и ферментативными системами в настоящее время, изучен не полностью [1, 6].
По мнению ряда авторов, на ранних стадиях метастазирования онкопроцесса, боль является ведущим симптомом и обусловлена раздражением внутрикостных и периостальных нервных окончаний, по средствам выделения цитокинов и явлениями внутрикостной гиперкальциемии. По мере распространения первичного онкологического очага, явления болевого синдрома прогрессируют, что также обусловлено целым рядом факторов. Так, отмечено повышение внутрикостного давления, обусловленного явлениями ацидоза, продуцируемого или активируемого химическими реакциями в мягкотканном опухолевом очаге, что способствует явления периферических отеков, застойных явлений и приводит к механической компрессии костной ткани [7].
Подобная боль не связана с нагрузкой на кость и может даже усиливаться в состоянии покоя. Однако по мере нарастания деструкции костной ткани появляется так называемая функциональная боль, обусловленная механическим ослаблением костных структур и их нестабильностью. Функциональная боль усиливается при нагрузке на пораженную кость и может свидетельствовать о риске развития патологического перелома.
Патологическим переломам, кроме оголения кости в полости рта, предшествуют явления длительной инфильтрации мягких тканей, без признаков нагноения. Патологические переломы сопровождаются смещением и аномальной функцией за счёт инфильтрации мышц, при вторичном инфицировании которых обрекает пациентов на мучительные боли усугубляя функциональные нарушения (рис. 1).
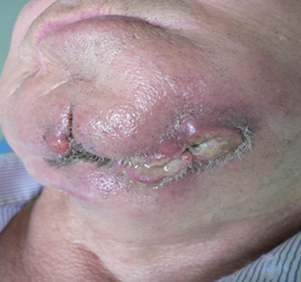
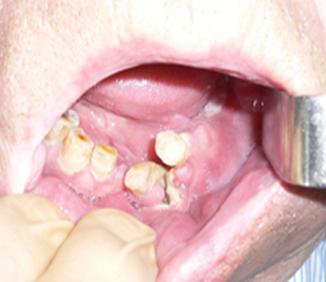
Рис. 1. Клинические проявления бисфосфонатных остеонекрозов в челюстно-лицевой области
С учётом существующих патогенетических аспектов бисфосфанатных остонекрозов определена цель исследования: обосновать необходимость планирования и изготовления аппарата, имитирующего анатомическую целостность нижней челюсти, обеспечивающего её функциональную активность при патологическом переломе, обусловленном бисфосфонатным остеонекрозом.
Материал и методы исследования. Оперативное лечение проведено 15 пациентам, обратившимся и находившимся под наблюдением в отделении челюстно-лицевой хирургии Краевой клинической больницы города Ставрополь с характерной клинической картиной патологического перелома нижней челюсти. 12 пациентам установлены стандартные бинаправленные аппараты компрессионно-дистракционного действия. В раннем послеоперационном периоде стандартные аппараты выполняли задачу иммобилизирующей конструкции, что способствовало восстановлению функциональной активности нижнечелюстной кости и мышечного аппарата. 3 пациентам установлены аппараты собственной конструкции.
Результаты исследования. Клинически отмечено улучшение общего состояние больных за счёт значительного снижения явлений болевого синдрома. Кроме этого, у пациентов в течение 12-14 дней в период функционального покоя установленных аппаратов, отмечено купирование явлений инфильтрации мягких тканей. Гноетечение практически отсутствует (в посеве на микрофлору патогенной микрофлоры не выявлено), отмечен скудный рост грануляционной ткани в устье свищевого хода.
Однако активация и динамическая нагрузка аппаратов с целью оптимизации функциональной активности поражённого органокомплекса вне зависимости от сроков начала процесса активации приводила к нестабильности фиксирующих конструкций. Положительная клиническая картина имела временный результат и была обусловлена ограниченными функциональными возможностями используемых стандартных аппаратов.
По мере снижения стабильной фиксации конструкции возникала необходимость проведения повторных оперативных вмешательств с целью стабилизации фиксирующих конструкций. Однако у трёх пациентов основной группы, с двусторонними патологическими переломами, проведение повторных оперативных вмешательств технически не представлялось возможным ввиду прогрессирования явлений остеонекроза и ограниченных функций стандартных бинаправленных аппаратов.
По результатам проведённого анализа и в соответствии с целью и задачами исследования, разработан и предложен способ профилактики патологических переломов нижней челюсти и их осложнений посредствам жёсткой иммобилизации фрагментов челюстей.
В качестве примера приводим следующий клинический случай. В марте 2013 года в отделение челюстно-лицевой хирургии краевой клинической больницы г. Ставрополь обратился пациент В. 1971 г. рождения. На момент обращения предъявлял жалобы: на диффузные боли в области нижней челюсти с иррадиацией по ходу II ветвей V пары черепно-мозговых нервов больше справа, носящих невыносимый характер, не купируемых ненаркотическими анальгетиками, на общую слабость, на наличие дефекта слизистой в преддверии полости рта и оголение кости нижней челюсти, на гноетечение через свищевой ход в подподбородочной области.
Из анамнеза установлено, что пациент в течение 1,5 лет употреблял дезоморфин, изготовленный кустарным способом из препаратов («Коделак», «Терпинкод», «Тетралгин», «Пенталгин», «Седал- М»). Дезоморфин в процессе получения подвергается обработке бензином или ацетоном, кроме того, содержит кристаллический йод, красный фосфор и ряд побочных, токсических веществ. Доказано, что химические вещества, входящие в состав дезоморфина, способны оказывать локальные токсические, так и общие тератогенные эффекты на различные органы и ткани организма.
Со слов больного, около 5 месяцев назад врачом стоматологом удален одиночно стоящий, подвижный нижний правый клык, выраженного болевого симптома указанный зуб не имел. После удаления зуба лунка зуба не закрылась, через некоторое время появилось гноетечение из лунки. В течение пяти месяцев пациенту трижды была проведена периостотомия, однако облегчения не наступало, пациент отмечает катастрофически быстрое оголение кости в полости рта после каждого хирургического вмешательства.
При поступлении в отделение пациенту проведено общеклиническое обследование, выполнена мультиспиральная компьютерная томография с трёхмерной реконструкцией, проведён курс противовоспалительной, нейротропной, общеукрепляющей терапии, пациент выписан через семь дней с улучшением под наблюдение хирурга по месту жительства с рекомендациями.
По данным контрольной ортопантомограммы, через 2 месяца, отмечено распространение патологического процесса, характеризующегося деструкцией костной ткани в проекции жевательной группы зубов нижней челюсти справа и подбородка. Деструкция костной ткани в проекции тела нижней челюсти справа, с сохранением целостности компактного слоя тела нижней челюсти на участке до 5 миллиметров.
С учётом полученного негативного результата лечения у 12 пациентов со стандартными аппаратами и представленной клинико-рентгенологической картины пациента В. с профилактической и лечебной целью по данным виртуального моделирования изготовлен индивидуальный полифункциональный аппарат (рис. 2).

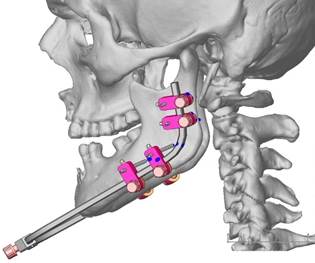
Рис. 2. Виртуальное моделирование для изготовления индивидуального полифункционального аппарата
В плановом порядке, с учётом выраженного болевого синдрома, под эндотрахеальным наркозом проведена установка и фиксация аппарата. В ходе установки аппарата проведена оценка функциональной активности отдельных его узлов (рис. 3).
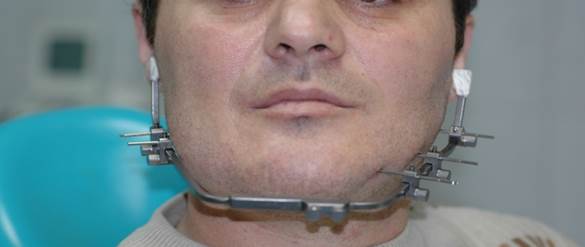
Рис. 3. Больной В. после операции
В ходе проведённого оперативного вмешательства сохранено анатомическое и окклюзионное соотношение челюстей. В раннем послеоперационном периоде пациент отмечает улучшение общего состояния, уменьшение гноетечения и значительное снижения болевого синдрома. Проведённое удаление некротизированной кости способствовало купированию локальных клинических симптомов воспаления в короткие сроки (рис. 4). Биопсия костной ткани у 5 пациентов, находившихся под наблюдением, показала наличие выраженного подавления костного обмена и существенное замедление или в некоторых случаях полное подавление процесса заживления. При этом было выявлено, что 37% пациентов получали бисфосфонаты, изготовленные кустарным способом, а 63% пациентов получали препараты, полученные промышленным способом.
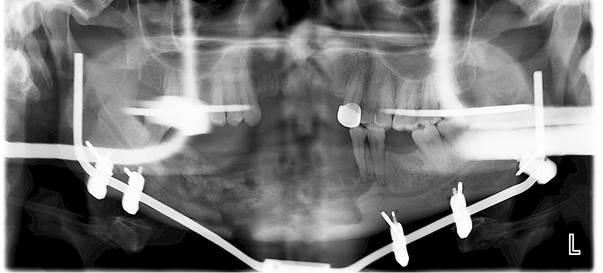
Рис. 4. Ортопантомограмма больного В.
Для пациентов, длительно принимавших бисфосфонаты (4,3±0,8 лет), являлось наличие специфических рентгенографических особенностей перелома, проявляющихся диффузным поражением кости и истончением кортикального слоя, сопровождающегося переломом и инфильтрацией окружающих тканей. Таких особенностей не наблюдалось при переломе у пациентов, принимавших бисфосфонаты на протяжении меньшего периода (1,5±0,3 лет). В группе пациентов, принимавших бисфосфонаты по показаниям, при санированной полости рта явления деструктивного и воспалительного характера были минимальными, однако у пациентов в данной группе с гигиеническим уровнем ниже 0.5 ед. отмечены явления, характерные для распространённого воспалительного процесса.
В целом имеющиеся литературные данные и полученные клинико-рентгенологические данные подтверждают тесную взаимосвязь между длительным приемом препаратов, содержащих фосфор, и развивающимися патологическими переломами и их осложнениями. Очевидно, что развивающимся осложнениям способствует химическая активность бисфосфонатов, угнетающая и подавляющая обменные процессы в костной ткани, сопровождающиеся повышением степени минерализации и как следствие хрупкости кости.
Выводы
1. Для своевременной профилактики описанных осложнений производителям необходимо расширить инструкцию по медицинскому применению бисфосфанатов, в разделы «Предостережения» внести рекомендации о регулярном, не менее одного раза в три месяца, проведении рентгенологического обследования костей лицевого скелета.
2. Среди лиц, употребляющих синтетические наркотические препараты, в обязательном порядке, кроме регламентированных обследований на опасные инфекции, проводить рентгенологическое обследование челюстных костей.
3. Раздел «Побочные реакции» дополнить информацией о риске патологических переломов с указанием возможных предшествующих перелому симптомах: беспричинная зубная боль, боль в области бедра, общей слабости или дискомфорте.
Рецензенты:
Гарус Я.Н., д.м.н., профессор кафедры пропедевтики стоматологических заболеваний ГБОУ ВПО «Ставропольский государственный медицинский университет» Минздрава России, г.Ставрополь.
Калиниченко А.А., д.м.н., главный врач стоматологической клиники «Фитодент», г.Михайловск.



