Введение
Обширный род Ре1аrgоnium L. семейства Gегaniасеае включает 250 видов. Родиной Пеларгонии является Капская провинция Южной Африки. В XVII веке Пеларгонии были завезены в Европу, а затем в США, и были введены в культуру как декоративные и эфиромасличные растения [1; 2].
Немногочисленные фармакогностические исследования, найденные в доступной литературе, показали наличие таких БАВ в эфирном масле рода Pelargonium, как цитронеллол (65–70 %) и гераниол, а также терпенеол, линалоол, борнеол (терпеновые спирты), терпены (а-пинен, фелландрен), эфиры (уксусной, бутановой, валериановой, муравьиной кислот), кетоны, фенол – эвгенол [4; 10].
Растения рода Pelargonium L. используются для лечения острых и хронических инфекционно-воспалительных заболеваний дыхательных путей и ЛОР-органов в форме оригинального экстракта EPs® 7630 (EPs® 7630 является зарегистрированной торговой маркой компании Dr.Willmar Schwabe, г. Карлсруэ, Германия) [6; 7; 9]. Изолированный экстракт надземной части растения обладает выраженной антиоксидантной активностью, сопоставимой с тимолом [10], может использоваться при лечении алкогольного поражения печени [8].
Цель исследования
Определение внешних признаков надземной части P. zonale, изучение анатомического строения с целью установления диагностических признаков сырья, а также проведение предварительного химического анализа и стандартизация полученного фитопрепарата.
Материалы и методы исследования
В качестве растительного сырья использовали соцветия и листья, собранные в фазе цветения многолетнего культивируемого травянистого растения Pelargonium zonale, сем. Geraniaceae.
Сырье для приготовления фитопрепарата использовали свежее.
Для получения настойки использовали спирт этиловый 40 % концентрации.
При проведении макроскопического анализа в качестве объекта исследования выступило всё растение целиком Пеларгонии зональной.
Для определения микроскопических признаков был изготовлен препарат Пеларгонии зональной листа с поверхности, помещенный между двумя стеклами (предметным и покровным), заключенный в хлоралгидрат. Пеларгонии зональной настойку получали методом мацерации (ГФ XI, вып. 2, с. 148-149). Для установления необходимого соотношения сырья и экстрагента был проведен анализ на наличие алкалоидов в свежем растительном сырье с применением общеалкалоидных осадительных реактивов. Определение содержания этанола, сухого остатка, общей золы, золы нерастворимой в хлористоводородной кислоте, проводили по методикам (ГФ XI, вып. 1, с. 24, 165). Количественный анализ извлечения проводили по сумме окисляемых веществ методом перманганатометрии (ГФ XI, вып.1, с. 285). Качественный состав природных соединений, содержащихся в настойке, исследовали с помощью хроматографических и спектральных методов анализа. Использовали следующие системы растворителей для бумажной хроматографии:
3 %, 15 % кислота уксусная; н-бутанол – кислота уксусная – вода (4:1:2) БУВ (4:1:5); хлороформ – этанол – вода (8:2:0,1); хлороформ – этанол – кислота муравьиная (30:2:0,15); бензол-этанол (8:2); н-бутанол – 25 % уксусная кислота (1 : 1); этилацетат-петролейный эфир (3:1).
для двумерной бумажной хроматографии:
первое направление
н-бутанол-кислота уксусная-вода (4:1:5),
второе направление
15%-ная кислота уксусная.
Обнаружение пятен веществ на хроматограммах проводили, используя следующие реактивы: Гепфнера, свежеприготовленные диазосоединения в растворе натрия карбоната, 2 % спиртовый раствор железа хлорида (III), 0,5 н. спиртовый раствор калия гидроксида, пары аммиака (25 %-ный водный раствор), 2 %-ный раствор натрия боргидрида с кислотой хлороводородной концентрированной, 5 % спиртовый раствор алюминия хлорида.
Фенольные соединения на хроматограммах обнаруживали по характеру свечения в УФ-свете в диапазоне длин волн 190–500 нм до и после обработки различными реактивами. Электронные спектры соединений в УФ области снимали на приборе СФ-2000 (Россия) в кюветах с толщиной поглощающего слоя 1 см; в качестве растворителя использовали 40 %-ный этанол. Гипогликемический эффект рассматривался у нелинейных крыс на фоне смоделированного аллоксаном («Alpha Aesar®») сахарного диабета. Диабет моделировали однократным внутрибрюшинным введением аллоксана в дозе 170 мг/кг. Концентрацию глюкозы в крови животных определяли глюкозооксидазным методом с использованием набора «Фотоглюкоза» (ООО «Импакт») до введения, а также через 120 минут после введения исследуемых веществ. Критерием включения животных с аллоксановым диабетом в эксперимент служил уровень глюкозы в крови в пределах 10-12 ммоль/л. Крыс лишали пищи за 16 часов до опыта и на время его проведения.
Результаты количественных исследований подвергнуты математической обработке методом вариационной статистики (Государственная Фармакопея СССР: Вып. 1, 1987).
Результаты исследования и их обсуждение
Результаты проведения качественных реакций на содержание алкалоидов представлены в таблице 1.
Таблица 1
Результаты качественных реакций на алкалоиды
|
№п/п |
Реактив |
Наблюдаемый результат |
|
1 |
Реактив Бушарда (раствор йода в иодиде калия) |
бурого осадка не наблюдается |
|
2 |
Реактив Драгендорфа (раствор йодистого висмута в присутствии йодистого калия) |
оранжевого осадка не обнаружено |
|
3 |
Реактив Майера (раствор йодистой ртути в присутствии йодистого калия) |
реакция отрицательная, осадка не наблюдается |
|
4 |
Раствор пикриновой кислоты |
желтого осадка нет |
|
5 |
Раствор танина |
бурого осадка не обнаружили |
Эксперимент показал отсутствие алкалоидов. Таким образом, листья Пеларгонии зональной, сем. Гераниевые относятся к несильнодействующему сырью (ГФ XI, вып. 1, с. 165).
Фитопрепарат, полученный методом мацерации, представляет собой жидкость светло-зеленого цвета с запахом гераниола. Концентрация этанола в настойке составила 49,8 % в объёмных долях; % содержание сухого остатка составило 0,89 %, показатель содержания тяжелых металлов соответствует требованиям к данной лекарственной форме, указанным в статье «Настойки» Государственной Фармакопеи XI (ГФ XI, вып. 1, с. 165). Содержание окисляемых веществ в процентах в пересчете на абсолютно сухое сырье составило 9,00±1,55 %.
Электронные спектры соединений в УФ области снимали на приборе СФ-2000 (Россия) в кюветах с толщиной поглощающего слоя 1 см; в качестве растворителя использовали 40 % спирт этиловый (рисунок 1).
Область поглощения спектра – УФ; диапазон длин волн 200–600 нм.
Оптическая плотность, А (lg(F0/F))
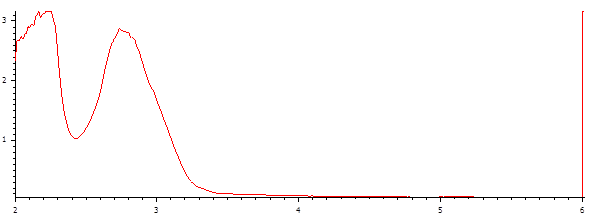
Длина волны, λ (нм)
Рис. 1. Электронный спектр Пеларгонии настойки
Пик, проявивший в диапазоне 230–300 нм оптическую активность, позволяет нам утверждать о наличии аминокислот.
Результаты качественных химических реакций на основные группы биологически активных соединений представлены в таблице 2.
Таблица 2
Результаты качественных реакций
|
№п/п |
Реакция |
Наблюдаемый результат |
|
1 |
Проба Синода |
Слабо-желтое окрашивание |
|
С конц. HCl |
Окраска не изменилась |
|
|
2 |
С 10 % раствором натрия гидроксида |
Желтое окрашивание |
|
3 |
С 2 % раствором алюминия хлорида |
Ярко-желтое окрашивание |
|
4 |
С 1 % водным раствором железа хлорида (III) |
Буро-зеленое окрашивание |
|
5 |
Реакция пенообразования |
Пенообразование не наблюдалось |
|
6 |
Холестерин |
Осадка не обнаружено |
|
7 |
Реакция Сальковского |
Оранжевое окрашивание, переходящее в красное, не наблюдалось |
|
8 |
Реакция Либермана – Бурхарда |
Сине-фиолетовое окрашивание, переходящее в зеленое, не наблюдалось |
|
9 |
«Лактонная» проба |
Желтое окрашивание в пробирке с раствором натрия гидроксида не обнаружено |
|
10 |
Реакция образования азокрасителя |
Красное окрашивание не обнаружено |
|
11 |
С кислотой азотной концентрированной |
Желтое окрашивание |
|
12 |
С железо-аммониевыми квасцами |
Черно-синее, черно-зеленое окрашивание и осадок не наблюдались |
|
13 |
С раствором 10 % уксусной кислоты и раствором 10 % средней соли ацетата свинца |
Черно-зеленое окрашивание фильтрата не наблюдалось |
Таким образом, результаты скринингового фитохимического анализа позволяют сделать предположение, что в свежих листьях Пеларгонии зональной из основных групп биологически активных веществ содержатся флавоноиды и вещества белковой природы.
Результаты хроматографирования показали, что при одномерном хроматографировании из использованных систем растворителей разделение происходит в системах н-бутанол – уксусная кислота – вода (4:1:2); 3 % раствор уксусной кислоты; н-бутанол – 25 % уксусная кислота (1:1).
В ходе исследования химического состава извлечения листьев свежих Пеларгонии зональной методом двумерной бумажной хроматографии в системе н-бутанол-кислота уксусная-вода БУВ (4:1:5) – первое направление и 15 %-ный раствор кислоты уксусной – второе направление, разделение биологически активных веществ не было обнаружено.
Результаты хроматографических исследований представлены в таблице 3.
Таблица 3
Результаты идентификации веществ фенольной природы
|
Величина Rf |
Видимый свет,
|
Свечение в УФ |
Наименование |
Величина Rf**
|
|
|
До проявления |
После проявления* |
|
|||
|
0,85 |
Бесцветная |
Бледно-фиолетовая |
Коричневая (диазосульфокислота) |
Арбутин |
0,85 I
|
|
0,80 |
Коричневая |
Голубая |
Усиление окраски (пары аммиака) |
Кофейная кислота |
0,82 I 0,26 II 0,78 III |
|
0,62 |
Синяя |
Светло-голубая |
Синяя (р-в Паули) |
Галловая кислота |
0,62 I
|
* В скобках указаны реактивы для проявления хроматограмм;
**Цифрами обозначены системы растворителей для хроматографирования: I – н-бутанол – уксусная кислота – вода (4 : 2 : 1) – БХ; II – 3 % раствор уксусной кислоты – БХ; III – н-бутанол – 25% уксусная кислота (1 : 1) – БХ [3; 5].
По величине Rf, окраске пятен в УФ и при обработке хромогенными реактивами установлено, что в сравнении с величиной Rf свидетелей обнаруженные пятна исследуемого фитопрепарата относятся к классу фенолкарбоновых кислот и гликозидов и являются: 1-арбутин, 2-кофейная кислота, 3-галловая кислота.
Проведенные исследования свидетельствуют о наличии в извлечении из листьев свежих Пеларгонии зональной фенолокислот: кофейной, галловой, а также арбутина и веществ белковой природы.
Также был установлен дозозависимый гипогликемический эффект Пеларгонии настойки. Результаты исследования представлены в таблице 4.
Таблица 4
Влияние Пеларгонии настойки на уровень глюкозы при аллоксановом диабете
|
Серии опытов |
Доза от LD50 |
Количество животных |
Уровень глюкозы, моль/л |
% торможения гликемии |
|
|
фон |
120 мин |
|
|||
|
Контроль 1 (интактные крысы) |
- |
6 |
4,1+0,1 |
3,93+0,1 |
- |
|
Пеларгонии настойка |
0,1 |
6 |
4,08+0,1 |
4,00+0,1 |
- |
|
Контроль 2 (алоксановый диабет) |
- |
6 |
11,87+0,3 ***1 |
11.85+0,3 ***1 |
0,00+0,0 |
|
Пеларгонии настойка (аллоксановый диабет) |
0,1 |
6 |
11,80+0,5 |
8,40+0,3 ***1, ***2, ***3 |
28,81+2,5 ***2 |
|
|
0,01 |
6 |
12,22+0,3 |
10,01+0,2 ***1, ***2, ***3 |
17,34+1,8 ***2, **4 |
|
|
0,001 |
6 |
11,70+0,3 |
10,60+0,4 ***1, *2 |
9,40+2,5 **2 |
Примечание: *** = P<0,001, ** = P<0,01, * = P<0,05.
1 – по сравнению с контролем 1;
2 – по сравнению с контролем 2;
3 – по сравнению с фоном;
4 – по сравнению с Пеларгонии настойкой в дозе 1/10 LD50.
Выводы
Проведенные исследования свидетельствуют о наличии в извлечении из листьев свежих Пеларгонии зональной фенолокислот: кофейной, галловой, а также арбутина и веществ белковой природы. Полученное извлечение Пеларгонии зональной настойка обладает самостоятельным дозозависимым гипогликемическим эффектом, что открывает новые перспективы использования данного растительного сырья.
Рецензенты:
Белоногова В.Д., д.фарм.н., профессор, заведующая кафедрой фармакогнозии с курсом ботаники ГБОУ ВПО «Пермская государственная фармацевтическая академия» Министерства здравоохранения Российской Федерации, г. Пермь.
Ларионов Л.П., д.м.н., профессор кафедры фармакологии и клинической фармакологии ГБОУ ВПО «Уральский государственный медицинский университет» Министерства здравоохранения Российской Федерации, г. Екатеринбург.



