Цель данной работы – исследование по разработке методик качественного и количественного анализа лекарственного препарата «Солодки сироп».
Материал и методы исследования
В качестве объектов исследования служили промышленные образцы лекарственного препарата «Солодки сироп» (ОАО «Татхимфармпрепараты»), а также образцы данного препарата, полученные в лабораторных условиях из корней солодки голой (Glycyrrhiza glabra L.) и солодки уральской (Glycyrrhiza uralensis Fisch.). В качестве стандартных образцов использованы глицирризиновая кислота, глицирам и ликуразид.
В работе использованы тонкослойная хроматография (пластинки «Сорбфил ПТСХ-АФ-А-УФ») в системе растворителей хлороформ – этиловый спирт – вода (26:16:3). Детекцию веществ на хроматограммах осуществляли просмотром пластинок в видимом и ультрафиолетовом свете (длина волны 254 нм и 366 нм). Регистрацию УФ-спектров исследуемых растворов проводили с помощью спектрофотометра «Specord 40» (Analytik Jena).
Результаты исследования и их обсуждение
Для достижения поставленной цели нами были изучены условия хроматографического разделения сапонинов и флавоноидов лекарственного препарата «Солодки сироп», позволяющие обнаруживать доминирующие биологически активные соединения (БАС) – глицирризиновую кислоту и ликуразид. Для достоверного определения веществ нами предложено использовать государственные стандартные образцы – глицирам (моноаммониевая соль глицирризиновой кислоты) (сапонин) и ликуразид (флавоноид). Использование данных стандартов позволяет исключить ошибки при идентификации диагностических веществ и, следовательно, обеспечивать валидацию методик качественного анализа сырья и препаратов солодки. Использование в качестве ГСО глицирама объясняется тем, что глицирризиновая кислота – вещество нестабильное [5], что препятствует использованию данного соединения в качестве государственного стандартного образца.
Установлено, что на хроматограмме сиропа солодки (рис. 1) ликуразид обнаруживается в виде доминирующего желтого или желтовато-оранжевого пятна с величиной Rf около 0,5, а глицирризиновая кислота – в виде фиолетового флуоресцирующего пятна (254 нм) с величиной Rf около 0,3 (на уровне ГСО глицирама). При этом обнаруживаются также пятна других БАС (рис. 1).
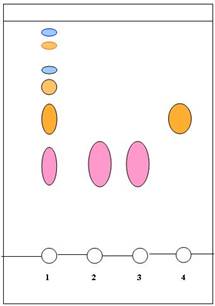
Рис. 1. Хроматографический профиль веществ препарата «Солодки сироп».
Обозначения: 1.Лекарственный препарат «Солодки сироп», 2.Глицирам, 3.Глицирризиновая кислота, 4.Ликуразид
Для целей количественного анализа предложено, как и в случае корней и экстракта солодки [3, 4, 8], использование двух показателей – содержания глицирризиновой кислоты (в пересчете на глицирам) и содержания суммы флавоноидов (в пересчете на ликуразид). При количественном определении содержания глицирризиновой кислоты в электронном спектре испытуемого раствора содержится один интенсивный максимум поглощения при длине волны 258+2 нм (рис. 2), коррелирующий с таковым глицирризиновой кислоты и глицирама [4, 5]. Для определения суммы флавоноидов, как и в случае корней и экстракта солодки, предложены подходы к стандартизации, заключающиеся в использовании дифференциальной спектрофотометрии при аналитической длине волны 420 нм [8]. При этом в УФ-спектре раствора сиропа солодки в присутствии AlCl3 в условиях дифференциальной спектрофотометрии (рис. 3), как и в случае ГСО ликуразида, наблюдается интенсивный максимум поглощения при длине волны 420 нм (рис. 4).
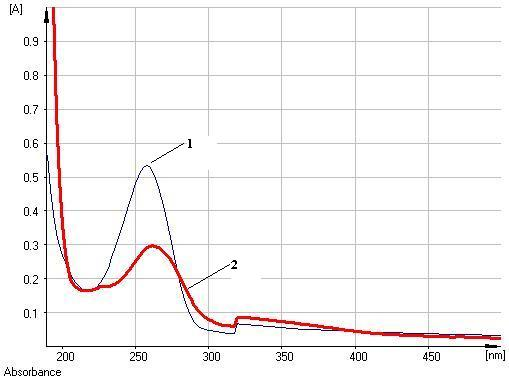
|
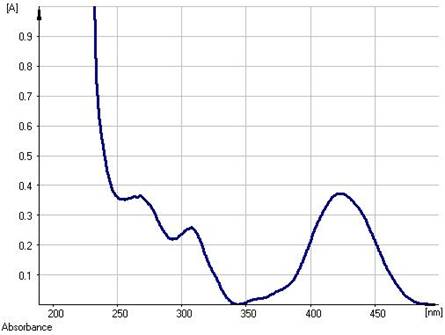
Рис. 3. УФ-спектр испытуемого раствора лекарственного препарата «Солодки сироп» (дифференциальный вариант)
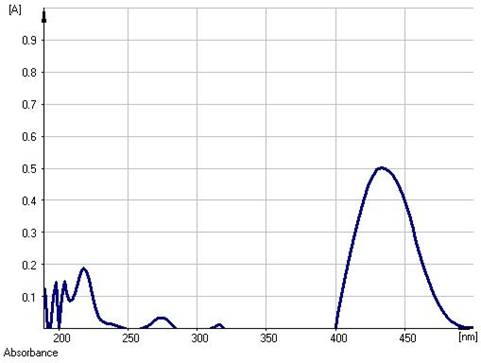
Рис. 4. УФ-спектр раствора ГСО ликуразида (дифференциальный вариант)
1. Методика качественного анализа лекарственного препарата «Солодки сироп». К 5,0 мл препарата «прибавляют 1 каплю ледяной уксусной кислоты и перемешивают. Затем прибавляют 5 мл ацетона и перемешивают. Ацетоновый (верхний) слой отделяют, упаривают в выпарительной чашке, растворяют в 1 мл 95 % спирта этилового и используют для анализа (испытуемый раствор). На линию старта пластинки «Сорбфил-ПТСХ-УФ-А-УФ» микропипеткой наносят 0,02 мл испытуемого раствора и затем рядом – 0,02 мл (20 мкг) 0,1 % раствора ГСО глицирама и 0,02 мл (20 мкг) 0,1% раствора ГСО ликуразида. Далее анализ осуществляют в соответствии с методикой, описанной в литературе [3, 4].
2. Методика количественного определения глицирризиновой кислоты в лекарственном препарате «Солодки сироп». Около 5 г (точная навеска) препарата помещают в колбу коническую со шлифом вместимостью 250 мл, прибавляют 25 мл раствора ацетонового 3 % кислоты трихлоруксусной, перемешивают, присоединяют к обратному холодильнику и нагревают на кипящей водяной бане 20 мин, считая с момента закипания раствора в колбе. В колбу через холодильник прибавляют 30 мл раствора ацетонового 3 % кислоты трихлоруксусной, раствор охлаждают и фильтруют через бумажный фильтр. Колбу промывают раствором ацетоновым 3 % кислоты трихлоруксусной 2 раза по 10 мл, фильтруя через тот же фильтр. Далее анализ осуществляют в соответствии с методикой, описанной в литературе [3, 4].
Содержание глицирризиновой кислоты (в пересчете на глицирам) в образцах сиропа солодки варьирует от 0,71 %+0,01 % до 1,33 %+0,03 %. Ошибка единичного определения методики с доверительной вероятностью 95 % составляет +4,97 %.
3. Методика количественного определения суммы флавоноидов в лекарственном препарате «Солодки сироп». Около 5 г (точная навеска) препарата помещают в мерную колбу вместимостью 25 мл и доводят объем раствора водой очищенной до метки (раствор А). 2 мл раствора А помещают в мерную колбу вместимостью 25 мл и доводят объем раствора 96% этиловым спиртом до метки (раствор сравнения). 2 мл раствора А вносят в мерную колбу вместимостью 25 мл, прибавляют 2 мл 2 % спиртового раствора хлорида алюминия и доводят объем раствора до метки объем 96 % этиловым спиртом (испытуемый раствор). Далее анализ осуществляют в соответствии с методикой, описанной в литературе [8].
Содержание суммы флавоноидов в образцах лекарственного препарата «Солодки сироп» варьирует от 0,18 %+0,001 % до 0,21 %+0,002 %. Ошибка единичного определения методики с доверительной вероятностью 95 % составляет +4,85 %.
Выводы
1. Разработаны новые подходы к стандартизации лекарственного препарата «Солодки сироп», основанные на использовании ТСХ, спектрофотометрии, а также государственных стандартных образцов глицирама и ликуразида.
2. Разработана методика качественного ТСХ-анализа лекарственного препарата «Солодки сироп», заключающаяся в определении глицирризиновой кислоты и ликуразида, имеющих диагностическое значение.
3. Разработаны методики количественного определения глицирризиновой кислоты и суммы флавоноидов в лекарственном препарате «Солодки сироп» с использованием спектрофотометрии при аналитической длине волны 258 нм и 420 нм соответственно.
Рецензенты:Первушкин С.В., д.фарм.н., профессор, зав. кафедрой фармацевтической технологии, государственное бюджетное образовательное учреждение высшего профессионального образования «Самарский государственный медицинский университет» Министерства здравоохранения Российской Федерации, г. Самара;
Авдеева Е.В., д.фарм.н., профессор, зам. директора Института инновационного развития, государственное бюджетное образовательное учреждение высшего профессионального образования «Самарский государственный медицинский университет» Министерства здравоохранения Российской Федерации, г.Самара.



