Черепно-мозговая травма (ЧМТ) возникает как следствие прямого механического воздействия на мозг, вызывает дегенерацию и гибель клеток в центральной нервной системе (ЦНС), что приводит к расстройству передачи нервных импульсов, и, в свою очередь, становится причиной потери памяти. Отсутствие существенных успехов в эффективности медикаментозной терапии, резко ограниченные собственные резервные возможности головного мозга в отношении восстановления нервных клеток вызывают высокий научный интерес к разработке принципиально новых методов лечения тяжелой ЧМТ. Одним из наиболее перспективных методов может стать нейротрансплантация стволовых или прогениторных клеток [9]. Восстановление функций возможно за счет интеграции трансплантированных клеток в областях повреждения и стимуляции компенсаторно-восстановительных процессов в патологически измененных клетках реципиента. В России имеется небольшой опыт применения стволовых клеток для лечения ТГМ [3, 4, 5]. Проведен ряд трансплантаций малодифференцированных нейральных и кроветворных клеток больным с тяжелыми черепно-мозговыми травмами [2]. Было показано, что клеточная терапия почти в 4 раза снижает число неблагоприятных исходов и обеспечивает хорошее восстановление почти у половины пациентов, участвовавших в клинических испытаниях [1].
Актуальным направлением работ является разработка адекватных носителей для трансплантируемых клеток. Клинические и экспериментальные эффекты трансплантации клеток в составе трехмерных носителей на основе синтетических биодеградируемых материалов изучены недостаточно. В основном в литературе на первый план выходит проблема адекватных носителей, поддерживающих выживание, пролиферативную активность, способность к миграции трансплантируемых клеток. В тоже время искусственный носитель должен достаточно долгое время находиться в ткани мозга реципиента при трансплантации для того, чтобы стволовые клетки, поддерживая свой фенотип, могли выселяться в прилежащие ткани, стимулируя в них посттравматическое выживание нейронов и рост нервных волокон.
Цель исследования – изучить биосовместимость биодеградируемого трехмерного скаффолда на основе модифицированного гиалуроновой кислотой хитозана в экспериментах с открытой травмой мозга мышей.
Материалы и методы исследования
Работа выполнена на 8-10 недельных аутбредных мышах самцах линии C57BL/6 массой 20-22 г. (n=40). Основные правила содержания и ухода за экспериментальными животными соответствовали нормативам, данным в Приказе Минздрава России № 708н от 23.08.10 «Об утверждении Правил лабораторной практики» и были согласованы с этическим комитетом при ГБОУ ВПО НижГМА Минздрава России.
3D биодеградируемый скаффолд был создан с использованием микростереолитографической техники путем комбинации модифицированного хитозана (Поли[(1 ? 4)-2-амино-2-деокси-?-D-глюкоза]) [6] и высокомолекулярной гиалуроновой кислоты [10].
Моделирование открытой черепно-мозговой травмы (ЧМТ) проводилось «weight-drop» способом [8] по оригинальной методике. Механическую травму наносили путем падения груза с тупой поверхностью, что обеспечивает ускорение головы при минимальном локальном воздействии в точке приложения травмирующей силы. Использование данной модели наиболее полно воспроизводит клиническую картину очагового повреждения, в том числе ушиба головного мозга, и позволяет изучать, помимо локальных, травматические изменения, сопровождающиеся вторичной гибелью нервных клеток в отдаленных отделах мозга, чувствительных к травме, таких как гиппокамп, зубчатая извилина, зрительный бугор, а также оценивать грубые двигательные нарушения, изменения тонкой координации движений, дефицит когнитивных функций.
Перед нанесением травмы, под изофлурановым наркозом фиксировали в стереотаксической установке для мышей «Narishige» (Япония). Голову животного прижимали к стальной пластине для избежания перелома челюсти и достижения горизонтального расположения свода черепа к торцевому участку груза. Затем на коже головы, свободной от шерсти, делали разрез и производили трепанацию фрезой костей черепа (d 4 мм, Bregma 0.82 mm). Твердая мозговая оболочка оставалась неповрежденной. Груз, представляющий собой стальной цилиндр, поднимался на заданную высоту, затем сбрасывался и наносил удар по области трепанационного окна (диаметр ударной части, соответствующей трепанационному окну, 3 мм; масса груза 4 грамма; высота поднятия груза 0,80 метра). После нанесения травмы в подлежащем мозговом веществе возникали повреждения в виде разрыва ТМО, образование очагов геморрагического ушиба или размозжения мозгового вещества, характерные для тяжелой черепно-мозговой травмы. После операции кожу животных ушивали, шов обрабатывали антисептическим раствором.
В ходе эксперимента животные случайным образом были разделены на группы: первая группа – интактные животные (n=10), вторая – контроль (ложнооперированные) животные (n=10), третья группа – контрольные животные (n=6), четвертая – опытные (n=5). Мышам контрольной и опытной групп на седьмые сутки после моделирования ЧМТ в очаг повреждения имплантировали либо забуференный физиологический раствор (PBS, 30 µl), либо биодеградируемый 3D скаффолд (размер 2х1 мм), соответственно. В группе ложнооперированных животных проводили те же процедуры (анестезия, трепанация костей черепа), за исключением моделирования ЧМТ и трансплантации. Мыши интактной группы не подвергались анестезии, моделированию ЧМТ и трансплантации.
Морфо-функциональными параметрами оценки биосовместимости скаффолда in vivo являлись визуализациия целостности ткани мозга с помощью МРТ и тестирование когнитивного поведения мышей.
Для морфологической оценки биосовместимости разработанных скаффолдов с тканями мозга мыши [7] применены методы высокопольной МРТ на томографе Agilent Technologies DD2-400 9.4 T (400 MHz) с объемной катушкой M2M (Н1). При томографии мозга мыши проводился мониторинг физиологических параметров животных, таких как температура, дыхание, ЭКГ на оборудовании фирмы SA Instruments с использованием программы PC-SAM при температуре окружающей среды 37оС. Для получения Т2-взвешенных изображений использовалась импульсная последовательность MGEMS (multi gradient echo multi slice). MGEMS – стандартная последовательность (была предустановлена в программе VnmrJ, работающей с томографом) для создания анатомических изображений, которая заключается в использовании вместо фокусирующего 180-градусного радиочастотного импульса двух биполярных импульсов градиентного магнитного поля. Время повторения (TR) - 1000 мс, время эхо (TE, TE2) – от 1.5 до 2 мс, количество эхо от 6 до 8, угол поворота (flip angle) 90, размер матрицы 128х128, количество срезов 15, толщина срезов составляла 1 мм, поле зрения от 20х20 мм2. Общая длительность последовательности была 8 мин 32 сек.
Для функциональной оценки нарушений процессов обучения у животных на 10 сутки посттравматического периода вырабатывали условный рефлекс пассивного избегания (УРПИ). Установка (Shuttle Box LE895, PanLab / Harvard Apparatus Испания; Stoelting, США) состояла из камеры (46x27x25) с электрифицированным решетчатым полом, разделенной на два отсека скользящей дверцей. Для электрической стимуляции использовался источник с фиксированным сопротивлением (LE100/26 Harvard Apparatus Испания; Stoelting, США). Подача электрокожного раздражения, положение дверки между отсеками и латентное время перехода в темный отсек, измеряемое с момента помещения животного в светлый отсек камеры, контролировались программой Shutavoid v1.8.03 (PanLab / Harvard Apparatus Испания; Stoelting, США). Регистрировали латентное время перехода (ЛВП) в темный отсек камеры при открытой дверке между отсеками. Тест заканчивался, когда животное вступало в темный отсек или если животное не делало этого в течение 3 минут. Функции долговременной памяти изучали, оценивая сохранность у мышей УРПИ на 30 сутки.
Для исследования нарушений функций непространственной гиппокамп опосредованной кратковременной памяти применяли тест распознавания нового объекта. Тест состоял из трех этапов: привыкание, обучение и тестирование. На 23 и 24 дни после моделирования ЧМТ животных помещали в центр квадратной арены (45х45х40 см) (LE802S PanLab / Harvard Apparatus Испания; Stoelting) на 10 минут для привыкания и уменьшения стресса, во время которого животные исследовали пустую арену. На 25 день на арену помещали два одинаковых объекта, расположенных на равном расстоянии. Мышей помещали в центр поля на 10 минут для исследования объектов (обучение). Через 24 часа животных снова помещали в центр арены с одним знакомым объектом и одним новым для регистрации исследовательского поведения в течение 10 минут (тестирование). В ходе эксперимента на этапах обучения и тестирования регистрировали совокупное время исследования знакомого и нового объектов. Исследовательское поведение включало реакции принюхивания (направление носа к объекту на расстоянии не более 2 см, касание объекта). Во время обучения и тестирования памяти поведение животных считали исследовательским, если реакции по отношению к объектам составляли не менее 10 секунд. Видеорегистрация отдельных поведенческих актов поведения животных осуществлялась с помощью видеокамеры SONY SSC-G118 (Япония). Регистрация и анализ данных контролировались программой Smart v.3.0.03. (Panlab Harvard Apparatus Испания; Stoelting, США). Состояние функций памяти определяли, как дискриминационное время исследования нового объекта (DIR) по формуле:
Dir = [(доля времени исследования животным нового объекта – доля времени исследования знакомого объекта во время сеанса тестирования) / общее время исследования во время сеанса тестирования] х 100.
Полученные результаты обрабатывались с помощью пакетов прикладных программ Statistica 5.5. Данные были проверены на нормальность распределения с помощью W-критерия Шапиро-Уилка. При малых объемах выборки (n?10) применяли непараметрические критерии: для двух зависимых выборок - критерий Вилкоксона, в случае двух независимых выборок – критерий Манна—Уитни. Различия между группами считали статистически достоверными при уровне значимости р<0,05.
Результаты исследования и их обсуждение
Полученные результаты поведенческих тестов свидетельствовали о нарушении у животных контрольной группы вследствие ЧМТ головного мозга способности к обучению. Во время сеанса обучения в контрольной группе мышей латентное время перехода (ЛВП) достоверно превышало аналогичные показатели интактной и контрольной группы ложнооперированных животных (p<0,05), что обусловлено нарушением моторных функций ЦНС в результате ЧМТ. Через 24 часа после обучения латентное время перехода в темный отсек камеры в данной группе достоверно не отличалось от ЛВП при обучении (p>0,05) (рис. 1).
Через 24 часа после сеанса обучения в группе животных с имплантированием в очаг повреждения биодеградируемого хитозанового скаффолда, также как в интактной и контрольной группе ложнооперированных животных, ЛВП в темный отсек камеры статистически значимо увеличивалось по отношению ко времени при обучении (p<0,05). Кроме того, в опытной группе с имплантированием в очаг повреждения скаффолда ЛВП в 1,82 раза (p<0,05) превышало время перехода животных контрольной группы с введением в очаг повреждения раствора PBS (рис. 1).
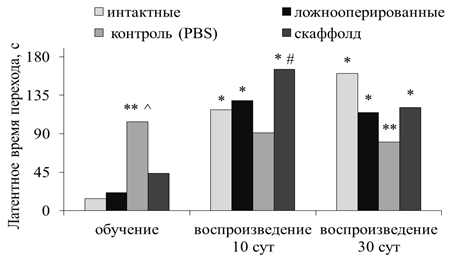
Рис. 1. Исследование способности к обучению и воспроизведению УРПИ мышей линии С57BL/6 в посттравматическом периоде
* - p<0,05 по отношению к латентному времени перехода в темный отсек при обучении, критерий Вилкоксона; # - p<0,05 по отношению к контрольной группе животных, критерий Манна-Уитни; ** - <0,05 по отношению к интактной группе животных, критерий Манна-Уитни; ^ - <0,05 по отношению к контрольной группе ложнооперированных животных, критерий Манна-Уитни
Функции долговременной памяти оценивали по способности животных к воспроизведению УРПИ на 30 сутки посттравматического периода. В группе мышей с имплантированием через неделю после моделирования ЧМТ в очаг повреждения биодеградируемого хитозанового скаффолда, ЛВП в темный отсек камеры достоверно превышало время при обучении (p<0,05), также как в интактной и контрольной группе ложнооперированных животных. И не отличалось от времени при проверке сохранности условнорефлекторного навыка на 10 сутки посттравматического периода (p>0,05).
Функции кратковременной памяти мышей оценивали в тесте «распознавания нового объекта» (NOR, Novel object recognition test) на 23-25 сутки посттравматического периода.
Анализ полученных результатов показал, что моделирование ЧМТ у животных контрольной группы приводило к значительным нарушениям гиппокамп зависимой кратковременной памяти. На этапе тестирования длительность исследовательского поведения нового объекта не превышала время исследования знакомого объекта. Дискриминационное соотношение исследования в контрольной группе с введением в очаг повреждения раствора PBS было достоверно меньше показателей интактной и контрольной группы ложнооперированных животных (p<0,05) (рис 2).
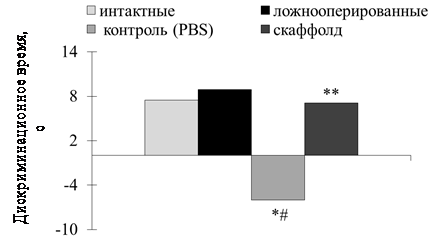
Рис. 2. Исследование функций кратковременной памяти мышей линии С57BL/6 в посттравматическом периоде
* - p<0,05 по отношению к интактной группе; критерий Манна-Уитни; # - p<0,05 по отношению к группе ложнооперированных животных; критерий Манна-Уитни; ** - p<0,05 по отношению к контрольной группе животных (PBS); критерий Манна-Уитни
У мышей группы с имплантированием на 7 сутки после моделирования ЧМТ в очаг повреждения биодеградируемого хитозанового скаффолда время исследования нового объекта на этапе тестирования превышало время исследования знакомого объекта. Дискриминационное соотношение длительности исследования не отличалось от соотношения времени интактной и контрольной группы ложнооперированных животных (p>0,05), но в то же время статистически значимо превышало показатель контрольной группы с введением в очаг повреждения раствора PBS (p<0,05), что свидетельствует о восстановлении функций СА1-СА3 полей гиппокамп зависимой кратковременной памяти распознавания (рис. 2).
Данные МРТ, полученные через 5 месяцев после перенесенной травмы показали, что ткань, образованная в месте введения скаффолда, сравнима с неповрежденной тканью головного мозга по интенсивности томограммы. В области очага не наблюдалось накопления жидкости, что выражалось бы в гиперинтенсивном сигнале и пересвеченной области на МРТ-изображении. Также в области травмы отсутствовало уплотнение ткани, о котором мог бы свидетельствовать гипоинтенсивный сигнал и спад интенсивности (затемнение). На рис. 3 (а, б, в) представлены МРТ-срезы головного мозга интактных мышей (а), мышей с инъекцией PBS-раствора (б) и мышей с внедренным в очаг повреждения биодеградируемым хитозановым скаффолдом (в). Как видно из рис. 3 мозг мыши со скаффолдом структурно не изменен и сравним с МРТ интактного мозга.

Рис. 3 МРТ-изображения срезов головного мозга интактных мышей (а), мышей с инъекцией в очаг повреждения PBS-раствора (б) и мышей с имплантируемым в очаг повреждения биодеградируемым хитозановым скаффолдом (в). Т2-взвешенные изображения получены с использованием импульсной последовательности MGEMS. Стрелками указана область травмы
Выводы:
1. Через 5 месяцев после нейротрансплантации биодеградируемого скаффолда на основе модифицированного хитозана в комплексе с гиалуроновой кислотой по данным МРТ в области очага повреждения обнаружено образование однородной ткани, которая по интенсивности сравнима с интактной тканью, не имеет выраженной границы с интактной тканью, не накапливает жидкость и не имеет уплотнений.
2. ЧМТ головного мозга приводит к нарушению процессов обучения и долговременной памяти при формировании УРПИ, а также функций кратковременной памяти в посттравматическом периоде;
3. Имплантация через неделю после моделирования ЧМТ в очаг повреждения биодеградируемого хитозанового скаффолда оказывала положительное действие на способность животных к обучению условным рефлексам на 10 сутки и актуализации следов кратковременной и долговременной памяти в отдаленном периоде.
Заключение
При моделировании ЧМТ у животных, вследствие нарушения неврологических функций, двигательного и эмоционального поведения, нарушалась способность к обучению, что согласуется с данными литературы. Поведенческие тесты выявили существенные улучшения восстановления когнитивных и моторных функций ЦНС у животных на фоне проведенной нейротрансплантации. Имплантирование через неделю после моделирования ЧМТ в очаг повреждения биодеградируемого о скаффолда оказывало протекторное действие, восстанавливая, вероятно, синаптическую пластичность нейронов головного мозга (коры, гиппокампа), лежащих в основе процессов обучения и памяти. Наблюдалось оптимизирующее действие на способность животных к обучению УРПИ на 10 сутки и актуализации следов кратковременной и долговременной памяти в отдаленном периоде.
Выявленные морфологические и функциональные параметры жизнедеятельности мышей свидетельствовали о биосовместимости биодеградируемого материала 3D скаффолда на основе модифицированного хитозана в комплексе с гиалуроновой кислотой. Интересным фактом явилось и то, что была сделана попытка частичного восстановления ткани, утраченной в результате травмы, которая в обычном случае навсегда остается невосполненной, так как на месте зоны повреждения остается киста, окруженная глиальным рубцом и заполненная ликвором. Трансплантация трехмерной оформленной биодеградируемой структуры способствовало формированию ткани мозга на месте поврежденной области при травме.
Рецензенты:
Ведунова М.В., д.б.н., зав.лабораторией по разработке методов нейропротекции Института биологии и биомедицины, ФГАОУ ВО «Национальный исследовательский Нижегородский государственный университет им. Н.И. Лобачевского» Министерства образования и науки Российской Федерации, г. Нижний Новгород;
Фраерман А.П., д.м.н., профессор ФГБУ «Приволжский федеральный медицинский исследовательский центр» Министерства здравоохранения Российской Федерации, г. Нижний Новгород



