Наследственный ангионевротический отек (НАО) – по международной статистике отек, возникающий в результате дефицита в системе С-1 комплемента, является орфанным заболеванием. Частота встречаемости 1:100000 населения [1, 2]. Характерными клиническими проявлениями являются плотные отеки в области лица, головы, верхних дыхательных путей, желудочно-кишечного тракта, сохраняющиеся от 2 до 5 суток, не купирующиеся глюкокортикостероидами, адреналином, антигистаминными средствами [3] . Об уровне распространенности НАО в регионах России, в том числе в Республике Башкортостан, где проживают 4 млн человек, неизвестно. Первые клинико-лабораторно верифицированные пациенты зарегистрированы в регистре пациентов с орфанными заболеваниями для обеспечения специфического лечения в соответствии с постановлением Правительства Российской Федерации в 2015 году.
Цель исследования: оценить анамнестические данные, особенности течения, клинические проявления, диагностику, дефицит в системе С-1 комплемента и лечение НАО на примере трех впервые выявленных клинических случаев в Республике Башкортостан.
Материал и методы исследования. Для оценки особенностей случаев ангионевротического отека представлены три клинических случая пациентов с НАО, выявленных в Республике Башкортостан. Всем пациентам проведены оценка объективного исследования, лабораторное обследование, где оценивался комплементэстеразный ингибитор С1. Проведено исследование на наличие мутаций в гене SERPING1(C1NH), ответственном за наследственный ангионевротический отек типа I и II. Осуществлен общеклинический анализ крови.
Ангиоотек (АО) – собирательное понятие, включающее в себя группу довольно распространенных заболеваний, периодически манифестирующих периферическими отеками. Считается, что 10–12% населения переболевает ангиоотеком хотя бы 1 раз в жизни [3, 4]. В группу ангиоотеков входит также заболевание, относящееся к категории редких – с частотой встречаемости менее 1:100000 населения, связанное с дефицитом в системе комплемента, относящееся при этом к жизнеугрожающим состояниям, чем и привлекает к себе особое внимание врачебного сообщества [4]. В чем же различие между этими состояниями, и какова распространенность ангиоотека, связанного с дефицитом в системе комплемента, в различных регионах России?
По данным Федеральных клинических рекомендаций ангиоотек носит остро возникающий характер, он локализован на коже или слизистых оболочек, транзиторный, склонен к рецидивированию. Важную роль в развитии АО играют брадикинин, гистамин, простагландин, они и приводят к обратимому увеличению проницаемости эндотелия сосудов. Обычно сильные проявления сохраняются от нескольких часов до нескольких дней и в большинстве случаев проходят бесследно, без дополнительной терапии [5].
При наследственном ангионевротическом отеке, связанном с дефицитом в системе комплемента (НАО), отек связан с нарушением в системе комплемента, в результате чего снижается или полностью исчезает функциональная активность комплемента С1 или отмечается его недостаточность, что приводит к накоплению брадикинина. Отеки при НАО чаще локализуются в области головы, шеи, живота и промежности, а также в области внутренних органов. Использование системных глюкокортикостероидов (сГКС) неэффективно и не позволяет купировать отек.
Система комплемента – это система каскадно действующих протеаз, которые последовательно активируются за счет отщепления и присоединения пептидных фрагментов. При активации системы комплемента против вирусной инфекции начинает участвовать фагоцитоз, который обладает хемотаксической активностью [6–9]. Ингибиторы системы комплемента содержатся в крови в более низких концентрациях, но при снижении концентрации С1-ингибитора более чем на 30% запускается каскадная реакция с активацией С1-компонента, повышением расхода С4- и С2-компонентов комплемента, синтезированием кинина, с сократительным действием, образованием брадикинина. В результате воздействия брадикинина расслабляются мышцы сосудов, увеличивается их проницаемость, что и приводит к АО [7, 8, 9]
Одним из механизмов в патогенезе НАО является активация фибринолиза, поскольку одной из функций С1-ингибитора является подавление образования плазмина из плазминогена.
Современная иммунологическая классификация разделяет все НАО на I, II, III типы. I тип (истинный НАО) составляет 80–85% всех клинических случаев. В этом случае в крови снижается концентрация С1-ингибитора от неопределяемых значений до содержания менее 30% от нормы НАО. Наследуется по аутосомно-доминантному типу. II тип составляет не более 15% всех клинических случаев НАО. В случае II типа абсолютный уровень С1-ингибитора сохраняется в пределах нормы, но при этом снижается его функциональная активность. Наследование происходит также по аутосомно-доминантному пути. III тип НАО изучен плохо, распространенность неизвестна, считается, что он связан с генетическими нарушениями контроля XII фактора свертывания крови [8]. В последние годы считается, что это не есть самостоятельный тип заболевания, а синдром, больше относящийся к другим заболеваниям.
Основными клиническими проявлениями НАО являются отеки, сохраняющиеся 2–5 дней. Наиболее вовлекаемыми органами человека являются кожа, верхние дыхательные пути и желудочно-кишечный тракт. Клинические проявления резко варьируют: от отсутствия клинических проявлений до жизнеугрожающих отеков, что проявляется человеческими и экономическими потерями. Ученые отмечают, что абдоминальные боли характерны для всех пациентов и вызваны временной кишечной непроходимостью из-за выраженного слизистого отека, в связи с чем многие пациенты с НАО подвергаются оперативным вмешательствам [9].
При установлении диагноза НАО пациент нуждается в назначении превентивного базисного лечения, которое он должен принимать ежедневно, предупреждая развитие отеков, также необходимы симптоматическое лечение для купирования приступов обострения заболеваний, обеспечение лечебного и профилактического лечения перед физически травматизирующими оперативными, в том числе стоматологическими, гинекологическими и иными, медицинскими вмешательствами. При выявлении заболевания на каждого пациента оформляется «Паспорт пациента», где описывается порядок обеспечения скоропомощных мероприятий.
Основными доступными препаратами для лечения пациентов являются: аттенуированные андрогены, антифибринолитические средства. В стационарных условиях – свежезамороженная плазма. Новыми лекарственными средствами являются Икатибант, антагонист В-2рецепторов брадикинина, который, избирательно связываясь с рецепторами, препятствует сцеплению излишне выработавшегося брадикинина с В-2 рецепторами, и Беринерт – С1 ингибитор (рекомбинантный). Препараты имеют государственную регистрацию.
Таблица 1
Основные группы препаратов для лечения НАО
|
Группа |
Механизм действия при НАО |
|
С1-NHГ (пп или рекомб.) Беринарт |
↑ недостатка активности С1-NHГ |
|
Икатибант (Фиразир) |
Блокада действия брадикинина (антагонист В2 рецепторов) |
|
Аттенуированные андрогены |
↑ концентрации С1 и С4 |
|
Антифибринолитики |
↓ образования плазмина |
|
Нативная или свежезамороженная плазма |
↑ недостатка активности С1-NHГ |
Результаты исследования и их обсуждение. Представляем вашему вниманию три клинических случая пациентов с НАО, выявленных в Республике Башкортостан. Пациентка Н., 1960 г.р., впервые обратилась за медицинской помощью к врачу аллергологу-иммунологу в 2008 г. Поводом для обращения 56-летней женщины стал предположительный диагноз: наследственный ангиоотек у ее беременной дочери при наличии жалоб на периодические отеки у мамы. При сборе анамнеза выявлено, что пациентка Н. отмечает примерно с 1980 г. (19 лет) периодическое появление отеков на лице, руках, теле, стопах, промежности. Проявления то усиливались, то уменьшались. За стационарной помощью не обращалась. В 1982 г. и в 1984 г. родила клинически здоровых детей. В последние годы беспокоят отеки, появляющиеся на разных участках тела: часто на лице, после стоматологических вмешательств отекали губы и десны. С момента обращения и установления клинического диагноза в 2008 г. до 2015 г. от приема табл. Даназол как базисного лечебного средства отказывалась.
Данные объективного исследования (15.04.2015): умеренно гиперстенического телосложения. На лице – плотный отек в области скуловой дуги, кожного зуда нет. Лимфатические узлы не пальпируются. Температура тела 36,4°С. Живот при пальпации умеренно болезненный в эпигастрии.
При лабораторном дообследовании: комплемент эстеразный ингибитор С1 (количественный) – 0,0285 г/л (норма 0,21–0,43 г/л); комплемент эстеразный ингибитор С1 (функциональный) – 10% (норма 70–130%).
Для постоянного приема была рекомендована транексамовая кислота в таблетках в дозе от 1 до 4 г в сутки. При приеме препарата в дозе более 1 г в сутки развивались боли в эпигастрии и в левом подреберье. В связи с этим продолжен ежедневный прием по 1 г в сутки, при нарастании отеков (временно) – до 4 г в сутки. Клинически препарат проявил себя как относительно эффективный. На фоне его приема снизилась частота рецидивов, но полностью исключить рецидивы отека на фоне этого препарата так и не удалось. В августе 2015 г. была экстренно госпитализирована в хирургическое отделение в связи с появлениями болей в животе. В анализах: гемоглобин 130 г/л, эритроциты – 4,25х1012 л, лейкоциты – 9,8х109 л; диастаза мочи 8 ед, белок 72 г/л, креатинин 72 мкмоль/л. Боли купированы в течение суток. Симптоматическая терапия – введение аминокапроновой кислоты или нативной плазмы, несмотря на предъявленный пациенткой паспорт больного НАО, где необходимость комплексного сопровождения наблюдения было указано – хирургами сопроводительная терапия не назначалась. В сентябре 2015 г. после консультации и заключения главного специалиста пациентка внесена в реестр пациентов с орфанными заболеваниями для получения препаратов купирования острых приступов НАО.
В число препаратов, закупаемых для пациентов, значатся Фиразир и Беринарт, аттенуированые андрогены. Алгоритм лечения пациентов представлен в таблице 2.
Таблица 2
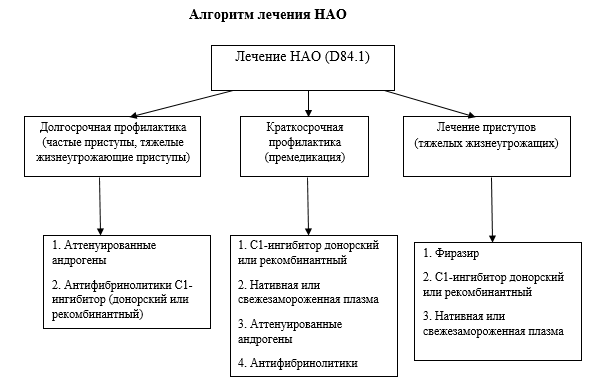
Выяснилось, что ее дочь А., 1982 г.р., имеет клинику НАО с детства: отеки на разных участках тела. Обследована у аллерголога, проводилась диагностика бытовыми аллергенами по плану диагностических мероприятий по отеку Квинке. Выявлены положительные пробы на домашнюю пыль. Проводилась аллергенспецифическая иммунотерапия (АСИТ). В 2001 г. (9 лет) по экстренным показаниям с отеком гортани госпитализирована в ЛОР-отделение. В 2007 г. (25 лет) во время беременности получала экстренную медицинскую помощь в аллергологическом отделении по поводу отеков различных участков тела, где впервые и было заподозрено заболевание НАО. Периодически принимает дексаметазон в таблетках и инъекциях. От приема препарата Даназол отказывается. Объективно: беспокоят плотные отеки, в основном в области лица, проходящие постепенно, не сопровождающиеся кожным зудом. Проведено обследование: комплемент, эстеразный ингибитор С1 (количественный) – 0,0497 г/л (норма 0,21–0,43 г/л); комплемент, эстеразный ингибитор (функциональный) – 18% (норма 70–130%). Была рекомендована для постоянного приема транексамовая кислота от 1 до 4 г в сутки: ежедневный прием – 1 г в сутки, при нарастании отеков – до 4 г в сутки. Препарат относительно эффективен: на фоне его приема снижается частота рецидивов, но полностью исключить рецидивы отека не удается. Пациентка включена в регистр орфанных заболеваний для получения специфических препаратов для экстренной помощи при отеках жизнеугрожающей локализации.
Третий случай НАО, диагностированный в Республике Башкортостан: пациент Е., 1997 г.р. Впервые диагноз был поставлен в июне 2014 г. при обращении к врачу аллергологу-иммунологу, в возрасте 15 лет, как отек Квинке. Отеки впервые появились в апреле 2014 г. и наблюдались с частотой 2–3 эпизода в месяц. Провоцирующими факторами выступали: физическая нагрузка (начал заниматься в тренажерном зале), вирусные инфекции. Выраженный отек, потребовавший стационарного лечения, наблюдался в сентябре 2014 г. В лечении применялись высокие дозы системных глюкокортикостероидов, антигистаминные препараты, но достоверного эффекта от лечения не наблюдалось. В течение года подросток неоднократно обращался к аллергологу-иммунологу по месту жительства. При обследовании общеклинический анализ крови — без существенных изменений, эозинофилии не выявлено, общий IgE – в пределах нормы. Специфические IgE на пищевые аллергены: молоко 3+, яйцо 2+, свинина 2+, говядина 4+, баранина 4+, соя 4+, арахис 3+, мандарин 3+, греча 3+. Скарификационные пробы: полынь 2+, бытовые и эпидермальные пробы отрицательные.
Из анамнеза следует: рожден от первой беременности, протекавшей на фоне угрозы прерывания в первом триместре. Родился в срок 40–41 недель с массой 3965 г, с оценкой по шкале АПГАР 7–8 баллов. В возрасте 23 дней оперирован в РДКБ с диагнозом: Врожденный гипертрофический пилоростеноз. Протокол исследования фиброэзофагогастродуоденоскопии (после оперативного вмешательства): пищевод свободно проходим на всем протяжении, слизистая обычной окраски. Складки легко расправляются при инсуфляции. Кардия и ora serrata сформированы правильно. В желудке следы пищи. Слизистая обычной окраски. Привратник округлой формы, легко проходим, складки вокруг несколько утолщены. Слизистая двенадцатиперстной кишки без особенностей. Заключение: Состояние после пилоромиотомии.
На искусственном вскармливании с 3 месяцев. В анамнезе с 6 месяцев частые простудные заболевания. Проявления атопического дерматита до 12 месяцев. У ребенка отмечались высыпания на горчичники, антибиотики пенициллинового ряда. В возрасте 9–10 лет неоднократно госпитализировался с клиникой острого живота в хирургическое отделение. Уже в школьном возрасте (10 лет) вновь обратился к врачу аллергологу-иммунологу. Была выявлена бытовая и эпидермальная сенсибилизация. В возрасте 11 лет консультирован в ГБУЗ Республиканская детская клиническая больница Республики Башкортостан гастроэнтерологом и иммунологом, выставлен диагноз: хронический гастрит, вне обострения. Лямблиоз. Дискинезия желчевыводящих путей. По результатам иммунограммы выставлено заключение: латентно протекающий воспалительный процесс на фоне гипоиммуноглобулинемии A (Д80.2), умеренно высокий титр антител к хламидиям, положительный титр к микоплазме, что характеризовало наличие активной персистирующей внутриклеточной микстинфекции.
Наследственность: отец ребенка погиб, есть младший брат 5 лет с наследственной отягощенностью по материнской и по отцовской линии: атопический дерматит, холодовая аллергия, инсектная аллергия. Отец младшего ребенка в семье не живет.
На фоне лечения с назначением препаратов – сингуляр 10 мг, сорбенты, рузам 0,2 п/к по схеме – состояние ребенка стабилизировалось. После завершения курсового лечения вновь появились повторные эпизоды отека Квинке. С предполагаемым диагнозом НАО в декабре 2014 г. (17 лет) был направлен на обследование в РКБ. Врачом аллергологом-иммунологом и гастроэнтерологом выставлен диагноз: Хроническая идиопатическая крапивница на фоне соматического неблагополучия. Язвенная болезнь двенадцатиперстной кишки, хроническая форма с локализацией на передней и задней стенке в фазе рубца. Из протокола исследования фиброгастродуоденоскопии от 17.12.2014 г.: Пищевод и кардия без особенностей. В желудке жидкость, слизь. Стенки желудка эластичные, перистальтика активная. Слизистая желудка гиперемирована, гипертрофирована по типу «булыжной мостовой». Привратник округлой формы, проходим. Стенки луковицы ригидные, грубо деформированы. По передней и задней стенкам два ярко-красных звездчатых рубца с конвергенцией складок к центру и обрывом перистальтики в указанной зоне. Слизистая двенадцатиперстной кишки гиперемирована, отечная с белесоватыми эрозиями до 0,5 мм в диаметре. Заключение: Эрозивный бульбит. Гипертрофический гастрит «зернистая форма». Рубцовая деформация луковицы двенадцатиперстной кишки. Аллергологическая диагностика у аллерголога в РКБ: бытовые пробы – отрицательные, пыльцевые пробы отрицательные, шерсть овцы ++, перхоть лошади +, морская свинка ++.
Повторно госпитализирован в стационар 31.03 2015 г. в связи с появлением плотного отека в зоне подбородка, губ, носа, щек, отек языка, затрудняющего дыхание, ощущения сдавления в груди. Ухудшение связывает с вирусной инфекцией. В течение 10 дней до госпитализации отеки рецидивировали трехкратно. При объективном обследовании: состояние пациента средней степени тяжести, в сознании, адекватно реагирует на обстановку обследования. Нормостенического телосложения. Отек в нижней части лица, четко ограниченный по площади, очень плотный, кожа над ним бледная, при пальпации безболезненная. Зуда в области отека нет. Слизистая ротоглотки гиперемирована, миндалины не увеличены, язык отечный, увеличенный в размерах, с отпечатками зубов. В легких дыхание жесткое, свистящие хрипы. Тоны сердца ритмичные, звучные. Живот мягкий, доступен пальпации, безболезненный.
Результаты лабораторных и инструментальных исследований. Общеклинический анализ крови: гемоглобин – 152 г/л, эритроциты 4,7х10х12/л, лейкоциты 10,6х10х9/л, палочкоядерных 4%, сегментоядерных 82%, лимфоцитов 14%; общеклинический анализ мочи – без особенностей; биохимический анализ: общий белок 70 г/л, сахар 6,1 ммоль/л, мочевина 3,7 ммоль/л, билирубин 11,7 мкмоль/л, АЛАТ 14,0 ед/л, АСАТ 24,0 ед/л. В стационаре получал лечение: адреналин, дексаметазон, фуросемид, лоратадин в соответствующих возрастных дозах. После улучшения состояния, исчезновения отека подросток выписан из стационара.
С учетом незначительного эффекта от предложенной схемы лечения, частых рецидивов отеков Квинке в анамнезе во время консилиума в отделении было принято решение провести обследование на наследственный ангионевротический отек (НАО). Проведены лабораторные тесты: комплемент, эстеразный ингибитор С1 (количественный) – 0,329 г/л (норма 0,21–0,43 г/л); комплемент, эстеразный ингибитор С1 (функциональный) – 59% (норма 79–130).
Проведено исследование на наличие мутаций в гене SERPING1(C1NH), ответственном за наследственный ангионевротический отек типа I и II. Заключение специалиста: В результате исследования всех экзонов (1–8) и области экзон-интронных соединений гена SERPING1 патологических мутации не обнаружено. На основании полученного результата не было возможности ни подтвердить, ни опровергнуть диагноз «наследственный ангионевротический отек», поскольку описаны редкие протяженные делеции и мутации в регулярных областях гена SERPING1, которые не анализировались в данном исследовании. Кроме того, известны другие гены, ответственные за развитие наследственного ангионевротического отека типа III. Возможен поиск крупных делеций в гене SERPING1 (C1NH). Также были проведены исследования ДНК матери и брата пациента. Результат аналогичен результату пациента Е.
В связи с наличием характерных клинических проявлений, положительного анамнеза, снижением функциональной активности С1-ингибитора выставлен диагноз НАО II типа. Пациент внесен в региональный сегмент Федерального регистра орфанных заболеваний. Рекомендовано проведение терапии антикоагулянтами (транексамовая кислота), заполнен паспорт пациента.
11.09.2015 г. проведено плановое оперативное вмешательство по диагнозу: задне-нижняя нестабильность правого плечевого сустава, дисплазия гленоида. После выхода из наркоза у пациента появились отеки языка, нижней губы, в области правого локтевого сустава и правой кисти (оперированная конечность). Отеки сходили медленно в течение 4–5 дней на фоне гормональной терапии. В последующие 6 месяцев переболел ОРЗ, отеков не было. И соответственно клиническим проявлениям пациент нуждается в превентивном медикаментозном сопровождении (по алгоритму лечения НАО).
Выводы: таким образом, НАО – редкое, малознакомое медицинскому сообществу, но угрожающее жизни пациентов заболевание. Если в международной практике считается, что отсроченность диагностики заболевания составляет около 13 лет, то, к сожалению, в российском здравоохранении выявление подобных пациентов затягивается на десятилетия. В современных условиях у медиков появились инструменты специфической лабораторной диагностики и абсолютно надежные, высокотехнологичные, но дорогостоящие методы медикаментозного лечения, которые регламентированы постановлением правительства РФ для бесплатного обеспечения этой категории пациентов при угрожающем жизни заболевании.



