Рентгенография грудной клетки является первым методом лучевой диагностики заболеваний легких, плевры и средостения, который позволяет обнаружить патологический объект и на основании теневой картины с той или иной вероятностью определить его природу. Схожесть рентгенологической семиотики разных образований в средостении не всегда позволяет сделать однозначный вывод о конкретном заболевании, и тогда следующим диагностическим этапом становится компьютерная томография. Ее большим преимуществом является получение двухмерных аксиальных срезов на разных уровнях грудной полости с высоким пространственным разрешением без эффекта суммации теней, что делает метод основным в диагностике патологии средостения [1].
Кардиодиафрагмальное пространство на рентгенограммах занимает передненижние паракардиальные отделы грудной полости и отграничено медиально краем сердечной тени, латерально и снизу – контуром диафрагмы, спереди – грудной стенкой, сзади без видимой границы переходит в диафрагмомедиастинальный плевральный синус и нижние отделы центрального средостения. Поскольку границами и компонентами кардиодиафрагмального пространства являются разные анатомические структуры, то их патологические изменения часто приводят к затемнению этого участка на рентгенограммах. Тенеобразующий объект может исходить из органов или клетчатки средостения, плевры или плевральной полости, легкого, диафрагмы, поддиафрагмального пространства [2]. Такое многообразие разных источников затемнения, проецирующихся на одну и ту же анатомическую область, создает диагностические сложности в определении нозологических форм и требует проведения дополнительных исследований, одним из которых является УЗИ грудной клетки [3, 4].
Эхография позволяет получать двухмерные сканы как в аксиальной, так и в других плоскостях с формированием серошкального изображения, построенного на основании интенсивности отраженного эхосигнала. Пристеночное расположение объекта исследования без экранирования воздушной легочной тканью предоставляет хорошие условия для его ультразвуковой визуализации как из межреберий, так и субкостально, а высокая пространственная и контрастная разрешающая способность метода дает возможность детально оценить строение и взаимоотношение с окружающими структурами [5, 6].
Цель исследования: разработать методику УЗИ кардиодиафрагмального пространства и дифференциальную ультразвуковую диагностику его рентгенографических затемнений.
Материал и методы исследования
В отделении торакальной хирургии ГБУЗ «Городская клиническая больница № 5» г. Нижнего Новгорода обследованы 404 пациента с одно- или двусторонним затемнением кардиодиафрагмального пространства на обзорной рентгенограмме грудной клетки или плевральным выпотом, занимавшим передний реберно-диафрагмальный синус. У 237 пациентов тенеобразующий объект располагался внеплеврально: абдоминомедиастинальная липома (АМЛ) (166 пациентов), целомическая киста перикарда (ЦКП) (37 пациентов), выраженная паракардиальная жировая клетчатка (29 пациентов), грыжа щели Ларрея (5 пациентов). У 167 пациентов диагностирован свободный плевральный выпот различной этиологии с эхогенными структурами в переднем реберно-диафрагмальном синусе: жировые подвески (83 пациента), плевральные шварты и скопления рыхлого фибрина (56 пациентов), мезотелиома (21 пациент), метастазы (7 пациентов), которые не определялись рентгенологически на фоне выпота и были обнаружены только эхографически. Очаги верифицированы: у 261 пациента комплексным клинико-инструментальным обследованием, у 117 – оперативно, у 46 – видеоторакоскопией с биопсией.
Все пациентам выполнено УЗИ грудной клетки на сканерах среднего класса секторным (3,5 МГц), конвексным (2–6 МГц) и линейным (7–12 МГц) датчиками на абдоминальной программе сканирования. Исследование плевральной полости проводили по принятой методике [7, 8], а кардиодиафрагмального пространства – по разработанной оригинальной методике, состоявшей из двух последовательных этапов. Сначала выполняли субкостальное сканирование из-под мечевидного отростка с направлением оси сканирования к правому плечу или справа парастернально из межреберья над местом прикрепления реберной дуги к грудине и выявляли дополнительное образование между куполом диафрагмы и сердцем. Измеряли его наибольшую ширину от диафрагмы до контура сердца и толщину от грудной стенки до наиболее удаленной вглубь средостения границы.
На втором этапе определяли степень распространения патологического объекта вниз, оценивая глубину проникновения в передний реберно-диафрагмальный синус и далее за его пределы или взаимосвязь с передней брюшной стенкой и органами брюшной полости через грудино-реберный треугольник диафрагмы (щель Ларрея–Морганьи). Для этого датчик при продольном сканировании из межреберья или субкостально направляли каудально, плавно смещая его далее вниз вдоль передней брюшной стенки, тем самым у АМЛ подтверждали сообщение жировой ткани в средостении с предбрюшинной клетчаткой, а у мезотелиом – прорастание опухоли в синус и ниже в мягкие ткани передней брюшной стенки [9]. В диагностике затемнений кардиодиафрагмального пространства УЗИ грудной клетки показало более высокую чувствительность, чем рентгенография: соответственно 92,5% и 74,1% при АМЛ и 90,8% и 70,8% при ЦКП.
Результаты исследования и их обсуждение
Причиной затемнения кардиодиафрагмального пространства служили различные патологические процессы, которые исходили из плевры и сопровождались накоплением выпота или возникали из окружающих органов и тканей, располагаясь внеплеврально. В зависимости от консистенции внеплевральные объекты были солидными или жидкостными, что определяло их эхогенность и эхоструктуру. Наиболее часто встречалась АМЛ – ложная грыжа из предбрюшинной клетчатки, проникшая через щель Ларрея–Морганьи в правое кардиодиафрагмальное пространство. В норме его частично заполняло немного жировой клетчатки треугольной формы до 2,0 см в ширину и в глубину средостения. Подозрение на АМЛ возникало при выявлении избыточного количества жировой ткани свыше 3,0 см в этих измерениях. Большинство пациенток были женщины с повышенной массой тела (97,0%).
АМЛ при субкостальном сканировании имела вид образования треугольной формы без капсулы, основанием к грудной стенке и вершиной вглубь средостения, с неоднородной эхоструктурой за счет множественных коротких гиперэхогенных сигналов на гипоэхогенном фоне, такой же, как у нормальной паракардиальной и предбрюшинной жировой клетчатки. Эти сигналы возникали при отражении ультразвука от соединительнотканных прослоек, разделявших жировую ткань на отдельные дольки. На глубоком вдохе образование незначительно меняло треугольную форму за счет смещения диафрагмы. Важным диагностическим признаком АМЛ являлась визуализация ее ножки при продольном сканировании в виде узкого гипоэхогенного участка на уровне диафрагмы, переходившего каудально в предбрюшинную клетчатку (рис. 1). Частота обнаружения зависела от толщины ножки, которая составила в среднем 8,0±1,3 мм и была видна у 102 (61,4%) больных.
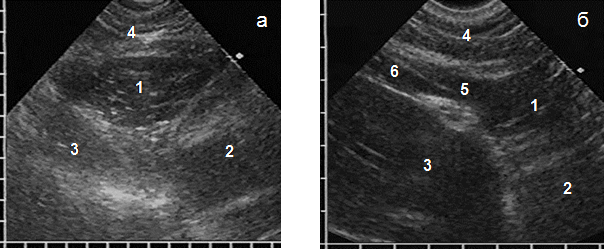
Рис. 1. Эхограммы АМЛ при субкостальном сканировании (а) и ее ножки при продольном сканировании (б): АМЛ (1), сердце (2, размыто при сокращении), печень (3), передняя брюшная стенка (4), ножка липомы (5), предбрюшинная клетчатка (6)
У пациентов со значительно повышенной массой тела абдоминомедиастинальную липому имитировала избыточная паракардиальная клетчатка средостения, имевшая типичную для жировой ткани эхоструктуру. Она лоцировалась не только в правом кардиодиафрагмальном пространстве, но по обе стороны сердца – вокруг верхушки и вдоль апикальных, а при значительном количестве – вдоль средних и базальных отделов стенок желудочков в виде треугольного или грушевидного образования, изменявшего свою форму синхронно с сокращениями сердца. Почти все пациенты были мужчины-гиперстеники (82,8%) с широкой грудной клеткой. Размеры паракардиальной клетчатки сильно варьировали, особенно слева, колеблясь от 3,0х2,5 см до 8,0х5,5 см. Принципиальным отличием от АМЛ являлось отсутствие связи с предбрюшинной клетчаткой, от которой она четко отграничивалась куполом диафрагмы, не распространяясь ниже его уровня. При большой толщине жирового слоя его латеральный контур вдоль левого желудочка частично перекрывался реверберациями от предлежащей воздушной легочной ткани.
ЦКП располагались как в кардиодиафрагмальном пространстве, так и на различном протяжении вдоль правого, реже левого желудочка, при крупном размере достигая предсердий. Рентгенографически нередко возникали затруднения в их дифференцировке с АМЛ, что стало стимулом для разработки дифференциальной ультразвуковой диагностики. Для ЦКП характерна овальная или каплевидная форма, при которой продольная ось располагалась параллельно длинной оси сердца, но кисты в правом кардиодиафрагмальном пространстве часто имели треугольную форму со сглаженными углами. Они содержали прозрачную жидкость, поэтому имели однородную анэхогенную структуру, что принципиально отличало их от гипоэхогенных липом с линейными эхосигналами. Важным эхопризнаком ЦКП являлась тонкая эхогенная стенка, а связь с предбрюшинной клетчаткой отсутствовала (рис. 2). Сообщение с полостью перикарда установлено у 2 (5%) больных. Размеры кист колебались в более широких пределах, чем АМЛ: от 4 до 17 см. Допплерографически в них наблюдалась передаточная пульсация за счет сокращений сердца.
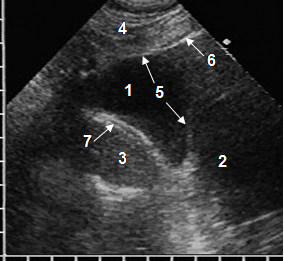
Рис. 2. Эхограмма ЦКП при субкостальном сканировании: анэхогенная ЦКП (1), сердце (2), печень (3), передняя брюшная стенка (4), стенка кисты (5), гиперэхогенная поверхность легкого с реверберациями (6), трехслойная структура мышечной части диафрагмы (7)
УЗИ при грыже щели Ларрея имело разную информативность в зависимости от содержимого грыжевого мешка. Диагностические сложности возникли при наличии в нем участков большого сальника, эхографически не отличавшихся от предбрюшинной клетчатки и ошибочно расцененных как АМЛ у 3 больных. Для дифференцировки необходимо прицельно оценивать ту структуру, в которую жировая ткань переходила ниже диафрагмы – в предбрюшинную клетчатку, расположенную поверхностно вдоль непрерывной гиперэхогенной линии брюшины, или в большой сальник глубже нее, когда в брюшине возникал участок перерыва в области грыжевых ворот. Ущемленная петля тонкой кишки определялась в грыжевом мешке в виде изогнутой трубчатой структуры с эхогенной стенкой и жидким содержимым с неоднородной малоподвижной взвесью, при этом в брюшной полости наблюдалась типичная эхокартина острой тонкокишечной непроходимости.
Эхографически выявление жидкости в полости плевры не вызывало диагностических затруднений. Выпот в переднем реберно-диафрагмальном плевральном синусе лоцировался как анэхогенное пространство с сохранением его анатомической формы в виде треугольника с остроконечной вершиной, направленной вниз. Диагностические вопросы возникали при выявлении на фоне выпота диффузного утолщения плевры или очаговых образований, требовавших определения их воспалительной или опухолевой природы. Для этого оценивали распространенность объекта в плевральной полости и за ее пределами, его размеры, форму, эхоструктуру и передаточную смещаемость, изменение анатомической формы синуса при заполнении его эхогенными массами, на основании чего дифференцировали мезотелиомы от скоплений фибрина и крупных плевральных шварт, а метастазы от жировых подвесок.
Диффузно-узловая мезотелиома распространялась, как правило, на два листка плевры, чаще диафрагмальный и костальный, в виде однородного гипоэхогенного пласта с четкими неровными контурами и неравномерной толщиной более 10 мм и протяженностью свыше 10 см. Максимальная толщина чаще составляла 15–30 мм (65%). Опухоли до 15 мм встречались редко (10%), но у 25% больных толщина превышала 30 мм, причем в 14% мезотелиома занимала значительный объем плевральной полости, достигая в наибольшем месте 60–80 мм. У 12 (39%) пациентов опухоль распространялась на весь передний реберно-диафрагмальный синус, расширяя его и прорастая вниз в переднюю брюшную стенку в виде образования удлиненной формы с закругленным дистальным краем (рис. 3). Крупные мезотелиомы сильно деформировали диафрагму, в месте прорастания купол локально истончался и замещался опухолевой тканью. Дыхательная подвижность диафрагмы отсутствовала при опухоли более 20 мм и переходе через передний плевральный синус на костальную плевру.
Фибриновым плевральным наложениям свойственна меньшая толщина – 6–8 мм, но мы наблюдали и массивные шварты неравномерной толщины до 25 мм, имитировавшие мезотелиому. В отличие от опухоли они имели неровную зазубренную поверхность и часто сочетались с множественными эхогенными нитями в виде разноячеистой фибриновой сети. Заполненный фибриновыми массами передний плевральный синус сохранял нормальные размеры и остроугольную форму. При рыхлой консистенции фибрина прослеживалось изменение его формы на глубоком вдохе синхронно с дыхательным смещением диафрагмы.

Рис. 3. Эхограммы мезотелиомы с ростом по плевре (а) и в переднем плевральном синусе (б): опухолевое утолщение диафрагмальной (1) и костальной (2) плевры, прорастание опухоли в синус (3), печень (4), мягкие ткани передней брюшной стенки (5), плевральный выпот (6)
Часто в переднем плевральном синусе на фоне выпота различной этиологии лоцировались жировые подвески, представленные нормальной жировой тканью, расположенной интраплеврально в виде отдельных элементов или массивных скоплений. Они имели вытянутую овальную или грушевидную форму с узким основанием в глубине синуса и краниальным расширением за его пределами и характерную для жировой ткани среднеэхогенную дольчатую структуру с множественными линейными гиперэхогенными включениями. Вследствие мягкой консистенции жировые подвески обладали выраженной передаточной смещаемостью при дыхании, что выражалось в их плавных качательных движениях синхронно с дыхательными смещениями диафрагмы.
В отличие от жировых подвесок метастазы, расположенные только в переднем плевральном синусе, не встречались, они выявлялись на разных листках плевры, в том числе и в синусе. Для них характерны овальная или уплощенная форма с широким основанием, однородная гипоэхогенная структура, отсутствие передаточной смещаемости при дыхании или сердцебиении. При диффузном росте их эхосемиотика не отличалась от мезотелиомы.
Выводы. УЗИ грудной клетки является эффективным методом диагностики патологии кардиодиафрагмального пространства. В дифференцировке затемнений данной локализации ультразвуковой метод более информативен, чем рентгенография, благодаря возможности оценки эхоструктуры тенеобразующего объекта и распространения за пределы грудной клетки, что позволяет своевременно выбрать правильную тактику лечения. АМЛ имела треугольную форму, неоднородную гипоэхогенную структуру с короткими линейными сигналами, ножку к предбрюшинной клетчатке; ЦКП – овальную форму, однородное анэхогенное содержимое, тонкую эхогенную капсулу без связи с передней брюшной стенкой. Для мезотелиомы характерно неравномерное утолщение плевры свыше 20–30 мм с четким контуром и однородной гипоэхогенной структурой, у трети больных опухоль заполняла весь передний плевральный синус и прорастала вниз за его пределы. Жировые подвески лоцировались как исходящие из глубины синуса вытянутые образования с узким основанием, с неоднородной дольчатой эхоструктурой и передаточной смещаемостью при дыхании, а метастазы – как однородные гипоэхогенные очаги овальной формы, плотно фиксированные к плевре и без передаточной смещаемости.



