В начале XXI века меланома остается потенциально смертельным злокачественным новообразованием. Заболеваемость злокачественной меланомой растет во всем мире, что приводит к важной социально-экономической проблеме. В настоящее время меланома рассматривается как многофакторное заболевание, возникающее в результате взаимодействия между генетической восприимчивостью и воздействием окружающей среды [1].
Выживаемость при меланоме, как и любом типе рака, снижается с прогрессированием и метастазированием опухоли. Метастазирование и прогрессирование меланомы кожи являются результатом сложных комплексных процессов, происходящих на уровне всего организма [2]. Основной причиной смерти больных меланомой является широкое распространение метастазов. Меланома кожи имеет склонность к метастазированию на ранних этапах заболевания и способна метастазировать как в регионарные, так и в отдаленные участки. Наиболее распространенными местами регионарного метастазирования являются близлежащая кожа, подкожная клетчатка и лимфатические узлы, а отдаленных метастазов – легкие, печень, головной мозг, кости и кишечник [3].
В последние годы многочисленные исследования доказали важную роль микроокружения в органах-мишенях для развития метастазов злокачественных новообразований. Микроокружение опухоли состоит из опухолевых, стромальных и иммунных клеток, а также внеклеточной среды [4]. Теория «seed and soil» рассматривает формирование преметастатических ниш – мест формирования будущих метастазов – в качестве определяющего фактора метастазирования опухоли. Ключевую роль в образовании преметастатических ниш играют вещества, выделяемые первичной опухолью, и мобилизуемые ими клетки иммунной системы [5]. Одной из основных характеристик преметастатических ниш является формирование новой сосудистой сети в преметастатических сайтах. Процесс неоангиогенеза необходим для роста и метастазирования большинства солидных опухолей, включая меланому. Без активно протекающего неоангиогенеза размер опухоли редко превышает 2–3 мм. Ангиогенез опухоли главным образом зависит от синтеза неопластическими клетками специфических для клеток эндотелия факторов роста, способных стимулировать неоангиогенез [6].
К основным регуляторам неоангиогенеза относят фактор роста эндотелия сосудов (VEGF) и маркер сосудистого эндотелия CD31. CD31 – наиболее известный иммуногистохимический маркер среди солидных опухолей [7]. Семейство VEGF состоит по меньшей мере из пяти генов (VEGF-A, VEGF-B, VEGF-C, VEGF-D, VEGF-E) и плацентарного фактора роста, из которых наиболее мощными активаторами ангиогенеза являются VEGF-A и VEGF-B. По литературным данным, клетки меланомы продуцируют и секретируют VEGFA. Инокуляция клеток меланомы человека, трансфецированных VEGFA, в иммунодефицитные модели мышей приводит к активации васкуляризации и повышению проницаемости микрососудов [8].
Тем не менее роль VEGFA и CD31 в преметастатической реорганизации органов, специфичных для метастазирования при меланоме, окончательно не установлена. Изучение ангиогенеза при злокачественных опухолях является важным и перспективным направлением для исследования прогрессирования опухоли и разработки антиангиогенной терапии.
Цель исследования: изучение уровней экспрессии фактора роста эндотелия сосудов VEGFA и маркера сосудистого эндотелия CD31 в органах-мишенях метастазирования меланомы в преметастатическую стадию для улучшения понимания их роли в процессе неоангиогенеза.
Материал и методы исследования
Объектом нашего исследования послужили биоптаты органов половозрелых самок мышей линии C57Bl6 (легкие, печень). Мыши предоставлены виварием ФГБНУ «Федеральный исследовательский центр Институт цитологии и генетики Сибирского отделения Российской академии наук». С перевитой меланомой В16 (культура клеток была получена в ФГБНУ «НИИ фундаментальной и клинической иммунологии») в преметастатическую стадию (14-е сутки) количество мышей составляло 13, в контрольной группе животных также было 13. Проведенное исследование утверждено на заседании биоэтической комиссии по работе с животными (от 19 апреля 2016 года № 3) и локального этического комитета КрасГМУ (от 6 июня 2016 года № 70/2016).
Перевиваемая меланома B16 является общепризнанной и доступной экспериментальной моделью меланомы, которая характеризуется быстрым развитием, экспоненциальным ростом, классическим метастазированием, что позволяет исследовать особенности развития и метастазирования, а также тестировать новые возможности лечения меланомы кожи.
Органы, фиксированные в 10%-ном нейтральном забуференном формалине, заключали в парафин и изготавливали гистологические срезы толщиной до 4 мкм на микротоме МС-2 («Точмедприбор», Харьков, Украина) на базе кафедры патологической анатомии им проф. П.Г. Подзолкова с курсом ПО. В дальнейшем срезы подвергались иммуногистохимическому окрашиванию по стандартной методике с использованием системы детекции REVEAL – Biotin-Free Polyvalent (Spring BioScience, Плезантон, США). Сначала проводили депарафинизацию изготовленных срезов в ксилоле в термостате при температуре +550С в течение 30 минут, затем осуществляли дегидратацию в смене растворов спиртов понижающей концентрации: 96%-ный этанол – 96%-ный этанол – 70%-ный этанол по 5 минут, а затем дважды промывали в дистиллированной воде по 5 минут. Блокировку эндогенной пероксидазы осуществляли при помощи 0,3%-ного раствора перекиси водорода Hydrogen Peroxide Block в течение 10 минут, затем промывали в дистиллированной воде. Демаскировку антигена проводили в печи в течение 10 минут при температуре +900С в цитратном буфере с pH 6,0 для первичных антител CD31 и в растворе 1мМ EDTA c pH 8,0 для VEGFA. Затем срезы оставляли на 20 минут при комнатной температуре и дважды по 5 минут промывали в фосфатно-солевом буфере с pH 7,4 («Биолот», Россия). Далее проводили инкубацию срезов с нормальной неиммунной сывороткой Protein Block в течение 20 минут, затем, не смывая со срезов протеинового блока, осуществляли инкубацию с первичными специфическими моноклональными антителами к CD-31 (клон SP38, кат. № MA5-16337, ThermoFisher, Рокфорд, США) в разведении 1:50 и к VEGFA (клон VG1, кат. № MA1-16629, ThermoFisher, Рокфорд, США) в разведении 1:300 для ткани легких и 1:500 для ткани печени в течение 60 минут во влажной камере при комнатной температуре. После инкубации стекла промывали в фосфатно-солевом буфере, далее наносили вторичные антитела – Complement и инкубировали в течение 10 минут при комнатной температуре, после чего стекла вновь промывали в фосфатно-солевом буфере. Далее проводили инкубацию HRP Conjugate во влажной камере при комнатной температуре в течение 30 минут, после чего стекла также промывали в фосфатно-солевом буфере. Для визуализации продукта реакции использовали AEC Single Solution, раствор наносили на стекла на 15 минут, после чего стекла также дважды промывали в дистиллированной воде по 5 минут. На следующем этапе применяли фоновый краситель – Hematoxylin Mayers (Dako, Дания), который наносили на срезы на 1 минуту, после чего снова промывали дистиллированной водой до чистых вод. В качестве монтажного средства для фиксации покровных стекол использовали монтирующую жидкость Mount quick aqueous (Bio-optica, Италия).
Результаты реакций с антителами к VEGFA, локализованному внутриклеточно, оценивали по интенсивности окрашивания с использованием Histochemical score (E=p(i)xi, где i – интенсивность окраски в баллах от 0 до 3, p(i) – процент окрашенных клеток с различной интенсивностью при увеличении х400 в 10 случайных полях зрения.
Относительный уровень экспрессии CD-31 определяли в 10 случайных полях зрения при увеличении х200 путем подсчета кровеносных сосудов с положительной окраской эндотелия.
Подсчет положительно окрашенных клеток и сосудов проводили с использованием микроскопа Olympus BX-41 (Olympus, Токио, Япония) с видеонасадкой Olympus u-CMAD3 и программного обеспечения Infinity Capture3 (Lumenera, Оттава, Канада).
Полученные результаты сравнивали между собой с использованием непараметрического статистического U-критерия Манна–Уитни для двух независимых выборок. Различия между сравниваемыми показателями считали достоверными при p<0,05.
Результаты исследования и их обсуждение
Неоангиогенез – процесс, представляющий собой образование новых кровеносных сосудов из уже существующих, таких как капилляры и посткапиллярные венулы, он играет ключевую роль во время эмбрионального развития, а также во взрослой жизни, в ряде физиологических и патологических состояний, таких как канцерогенез и хроническое воспаление, где сам ангиогенез может способствовать прогрессированию заболевания. Контроль ангиогенеза осуществляется балансом между проангиогенными и антиангиогенными молекулами, которые обладают положительной и отрицательной регуляторной активностью, с формированием так называемого ангиогенного переключателя [8]. Неоангиогенез является одним из наиболее интенсивно изучаемых направлений онкологических исследований последних лет. Исследования, проводимые на животных моделях меланомы и рака молочной железы, выявили реорганизацию сосудистой системы в региональных лимфатических узлах до вторжения метастатических клеток [9].
CD31 относится к суперсемейству иммуноглобулинов PECAM-1, которые экспрессируются на поверхности клеток эндотелия. В состав молекулы СD31 входит шесть иммуноглобулиноподобных доменов. СD31 играет одну из главных ролей в ангиогенезе, принимает участие в регуляции регенерации ткани, клеточной миграции, выживаемости клеток [10]. Показано, что низкие уровни экспрессии CD31 коррелируют с лучшей выживаемостью у пациентов с в-клеточным хроническим лимфолейкозом [11]. Также ранее было установлено, что анти-СD31 антитела способны ингибировать процесс неоангиогенеза в злокачественных опухолях мышей in vivo. Кроме того, показано, что у нокаутных животных по гену СD31 неоангиогенез злокачественного новообразования был заблокирован [12].
При оценке экспрессии маркера сосудистого эндотелия СD31 в ткани легких и печени мышей C57Bl6 контрольной и экспериментальной групп получены следующие результаты: в ткани легких значимых различий экспрессии CD31 между контрольной и экспериментальной групп не выявлено (р-0,08), обнаружено достоверное увеличение уровня экспрессии маркера сосудистого эндотелия в ткани печени в преметастатическую стадию по сравнению с группой контроля (р-0,02) (рис. 1).
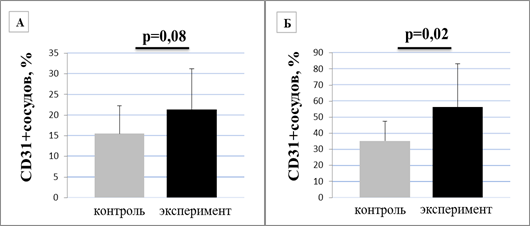
Рис. 1. Уровни экспрессии CD31 в исследуемых группах:
А – в нормальной ткани легких и в преметастическую стадию при меланоме;
Б – в нормальной ткани печени и в преметастическую стадию при меланоме
Нами было обнаружено, что в печени уровень экспрессии СD31 в преметастатическую стадию достоверно выше по сравнению с группой контроля. Исходя из полученных данных можно предположить, что полученный нами результат свидетельствует о важной роли данной молекулы в процессах, играющих важную роль в подготовке ткани органа-мишени метастазирования к данному процессу.
Известно, что CD31 отвечает за формирование сосудистоподобных образований на самых ранних этапах ангиогенеза. Интересно отметить, что использование ингибиторов VEGF приводило к повышению популяции CD31+ клеток меланомы и активации VEGF-независимого ангиогенеза [13].
Фактор роста сосудистого эндотелия VEGFA – один из ключевых факторов регуляции неоангиогенеза, который секретируется клетками эндотелия, макрофагами, фибробластами, гладкомышечными клетками и тромбоцитами [8]. Кроме того, VEGFA активно участвует в стимуляции пролиферации и миграции клеток сосудистого эндотелия, способствует дедиффиренцировке и выживаемости опухолевых клеток, принимает участие в контроле процессов вазодилатации. При иммуногистохимических исследованиях было обнаружено, что семейство VEGF экспрессируется примерно в половине исследованных случаев солидных опухолей человека. Доказано, что ингибирование VEGF приводит к замедлению роста и метастазирования меланомы [7]. Экспрессия гена VEGF регулируется различными механизмами, наиболее важным из которых является гипоксия, особенно через регуляцию HIF-1α [14].
В проведенном исследовании не выявлено изменений в уровнях экспрессии VEGFА в ткани легких контрольной и экспериментальной групп (р-0,13), однако уровень экспрессии VEGFA статистически значимо повышался в преметастатическую стадию в ткани печени по сравнению с группой контроля (p-0,0001) (рис. 2).
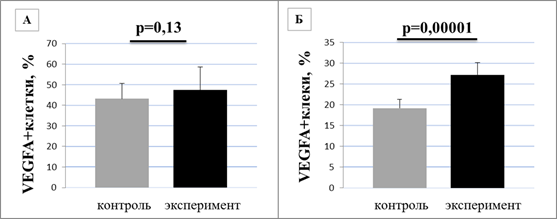
Рис. 2. Уровни экспрессии VEGFA в исследуемых группах:
А – в нормальной ткани легких и в преметастическую стадию при меланоме;
Б – в нормальной ткани печени и в преметастическую стадию при меланоме
Можно предположить, что повышение уровня VEGFА в преметастатическую стадию в ткани печени обусловлено стимуляцией его локального синтеза, который может быть связан с гипоксией, способствующей повышению экспрессии транскрипционного фактора HIF-1α, и процессом воспаления, развивающегося в органах-мишенях.
Однако клетками первичной опухоли вырабатываются экстравезикулы, подразделяющиеся на опухольпроизводные экзосомы, микровезикулы и большие онкосомы. Показано, что наряду с другими компонентами экзосомы содержат микроРНК [5]. Можно предположить, что ряд содержащихся в экзосомах miRs способствует повышению экспрессии VEGFА в преметастатическую фазу меланомы в клетках печени.
Повышение уровня VEGFА приводит к мобилизации и рекрутингу миелоидных клеток из костного мозга в места формирования преметастатических ниш. В дальнейшем эти клетки принимают участие в процессе ремоделирования локального микроокружения, вырабатывая и выделяя провоспалительные цитокины, факторы роста и ангиогенные молекулы, способствуя тем самым колонизации органов-мишеней, пролиферации в них опухолевых клеток и в конечном счете формированию метастазов [15].
Заключение
Метастазирование – очень сложный процесс. Существует множество различных гипотез и теорий, касающихся участия опухолевого микроокружения в развитии и прогрессии опухоли. Большая проблема заключается в том, чтобы научиться использовать эту информацию в терапевтических целях, например для прерывания или блокирования каскада событий, и таким способом – предотвращения метастатического поражения органов.
Таким образом, в результате проведенного исследования установленное нами повышение уровней экспрессии маркера сосудистого эндотелия СD31 и фактора роста эндотелия сосудов VEGFA в ткани печени в преметастатическую стадию обусловлено участием данных факторов в неоангиогенезе и формировании так называемых преметастатических ниш – важного подготовительного этапа метастазирования меланомы.



