Расщепление кистей и стоп (cleft hand and foot or split-hand/split-foot malformation (SHFM)) – это продольное недоразвитие кистей и стоп, начиная от незначительного укорочения третьего луча до полного отсутствия 1–4 пальцев. Частота встречаемости SHFM варьирует, по данным литературы, от 1/18 000 до 1/90 000 новорожденных, что составляет 8–17% от всей патологии конечностей [1, 2]. Наследование в основном аутосомно-доминантное с внутрисемейной клинической вариабельностью, но могут быть и спорадические случаи [3, 4]. На сегодняшний день описано семь хромосомных локусов, ассоциированных с изолированной SHFM, т.е. SHFM1-6 и SHFM, сочетающаяся с гипо-/аплазией длинных трубчатых костей голени (таблица) [5].
Клинические и молекулярные характеристики различных локусов SHFM
|
SHFM локус |
Тип мутации |
Тип наследования |
|
SHFM 1-го типа |
Перестройки в локусе 7q21.3-q22.1 либо мутация DLX5 |
Аутосомно-доминантный либо аутосомно-рецессивный |
|
SHFM 2-го типа |
Xq26Дупликация |
X-сцепленный рецессивный |
|
SHFM 3-го типа |
Делеция 10q24 |
Аутосомно-доминантный |
|
SHFM 4-го типа |
Мутация TP63 |
Аутосомно-доминантный |
|
SHFM 5-го типа |
Делеция в локусе 2q31 |
Аутосомно-доминантный |
|
SHFM 6-го типа |
Мутация WNT10B |
Аутосомно-рецессивный |
|
SHFM, сочетающаяся с недоразвитием длинных трубчатых костей голени |
Дупликация в локусе 17p13.3 |
Аутосомно-доминантный |
Расщепление кистей и стоп может быть как отдельным симптомом, так и входить в структуру различных генетических синдромов (EEC, LADD, ADULT, CHARGE, VACTERL, Smith–Lemli–Opitz [5, 6].
SHFM – это клинически неоднородное заболевание, проявление которого варьирует от относительно легкого дефекта, такого как гипоплазия одной фаланги или синдактилия, до аплазии одного или нескольких центральных пальцев, т.е. классического расщепления, известного как lobster-claw anomaly (рис. 1) [4, 5].
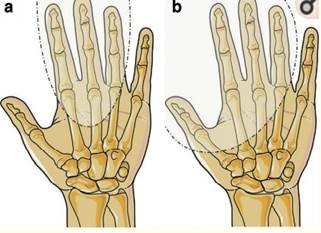
Рис. 1. Схематическое представление различных типов SHFM: а) классическое расщепление с аплазией центральных лучей; b) аплазия фаланг 1–4 пальцев [5]
На сегодняшний день известно значительное количество вариантов клинических классификаций SHFM в зависимости от тяжести недоразвития на кисти [7, 8].
Клинически расщепление разделяют на типичное, когда имеется расщепление кистей и стоп, а также атипичное, когда расщепление представлено только на кисти [9, 10]. Предложенные классификации основаны на сохранности лучей и видах деформации кисти.
Хирургическому лечению расщепления кисти посвящено значительное количество работ [4, 7, 8]. Однако в основном они описывают различные виды реконструкций у пациентов с расщеплением кисти при сохранности 1-го, 5-го лучей. Хирургическому лечению пациентов с крайними формами расщепления кистей и стоп посвящено незначительное количество работ. Основная цель хирургического лечения – восстановление максимально эффективного схвата между двумя пограничными пальцами, что возможно за счет микрохирургической аутотрансплантации пальца со стопы на кисть [7, 8, 11]. Для получения хорошего функционального и косметического результата оперативное лечение необходимо начинать в раннем возрасте.
Проведенный литературный поиск показал, что остаются неизученными многие проблемы микрохирургической аутотрансплантации пальца стопы на кисть у пациентов с SHFM, что и потребовало проведения данного исследования.
Цель исследования: провести ретроспективный анализ лечения пациентов детского возраста с SHFM, которым выполняли микрохирургическую аутотрансплантацию 5-го пальца стопы в позицию 1-го пальца кисти.
Материалы и методы исследования. В исследование были включены 17 пациентов (12 девочек (70,6%) и 5 мальчиков (29,4%)) с SHFM, которым была выполнена свободная пересадка 5-го пальца стопы в позицию 1-го пальца кисти в период с 1984 по 2019 гг. в отделении реконструктивной микрохирургии и хирургии кисти ФГБУ «НМИЦ детской травматологии и ортопедии им. Г.И. Турнера» Минздрава России. 9 пациентам данная операция была выполнена дважды. Критерий исключения – пациенты, которым выполняли микрохирургическую аутотрансплантацию других пальцев стоп в позицию 1-го пальца кисти.
Микрохирургическая аутотрансплантация 5-го пальца стопы включала несколько этапов. Этапы в реципиентной области включали выделение: а) сухожилий сгибателей/разгибателей; б) 1-й пястной кости, при необходимости ее отведение в положение оппозиции к остальным пальцам кисти либо создание 1-й пястной кости за счет транспозиции 4-й пястной кости; в) пальцевых нервов, артерии и вены в проксимальном отделе кисти. Этапы в донорской области включали: а) выделение вен, артерий и нервов, кровоснабжающих и иннервирующих 5-й палец; б) отсечение как можно более проксимально сухожилий сгибателей и разгибателей пальцев; в) отделение трансплантата от плюсневой кости путем капсулотомии плюснефалангового сустава или остеотомии 5-й плюсневой кости.
Выделение питающей ножки трансплантата 5-го пальца расщепленной стопы имело ряд особенностей, связанных со значительными отличиями от нормальной анатомии стопы. Поэтому предоперационное обследование детей с данной патологией, такое как допплерография или селективная ангиография, имело большое значение и целесообразность. Идентификацию тыльной артерии стопы начинали в проксимальном отделе стопы. На уровне проксимальных метаэпифизов плюсневых костей магистральная артерия начинала делиться на несколько ветвей. Здесь важно было проследить ход каждой из них, убедиться в их участии в кровоснабжении 5-го пальца и, соответственно, определиться: какие ветви сохранять, а какие коагулировать. При этом артериальные ветви вопреки законам нормальной анатомии часто занимали нестандартные положения, «ныряли глубоко в ткани под сухожилия и связки». Риск их повреждения чрезвычайно высок. Выделение нервов также вызывало трудности, поскольку из-за их нестандартного расположения сохранялся высокий риск их случайного повреждения.
Полученный трансплантат со стопы переносили в реципиентную область и помещали в позицию 1-го пальца, фиксацию производили спицами Киршнера в положения отведения и противопоставления к имеющимся «локтевым» пальцам кисти. Сшивали сухожилия сгибателей и разгибателей, пальцевые нервы. Накладывали анастомозы между сосудами трансплантата и кисти. После снятия клипс и контроля восстановления кровообращения (оценкой цвета, температуры и капиллярной реакции) в трансплантате послойно накладывали швы на подкожно-жировую клетчатку и кожу. При необходимости выполняли замещение раневых кожных дефектов толстыми расщепленными кожными трансплантатами. После операции обе конечности фиксировали гипсовыми шинами на срок 5–6 недель – до удаления металлических фиксаторов.
В течение первых 3–4 суток пациент находился под регулярным контролем в условиях ОАРИТ, проводилась антикоагулянтная и способствующая улучшению микроциркуляции инфузионная терапия.
Были проанализированы протоколы оперативных вмешательств и следующие данные: 1) возраст и пол пациента; 2) варианты донорских и реципиентных сосудов; 3) виды реконструкций на кисти; 4) осложнения. Все осложнения были классифицированы как интраоперационные и послеоперационные [12]. При оценке послеоперационных осложнений учитывалась классификация Caton [13]. Кроме того, проведен анализ количества последующих оперативных вмешательств.
Полученные результаты подвергали статистической обработке в системе Statistica 7.0 for Windows с помощью методов параметрической и непараметрической статистики.
Результаты исследования и их обсуждение. В период с 1984 по 2019 гг. в отделении реконструктивной микрохирургии и хирургии кисти ФГБУ «НМИЦ детской травматологии и ортопедии им. Г.И. Турнера» Минздрава России было произведено 26 микрохирургических аутотрансплантаций 5-го пальца стопы в позицию 1-го пальца кисти у пациентов с расщеплением кистей и стоп. Средний возраст пациентов составил 4,1±2,5 года.
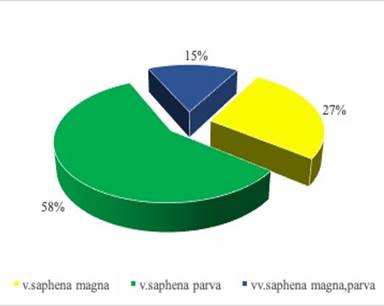
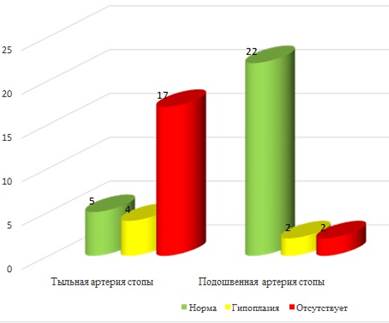
Заимствование трансплантата на стопе чаще всего производили на малой (58% пациентов) и большой (27%) подкожных венах. Отмечена особенность ангиоархитектоники 5-го пальца стопы – в 65,4% случаев тыльная артерия стопы отсутствовала, кровоснабжение осуществлялось только из подошвенных артерий (рис. 2). При этом у 46,1% пациентов подошвенная артерия стопы была представлена только одной веткой.
А
Б
Рис. 2. Диаграмма распределения выделенных вен (А) и артерий (Б) в донорской области
Литературный поиск не выявил данных об ангиоархитектонике донорской области у пациентов с SHFM при микрохирургической аутотрансплантации пальцев стопы на кисть. Однако отмечено, что в 32% случаев при выделении 2-го пальца стопы у детей тыльная артерия стопы отсутствует [14].
В 50% случаев заимствование трансплантата выполняли на уровне плюснефалангового сустава, в 26,9% – по зоне роста и в 23,1% – в средней трети диафиза 5-й плюсневой кости. Во всех случаях раневой дефект на стопе был закрыт местными тканями. Дополнительной реконструкции не требовалось.
При подготовке реципиентной области на кисти выполнялись различные виды реконструкций 1-й пястной кости (рис. 3). В основном производили транспозицию 2-й пястной кости (42% случаев) или отведение «лучевой» пястной кости (II–III) в положение оппозиции посредством капсулотомии запястно-пястного сустава (23%).
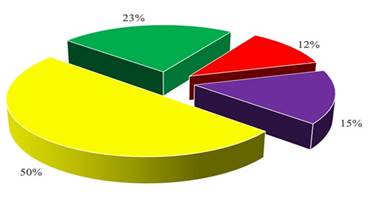

Рис. 3. Диаграмма вариантов одномоментной реконструкции в реципиентной области
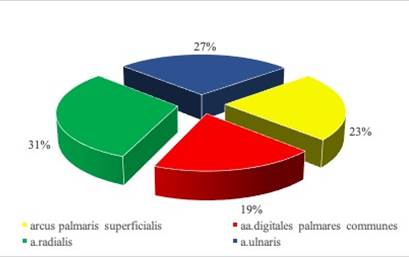
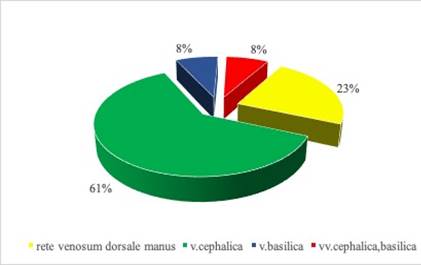
На рисунке 4 представлены варианты подключения сосудов в реципиентной области. В основном использовали лучевую либо локтевую артерии (31% и 27% соответственно), реже – поверхностную ладонную дугу (23%) и межпальцевые артерии (19%). При наложении венозных анастомозов в 61% случаев использовали v. сephalica, а у 23% пациентов – различные ветви венозной сети кисти. Полученные результаты совпадают с данными литературы [14].
А
Б
Рис. 4. Диаграмма вариантов подключения артерий (А) и вен (Б) трансплантатов в реципиентной области
В 84,6% случаев после снятия клипс в течение нескольких минут в трансплантате был восстановлен устойчивый кровоток.
В 11,5% случаев столкнулись с интраоперационными осложнениями. В 3 случаях после снятия клипс не произошло восстановления кровообращения в пересаженном трансплантате, что потребовало проведения ревизии, механического «прокачивания» сосудов и введения сосудорасширяющих препаратов, после чего у 2 пациентов был получен устойчивый кровоток. В 1 случае кровоток получен не был, в связи с чем пересаженный трансплантат был скелетирован, сохранен только костно-сухожильный комплекс тканей, а для восстановления мягких тканей аутотрансплантата выполнена пластика круглым стеблем.
Осложнения II степени были связаны с нарушением микроциркуляции. В литературе нет данных по частоте ревизий сосудистых анастомозов пересаженных аутотрансплантатов у пациентов с SHFM. При свободной аутотрансплантации 2-го пальца стопы на кисть частота ревизий составляет около 6% [12]. В нашем исследовании в 23% случаев в раннем послеоперационном периоде (первые 3 суток) мы наблюдали различные варианты нарушения кровообращения в пересаженных аутотрансплантатах. В 4 случаях отмечена артериальная недостаточность и в 2 – смешанный тип нарушения микроциркуляции. У всех пациентов была произведена ревизия сосудистых анастомозов с наложением реанастомозов, в 2 случаях потребовалась дополнительная венозная вставка. Однако после ревизии сосудистых анастомозов в 4 случаях (осложнения III степени по классификации Caton) в последующем отмечен полный или частичный некроз трансплантата. При иссечении некротических тканей (15–21-е сутки от дня ревизии) в 25% случаев рана закрыта собственными тканями с наложением вторичных швов, а в 75% случаев выполнена комбинированная кожная пластика.
По данным литературы, выживаемость аутотрансплантатов составляет 94–97% [12, 15]. В нашем исследовании выживаемость лоскутов составила 84,6%. Это было связано с выраженными изменениями ангиоархитектоники перемещаемого пальца стопы.
У 73,1% пациентов в последующем проводились различные дополнительные операции с целью улучшения косметического и функционального состояния кистей и стоп.
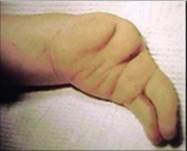
Клинический пример. Пациент С., 2,5 года, поступил с диагнозом: врожденное расщепление кистей и стоп. С учетом клинических данных, выраженного ограничения функции кисти принято решение о выполнении микрохирургической аутотрансплантации 5-го пальца стопы на кисть в позицию 1-го пальца. Послеоперационный период протекал гладко. При контрольном осмотре через 3 года функция двустороннего схвата кисти удовлетворительная (рис. 5).
|
|
Рис. 5. Результат микрохирургической аутотрансплантации 5-го пальца стопы на кисть у пациента с SHFM: А, Б) внешний вид и рентгенограмма кисти до оперативного лечения;
В) этап выделения трансплантата на стопе; Г) внешний вид кисти в конце операции;
Д) отдаленный результат через 3 года после оперативного вмешательства
Заключение. Таким образом, микрохирургическая аутотрансплантация 5-го пальца стопы на кисть возможна даже при крайних степенях недоразвития SHFM. В таких случаях, когда на кисти отсутствуют 1-й, 2-й, 3-й, а часто и 4-й пальцы кисти, для восстановления функции двухстороннего схвата кисти необходимы реконструкция 1-го пальца либо протезирование. Аутотрансплантация 5-го пальца с расщепленной стопы является довольно сложной операцией, поскольку анатомия сосудистого строения стопы значительно отличается от нормальных представлений. Это обстоятельство обусловило больший процент осложнений и некроза пересаженного трансплантата по сравнению с таковыми при стандартной аутотрансплантации пальцев стоп на кисть у детей с нормальным развитием стопы. Тем не менее при использовании такой сложной технологии реконструкции 1-го пальца у детей с SHFM можно получать хороший функциональный результат и приемлемый эстетический вид кисти.




 А
А 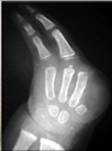 Б
Б 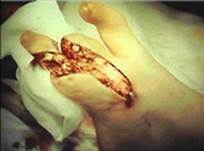 В
В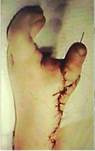 Г
Г  Д
Д