Среди онкологических заболеваний по числу летальных исходов 4-е место занимают злокачественные новообразования кишечника. В данной группе наибольший процент составляют опухоли прямой кишки [1; 2]. В настоящее время для лечения рака прямой кишки применяют комбинированные протоколы, отличающиеся от протоколов для других отделов кишечника, так как сочетают предоперационную лучевую терапию (в стандартном варианте - разовая очаговая доза (РОД) 2,4 Гр до суммарной очаговой дозы (СОД) 54 Гр) и последующее хирургическое вмешательство [3; 4]. Анализ результатов отечественной и мировой радиотерапевтической практики показывает наличие большого числа (до 30-40%) случаев с радиорезистентностью опухолей, обусловленной молекулярными (генетическими/эпигенетическими) аномалиями в опухолевых клетках, в частности аберрантной экспрессией определенных групп генов. Ранее нами было показано, что транскрипционная активность генетических локусов, регулирующих системы репарации (RBBP8, H2AX, BRCA2), пролиферации и апоптоза (CASP9, BCL2), связана с эффективностью проводимой лучевой терапии у больных раком прямой кишки [1]. Как известно, важнейшими регуляторами транскрипционной активности генов являются микроРНК, представляющие собой некодирующие одноцепочечные РНК, содержащие приблизительно два десятка нуклеотидов, осуществляющие регуляцию трансляции и деградации матричной РНК посредством связывания с комплементарными сайтами в нетранслируемых участках молекул последних, служащих их мишенями [5].
Поэтому целью исследования стало выявление с помощью биоинформационного анализа микроРНК, таргетирующих гены RBBP8, H2AX, BRCA2, CASP9 и BCL2, и изучение влияния изменения экспрессии этих микроРНК на эффективность лучевой терапии опухолей прямой кишки.
Материалы и методы исследования
Биоинформационный поиск микроРНК, таргетирующих гены RBBP8, H2AX, BRCA2, CASP9 и BCL2, осуществляли с использованием модифицированного алгоритма TarPmiR и базы данных mirDB. TarPmiR для прогнозирования сайта связывания мРНК и микроРНК использует алгоритм машинного обучения random forest («случайный лес»), сочетающий в себе метод случайных подпространств и метод бэггинга Бреймана. Результатом работы алгоритма является значение вероятности того, что обнаруженный сайт-мишень кандидат и есть истинный сайт-мишень [6; 7].
В исследовании участвовали 32 пациента (возраст от 45 до 65 лет), госпитализированных в ФГБУ «НМИЦ онкологии» с диагнозом аденокарцинома прямой кишки (G1-2). До лучевой терапии (ЛТ) от этих пациентов при проведении видеоколоноскопии (ВКС) получали препараты биопсии - фрагменты немалигнизированных (нормальных) и опухолевых тканей прямой кишки. Фрагменты ткани, извлеченные во время биопсии, мгновенно замораживали при минус 195 °C и в последующем использовали для выделения суммарной РНК. ЛТ проводили по стандартной схеме - РОД 2,4 Гр, СОД 54,0 Гр - на линейном ускорителе частиц Novalis TX.
Препараты суммарной РНК выделяли методом фенол-хлороформной экстракции в модификации [7]. Для выявления микроРНК и малой РНК U6 препараты суммарной РНК подвергали реакции обратной транскрипции (ОТ), которая проводилась одновременно с полиаденилированием РНК, с использованием специфичных RT-праймеров. Олигонуклеотидные праймеры были разработаны нами с использованием алгоритма предложенного Balcells I. [8]. Реакцию ОТ проводили в одном повторе, отдельно для каждой микроРНК, для этого использовали лиофилизированную смесь «Мастер-микс ОТ» («Вектор-Бест», Россия). ОТ проводили при 16 °С (15 минут), далее при 42 °С (15 минут), обратную транскриптазу инактивировали инкубацией при 95 °С в течение 2 минут [7].
Относительную экспрессию микроРНК оценивали методом RT-qPCR. Постановку RT-qPCR каждого образца проводили в 3 повторах. Для подбора референсных локусов оценивали стабильность экспрессии микроРНК по алгоритму geNorm [9]. Первоначальный список предполагаемых референсных локусов для микро-РНК включал: miR-191; miR-23a и U6. С помощью geNorm для нормализации данных по экспрессии микроРНК был выбран U6. Нормализацию проводили по референсному локусу и уровню экспрессии соответствующих микроРНК в образцах нормальной ткани. Относительную экспрессию микроРНК (RЕmir) определяли по формуле RЕmir=Е-ΔΔCt, где Е - вычисленная эффективность реакции амплификации [5].
Статистический анализ данных проводили с использованием языка программирования Python (библиотека SciPy). Различия между группами оценивались с использованием U-критерия Манна-Уитни, для корректировки множественного сравнения была применена поправка Бонферрони [7]. Также проводили анализ избыточной представленности микроРНК в сигнальных путях (ORA, Over-Representation Analysis). Этот метод определяет долю участия дифференциально экспрессирующихся микроРНК в определенных сигнальных путях, его результатом является получение списка наиболее значимых сигнальных путей. Статистическая значимость в ORA рассчитывалась с применением точного критерия Фишера [10].
Результаты исследования и их обсуждение
Биоинформационный поиск микроРНК, таргетирующих гены RBBP8, H2AX, BRCA2, CASP9 и BCL2, с использованием модифицированного алгоритма TarPmiR, выявил 1338 микроРНК (рис. 1А), из которых валидированы в базе данных miRDB 86 микроРНК (рис. 1Б), в том числе 26 с минимальным значением термодинамического потенциала (свободной энергии) взаимодействия микроРНК и матричной РНК (табл. 1): 9 микроРНК, взаимодействующих с BCL2, 2 микроРНК, взаимодействующие с BRCA2, 12 микроРНК, взаимодействующих с CASP9, 2 микроРНК, взаимодействующие с H2AX, и 1 микроРНК, взаимодействующая с RBBP8.
Таблица 1
МикроРНК, таргетирующие гены RBBP8, H2AX, BRCA2, CASP9 и BCL2, выявленные с использованием алгоритма TarPmiR*
|
МикроРНК |
RefSeq id |
Ген |
Координаты в геноме |
Энергия |
AU |
Длина участка связывания, п.н. |
Участок связывания |
Валидировано в miRDB |
|
|
start |
end |
||||||||
|
hsa-miR-1249-5p |
NM_000633 |
BCL2 |
3468 |
3517 |
-30.1 |
0.382 |
49 |
3UTR |
да |
|
hsa-miR-6861-5p |
NM_000633 |
BCL2 |
3474 |
3513 |
-29.6 |
0.368 |
20 |
3UTR |
да |
|
hsa-miR-8052 |
NM_000633 |
BCL2 |
4393 |
4412 |
-29.3 |
0.412 |
19 |
3UTR |
да |
|
hsa-miR-324-3p |
NM_000633 |
BCL2 |
4680 |
4700 |
-28.6 |
0.618 |
20 |
3UTR |
да |
|
hsa-miR-6820-3p |
NM_000633 |
BCL2 |
1670 |
1701 |
-28.1 |
0.456 |
31 |
3UTR |
да |
|
hsa-miR-4717-5p |
NM_000633 |
BCL2 |
2322 |
2364 |
-28.0 |
0.368 |
18 |
3UTR |
да |
|
hsa-miR-3943 |
NM_000633 |
BCL2 |
2750 |
2774 |
-27.8 |
0.632 |
24 |
3UTR |
да |
|
hsa-miR-557 |
NM_000633 |
BCL2 |
2549 |
2584 |
-27.6 |
0.5 |
20 |
3UTR |
да |
|
hsa-miR-4690-5p |
NM_000633 |
BCL2 |
2147 |
2172 |
-27.3 |
0.426 |
25 |
3UTR |
да |
|
hsa-miR-6757-3p |
NM_000059 |
BRCA2 |
10786 |
10812 |
-25.7 |
0.412 |
26 |
3UTR |
да |
|
hsa-miR-7151-3p |
NM_000059 |
BRCA2 |
10797 |
10825 |
-25.1 |
0.441 |
20 |
3UTR |
да |
|
hsa-miR-6779-5p |
XM_011542273 |
CASP9 |
1482 |
1537 |
-34.3 |
0.441 |
35 |
3UTR |
да |
|
hsa-miR-1273h-5p |
NM_032996 |
CASP9 |
2555 |
2590 |
-33.1 |
0.456 |
23 |
3UTR |
да |
|
hsa-miR-6812-5p |
NM_001229 |
CASP9 |
2593 |
2622 |
-30.6 |
0.441 |
29 |
3UTR |
да |
|
hsa-miR-6737-5p |
NM_032996 |
CASP9 |
1329 |
1347 |
-30.1 |
0.5 |
18 |
3UTR |
да |
|
hsa-miR-661 |
XM_011542273 |
CASP9 |
1516 |
1552 |
-29.8 |
0.456 |
36 |
3UTR |
да |
|
hsa-miR-6799-5p |
NM_032996 |
CASP9 |
2609 |
2656 |
-29.7 |
0.574 |
23 |
3UTR |
да |
|
hsa-miR-6893-5p |
NM_032996 |
CASP9 |
2442 |
2484 |
-28.5 |
0.574 |
42 |
3UTR |
да |
|
hsa-miR-6819-5p |
NM_032996 |
CASP9 |
1329 |
1347 |
-27.0 |
0.5 |
18 |
3UTR |
да |
|
hsa-miR-6874-5p |
NM_001278054 |
CASP9 |
2505 |
2535 |
-26.6 |
0.559 |
30 |
3UTR |
да |
|
hsa-miR-4728-5p |
NM_001229 |
CASP9 |
2906 |
2925 |
-26.3 |
0.426 |
19 |
3UTR |
да |
|
hsa-miR-6808-5p |
NM_032996 |
CASP9 |
1588 |
1610 |
-26.2 |
0.471 |
22 |
3UTR |
да |
|
hsa-miR-30b-3p |
XM_011542273 |
CASP9 |
1967 |
1987 |
-25.6 |
0.485 |
20 |
3UTR |
да |
|
hsa-miR-3202 |
NM_002105 |
H2AFX |
620 |
639 |
-20.3 |
0.221 |
19 |
3UTR |
да |
|
hsa-miR-5195-3p |
NM_002105 |
H2AFX |
1478 |
1504 |
-23.8 |
0.471 |
26 |
3UTR |
да |
|
hsa-miR-130b-3p |
NM_002894 |
RBBP8 |
3196 |
3215 |
-23.7 |
0.676 |
19 |
3UTR |
да |
* - представлены только микроРНК, валидированные в базе данных miRDB и с минимальной свободной энергией взаимодействия микроРНК и матричной РНК.
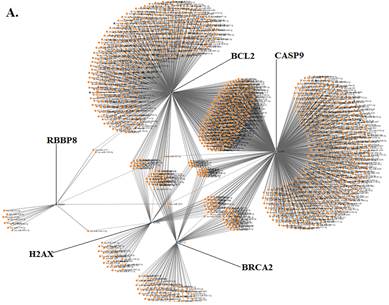
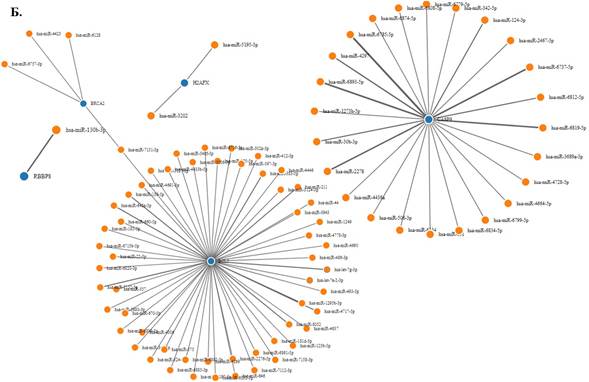
Рис. 1. А - все микроРНК, таргетирующие гены RBBP8, H2AX, BRCA2, CASP9 и BCL2, выявленные с использованием алгоритма TarPmiR. Б - микроРНК, выявленные с использованием алгоритма TarPmiR и валидированные в базе данных miRDB
Для 26 микроРНК, выявленных с использованием биоинформационных подходов, проведено профилирование экспрессии в нормальных и опухолевых тканях у больных раком прямой кишки.
Анализ результатов ЛТ опухолей прямой кишки у 32 больных позволил разделить их на 2 группы. У 17 больных после ЛТ был зафиксирован полный регресс опухоли (группа 1), у 8 больных был зафиксирован незначительный регресс опухоли, и у 7 больных отсутствовала динамика изменения размера опухоли (группа 2). В этих двух группах пациентов наблюдалась дифференциальная экспрессия ряда микроРНК (как относительно нормальной ткани, так и относительно каждой из групп). Так, у больных с незначительным регрессом опухоли или отсутствием динамики после лучевой терапии (n=15) выявлено статистически значимое (p<0,05) снижение экспрессии miR-1249 в 2,5 раза относительно экспрессии в нормальной ткани и в 2,3 раза относительно экспрессии в опухолевой ткани больных с полным регрессом опухоли, снижение экспрессии miR-6820 в 1,7 раза относительно экспрессии в нормальной ткани и в 1,6 раза относительно экспрессии в опухолевой ткани у больных с полным регрессом опухоли, снижение miR-4717 в 2,5 раза относительно нормальной ткани, снижение hsa-miR-3943 в 3,3 раза по сравнению с уровнем экспрессии в нормальной ткани, снижение miR-557 в 2,5 раза относительно нормальной ткани и в 2,3 раза относительно пациентов с полным регрессом опухоли, при этом наблюдается увеличение экспрессии hsa-miR-4690-5p в 2,1 раза относительно нормальной ткани (рис. 2).
Также у больных с полным регрессом опухоли была снижена экспрессия miR-4717 в 1,8 раза (р<0,05) относительно уровня экспрессии в нормальной ткани прямой кишки. Данные микроРНК (miR-557, miR-1249, miR-6820, miR-4717, miR-3943), за исключением miR-4717, в опухолевой ткани у больных с незначительным регрессом опухоли или отсутствием динамики обладают преимущественно сниженной экспрессией как относительно нормальной ткани, так и относительно опухолевой ткани пациентов с полным регрессом опухоли после лучевой терапии. Эти микроРНК таргетируют антиапоптозный ген BCL2, и их сниженная активность может способствовать сохранению на повышенном уровне транскрипционной активности этого гена-мишени. BCL2 кодирует белок, участвующий в подавлении апоптоза двумя путями: во-первых, этот белок изменяет проницаемость мембран митохондрий и предотвращает выход из них цитохрома C, тем самым останавливая активацию каспазного каскада; во-вторых, он инактивирует белок CED4 (фактор активации апоптоза) [11]. Соответствующий эффект увеличения экспрессии гена BCL2 у пациентов с незначительным регрессом опухоли или отсутствием динамики после лучевой терапии мы и обнаружили в предыдущем исследовании [1].
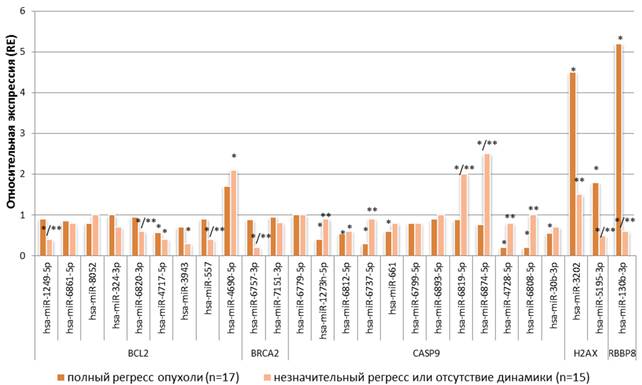
Рис. 2. Уровень экспрессия микроРНК в ткани опухоли прямой кишки больных с полным регрессом (группа 1) или его отсутствием (группа 2). * – статистически значимые отличия (р<0,05) относительно уровня экспрессии в нормальной ткани, ** – статистически значимые отличия (р<0,005) экспрессии микроРНК в опухолевой ткани пациентов
группы 2 от группы 1
Также в опухолевой ткани у больных с незначительным регрессом опухоли или отсутствием динамики после лучевой терапии обнаружено статистически значимое (p<0,05) снижение экспрессии микроРНК-6757 в 5,0 раз относительно уровня экспрессии в нормальной ткани и в 4,4 раза относительно экспрессии в опухолевой ткани у больных с полным регрессом опухоли. Данная микроРНК таргетирует ген BRCA2, и её снижение теоретически должно способствовать увеличению экспрессии BRCA2, что показано нами ранее [1].
Экспрессия miR-1273h, miR-6737, miR-661, miR-4728, miR-6808 и miR-30b статистически значимо (p<0,05) снижена в 2,5; 3,3; 1,7; 5,0; 5,0 и 1,8 раза в опухолевой ткани у больных с полным регрессом опухоли относительно нормальной ткани. При этом уровень экспрессии miR-1273h в 2,3 раза, miR-6819 в 2,3 раза, miR-6737 в 3,0 раза, miR-6874 в 3,3 раза, miR-4728 в 4,0 раза и miR-6808 в 5,0 раз статистически значимо (p<0,05) выше в опухолевой ткани у больных с незначительным регрессом опухоли/ отсутствием динамики после лучевой терапии относительно аналогичных показателей в опухолевой ткани больных с полным регрессом опухоли. Следует отметить, что hsa-miR-6812-5p статистически значимо (p<0,005) снижает экспрессию в опухолевой ткани пациентов группы 1 и 2 в 1,9 и 1,7 раза соответственно относительно нормальной ткани прямой кишки. Указанные выше микроРНК таргетируют ген каспазы-9, и теоретически их высокая экспрессия у больных с незначительным регрессом опухоли/ отсутствием динамики должна способствовать снижению экспрессии этого гена, а их более низкая экспрессия у больных с полным регрессом опухоли, наоборот, должна способствовать повышенному уровню транскрипционной активности гена инициаторной каспазы-9, выполняющей критическую для запуска апоптоза функцию. Дифференциальная экспрессия CASP9 в этих двух группах больных была обнаружена в нашем предыдущем исследовании [1].
В опухолевой ткани у пациентов с полным регрессом опухоли обнаружено статистически значимое (p<0,05) увеличение экспрессии микроРНК miR-3202 и miR-5195 в 4,5 и 1,8 раза соответственно относительно экспрессии в нормальной ткани и в 3,0 и 3,6 раза соответственно относительно экспрессии в опухолевой ткани у пациентов с незначительным регрессом опухоли/отсутствием динамики после лучевой терапии. Эти две микроРНК таргетируют H2AFX (H2AX) - ген, который кодирует гистоновый белок, инициирующий ремоделирование хроматина при двуцепочечных разрывах в ДНК, вызванных ионизирующим облучением. Такое ремоделирование хроматина позволяет белку BRCA1/2 связаться с участком ДНК, на котором произошел двуцепочечный разрыв [12; 13]. Соответственно, повышенная экспрессия miR-3202 и miR-5195 у больных с полным регрессом опухоли будет способствовать сниженной экспрессии гена H2AX, а обратный эффект будет наблюдаться у больных с незначительным регрессом опухоли/ отсутствием динамики после лучевой терапии, что находит подтверждение в результатах исследования Кутилина Д.С. и соавторов [1], выполненного в 2019 году.
Также обнаружено статистически значимое (p<0,05) повышение уровня экспрессии miR-130b в 5,2 раза в опухолевой ткани у больных с полным регрессом опухоли и снижение в 1,7 раза в опухолевой ткани у больных с незначительным регрессом опухоли или отсутствием динамики относительно нормальной ткани прямой кишки. При этом у больных первой группы экспрессия hsa-miR-130b-3p была в 8,7 раза выше (p<0,05) по сравнению с больными второй группы. Это, очевидно, способствовало снижению экспрессии гена RBBP8 у больных первой группы и повышению его экспрессии у больных второй группы, показанному в работе Кутилина Д.С. и соавторов [1]. Данный ген кодирует белок, регулирующий пролиферацию клеток [14].
Как известно, микроРНК имеют множество мишеней [5; 15], поэтому для дифференциально экспрессирующихся (hsa-miR-130b-3p, hsa-miR-6819-5p, hsa-miR-1249-5p, hsa-miR-6874-5p, hsa-miR-4728-5p, hsa-miR-6808-5p, hsa-miR-3202, hsa-miR-5195-3p, hsa-miR-6820-3p, hsa-miR-557, hsa-miR-6757-3p, hsa-miR-1273h-5p, hsa-miR-6737-5p) в опухолевых тканях двух групп пациентов микроРНК был проведен анализ избыточной представленности микроРНК в сигнальных путях (ORA, Over-Representation Analysis). Результаты анализа представлены в таблице 2.
Таблица 2
Представленность (over-represented) дифференциально экспрессирующихся микроРНК в сигнальных путях (KEGG Pathways)
|
Сигнальный путь |
P-value |
Кол-во miRNA |
микроРНК |
|
Переваривание и всасывание белков |
0,0005 |
11 |
miRNA-130b, miRNA-557, miRNA-3202, miRNA-1273h, miRNA-6737, miRNA-6819, miRNA-4728, miRNA-6808, miRNA-6757, miRNA-5195, miRNA-1249 |
|
Апоптоз |
0,0006 |
11 |
miRNA-1249, miRNA-6820, miRNA-557, miRNA-6757, miRNA-1273h, miRNA-6737, miRNA-6819, miRNA-4728, miRNA-6808, miRNA-3202, miRNA-130b |
|
Сигнальные каскады эпителиальных клеток при инфекции Helicobacter pylori |
0,0010 |
11 |
miRNA-1249, miRNA-6820, miRNA-557, miRNA-6757, miRNA-1273h, miRNA-6737, miRNA-6819, miRNA-4728, miRNA-3202, miRNA-5195, miRNA-130b |
|
Сигнальный путь Notch |
0,0023 |
10 |
miRNA-1249, miRNA-557, miRNA-1273h, miRNA-6737, miRNA-6819, miRNA-4728, miRNA-6808, miRNA-3202, miRNA-5195, miRNA-130b |
|
Сигнальный путь RIG-I-подобного рецептора |
0,0027 |
10 |
miRNA-1249, miRNA-6820, miRNA-557, miRNA-6757, miRNA-6737, miRNA-6819, miRNA-4728, miRNA-6808, miRNA-3202, miRNA-130b |
|
Сигнальный путь Wnt |
0,0060 |
13 |
miRNA-1249, miRNA-6820, miRNA-557, miRNA-6757, miRNA-1273h, miRNA-6737, miRNA-6819, miRNA-6874, miRNA-4728, miRNA-6808, miRNA-3202, miRNA-5195, miRNA-130b |
|
Сигнальный путь p53 |
0,0061 |
13 |
miRNA-1249, miRNA-6820, miRNA-557, miRNA-6757, miRNA-1273h, miRNA-6737, miRNA-6819, miRNA-6874, miRNA-4728, miRNA-6808, miRNA-3202, miRNA-5195, miRNA-130b |
|
Окислительное фосфорилирование |
0,0062 |
11 |
miRNA-1249, miRNA-6757, miRNA-1273h, miRNA-6737, miRNA-6819, miRNA-6874, miRNA-4728, miRNA-6808, miRNA-3202, miRNA-5195, miRNA-130b |
|
Сигнальный путь IL-17 |
0,0079 |
11 |
miRNA-1249, miRNA-6820, miRNA-557, miRNA-6757, miRNA-1273h, miRNA-6737, miRNA-6819, miRNA-4728, miRNA-6808, miRNA-3202, miRNA-130b |
|
Метаболизм лекарств |
0,0094 |
8 |
miRNA-1249, miRNA-557, miRNA-6737, miRNA-6819, miRNA-4728, miRNA-6808, miRNA-3202, miRNA-130b |
|
Сигнальные пути сфинголипидов |
0,0173 |
12 |
miRNA-1249, miRNA-6820, miRNA-557, miRNA-6757, miRNA-1273h, miRNA-6737, miRNA-6819, miRNA-4728, miRNA-6808, miRNA-3202, miRNA-5195, miRNA-130b |
|
Некроптоз |
0,0174 |
12 |
miRNA-1249, miRNA-6820, miRNA-557, miRNA-6757, miRNA-1273h, miRNA-6737, miRNA-6819, miRNA-4728, miRNA-6808, miRNA-3202, miRNA-5195, miRNA-130b |
|
Сплайсосома |
0,0180 |
12 |
miRNA-1249, miRNA-557, miRNA-6757, miRNA-1273h, miRNA-6737, miRNA-6819, miRNA-6874, miRNA-4728, miRNA-6808, miRNA-3202, miRNA-5195, miRNA-130b |
|
Транспорт РНК |
0,0228 |
12 |
miRNA-1249, miRNA-6820, miRNA-4728, miRNA-6808, miRNA-3202, miRNA-5195, miRNA-6757, miRNA-1273h, miRNA-6737, miRNA-6819, miRNA-6874, miRNA-130b |
|
Сигнальный путь Toll-подобного рецептора |
0,0262 |
10 |
miRNA-1249, miRNA-6820, miRNA-557, miRNA-6757, miRNA-6737, miRNA-6819, miRNA-4728, miRNA-6808, miRNA-3202, miRNA-130b |
|
Сигнальный путь NOD-подобного рецептора |
0,0318 |
12 |
miRNA-1249, miRNA-6820, miRNA-557, miRNA-6757, miRNA-1273h, miRNA-6737, miRNA-6819, miRNA-6874, miRNA-4728, miRNA-6808, miRNA-3202, miRNA-130b |
|
Биогенез рибосом |
0,0360 |
9 |
miRNA-1249, miRNA-557, miRNA-6757, miRNA-1273h, miRNA-4728, miRNA-6808, miRNA-3202, miRNA-5195, miRNA-130b |
|
Сигнальный путь TGF-beta |
0,0386 |
11 |
miRNA-1249, miRNA-6820, miRNA-557, miRNA-1273h, miRNA-6737, miRNA-6819, miRNA-4728, miRNA-6808, miRNA-3202, miRNA-5195, miRNA-130b |
|
Клеточное старение |
0,0396 |
13 |
miRNA-1249, miRNA-6820, miRNA-557, miRNA-6757, miRNA-1273h, miRNA-6737, miRNA-6819, miRNA-6874, miRNA-4728, miRNA-6808, miRNA-3202, miRNA-5195, miRNA-130b |
|
Сигнальный путь нейротрофина |
0,0404 |
12 |
miRNA-1249, miRNA-6820, miRNA-557, miRNA-6757, miRNA-1273h, miRNA-6737, miRNA-6819, miRNA-4728, miRNA-6808, miRNA-3202, miRNA-5195, miRNA-130b |
|
Сигнальный путь ABC транспортеров |
0,0431 |
6 |
miRNA-557, miRNA-1273h, miRNA-4728, miRNA-6808, miRNA-5195, miRNA-130b |
|
Сигнальный путь VEGF |
0,0444 |
9 |
miRNA-1249, miRNA-6820, miRNA-6757, miRNA-6737, miRNA-6819, miRNA-4728, miRNA-6808, miRNA-3202, miRNA-130b |
|
Формирование плотных контактов |
0,0453 |
12 |
miRNA-1249, miRNA-6820, miRNA-557, miRNA-1273h, miRNA-6737, miRNA-6819, miRNA-6874, miRNA-4728, miRNA-6808, miRNA-3202, miRNA-5195, miRNA-130b |
|
Цитомегаловирусная инфекция человека |
0,0469 |
13 |
miRNA-1249, miRNA-6820, miRNA-557, miRNA-6757, miRNA-1273h, miRNA-6737, miRNA-6819, miRNA-6874, miRNA-4728, miRNA-6808, miRNA-3202, miRNA-5195, miRNA-130b |
|
Убиквитин-опосредованный протеолиз |
0,0481 |
11 |
miRNA-1249, miRNA-6820, miRNA-557, miRNA-1273h, miRNA-6737, miRNA-6819, miRNA-6874, miRNA-4728, miRNA-6808, miRNA-3202, miRNA-130b |
Как видно из представленных в таблице 2 данных, дифференциально экспрессирующиеся в двух группах пациентов микроРНК, помимо регуляции транскрипционной активности генов RBBP8, H2AX, BRCA2, CASP9 и BCL2, участвуют в следующих ключевых сигнальных путях и биологических процессах: апоптоз, окислительное фосфорилирование, убиквитин-опосредованный протеолиз, формирование клеточных плотных контактов, сигнальный путь VEGF, сигнальный путь Toll-подобного рецептора и NOD-подобного рецептора, сигнальный путь Notch и Wnt, сигнальный путь p53 и др. (табл. 2, рис. 3).

Рис. 3. Облако категорий (wordcloud of categories) сигнальных путей дифференциально экспрессирующихся микроРНК (100 категорий с наименьшим значением P-value)
Заключение
Данное исследование выявило, что эффективность ЛТ опухолей прямой кишки может быть ассоциирована с дифференциальной экспрессией 13 микроРНК (miRNA-130b, miRNA-1249, miRNA-6820, miRNA-6757, miRNA-1273h, miRNA-6737, miRNA-6819, miRNA-557, miRNA-6874, miRNA-4728, miRNA-6808, miRNA-3202, miRNA-5195), которая обеспечивает эффективную регуляцию системы восстановления двухцепочечных разрывов ДНК (увеличение экспрессии BRNACA2, H2AX и RNABBP8 при снижении экспрессии miRNA-6757, miRNA-3202, miRNA-5195 и miRNA-130b, и наоборот) и регуляцию апоптоза (увеличение экспрессии CASP9 при снижении экспрессии miRNA-1273h, miRNA-6737, miRNA-661, miRNA-4728 и miRNA-6808, снижение экспрессии BCL2 при повышении экспрессии miRNA-1249, miRNA-6820, miRNA-557, и наоборот).
Исследование выполнено в рамках гос. задания «Поиск предикторов радиорезистентности рака прямой кишки и разработка персонифицированных неоадъювантных терапевтических подходов».



