Определение высоко- и низкомолекулярных биологически активных соединений представляет как практический, так и теоретический интерес для изучения их свойств, содержания в биологических жидкостях, влияния на организм человека и животных, фармакокинетики, структуры синтезированных соединений и биохимических реакций с их участием. Биологически активные соединения способны оказывать положительное или отрицательное воздействие на организм в зависимости от концентрации и длительности воздействия. Кроме того, в связи с широким применением высокоэффективных биологически активных соединений в других областях жизнедеятельности (например, в сельском хозяйстве) в воде и пищевых продуктах могут содержаться остатки этих препаратов в количествах, превышающих безопасный уровень [6]. В связи с требованиями повышения качества жизни и увеличением поступлений фальсифицированной продукции на фармацевтический рынок, в последнее время необходимы разнообразные варианты количественного определения широкого круга биологически активных соединений для оценки их качества, а также для определения их содержания в организме человека и животных.
Весьма перспективными в этом отношении являются биосенсоры, обладающие преимуществом on-site тестирования и позволяющие одновременно анализировать большое количество образцов [3]. Интерес к биосенсорным методам анализа связан с возможностью относительно простого варьирования селективности определений по отношению к ряду соединений. Несмотря на существующие варианты биосенсорного анализа, разнообразие объектов исследования, усложнение аналитических задач требуют дальнейшего усовершенствования подходов к разработке вариантов анализа и схем био- и иммуносенсорных методов [4].
Новейшие достижения в области создания электрохимических био- и иммуносенсоров связаны с разработкой и получением новых функциональных материалов для физического трансдьюсера. Развиваются методы хемо- и биоселективного распознавания и связывания, а также эффективные методы микро- и наноструктурирования. Для электрохимических детекторов перспективным материалом являются тонкие пленки [2].
Применение органических материалов расширяет функциональные возможности тонких пленок. К тому же технология органических тонких пленок значительно проще по сравнению с традиционным материалом - кремнием. Удобным свойством органических пленок является возможность их функционализации [5].
Среди тонких пленок в настоящее время особый интерес проявляется к проводящим пленкам Ленгмюра-Блоджетт на основе квазиодномерных комплексов с переносом заряда [1]. Высокая проводимость пленок Ленгмюра-Блоджетт - необходимое условие их использования в качестве материалов в тонкопленочных структурах биосенсорных устройств. В результате интенсивных исследований последнего времени электропроводность пленок удалось повысить почти на два порядка величины: с 0,5-1 См/см в начале 90-х годов ХХ века до 40 См/см в 2001 году.
Несмотря на большое научное и практическое значение исследований внутрикристаллитного транспорта в пленках Ленгмюра-Блоджетт, работы, посвященные этому вопросу, немногочисленны, главным образом, из-за серьезных трудностей, обусловленных спецификой ленгмюровских систем (их поликристалличностью, исключительной тонкостью, невозможностью отделения пленок от поддерживающих их подложек) [7].
Цель исследования
Настоящее исследование направлено на изучение функциональных характеристик и потребительских свойств биосенсоров на основе пленок Ленгмюра-Блоджетт, полученных ранее.
Материалы и методы исследования
Тонкие пленки получали методом Ленгмюра-Блоджетт, позволяющий воспроизводимо получать молекулярные моно- и мультислои на основе органических веществ [1]. Пленка в данном случае формируется в результате последовательного переноса монослоев поверхностно активных веществ (ПАВ) с поверхности воды или водного раствора на твердую подложку. Монослой представляет собой слой из близко находящихся в плоскости, а не в пространстве, молекул того или иного вещества. В качестве ПАВ в работе использовали поли(a-L-глутаминовой кислоты)-β-поли(g-метил-L-глутамат-g-стерил-L-глутамат) (ПLГК-β-ПMLГСLГ).
Установка для получения и изучения пленок Ленгмюра-Блоджетт представлена на рис. 1.
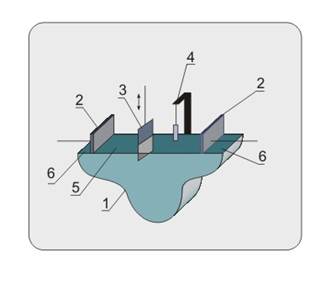
Рис. 1. Установка для получения пленок Ленгмюра-Блоджетт: 1 - ванна, 2 - поверхностные барьеры, 3 - подложка, 4 - электронные весы Вильгельми, 5 - поверхность воды с ПАВ, 6 - поверхность воды без ПАВ
Основная идея метода заключается в формировании на водной поверхности мономолекулярного слоя амфифильного вещества и последующем его переносе на твердую подложку. В водной фазе молекулы амфифильного вещества располагаются на поверхности раздела «воздух - вода». Для формирования поверхностного мономолекулярного слоя использовали сжатие поверхностного слоя с помощью специальных поршней. При последовательном изотермическом сжатии изменяется структура мономолекулярной пленки, которая проходит через ряд двухмерных состояний, условно именуемых состояниями газа, жидкого кристалла и твердого кристалла. Перенос пленки на твердый носитель осуществляли погружением в раствор и последующим извлечением из него плоской подложки, на которой при этом происходит адсорбция поверхностной пленки.
Время отклика биосенсоров определяли с помощью секундомера, регистрируя минимальный промежуток времени от момента помещения биосенсора в анализируемый образец до регистрации сигнала.
Операционную стабильность биосенсоров определяли путем измерения сигнала электрода через определенные промежутки времени.
Пороговую чувствительность биосенсоров определяли путем измерения отклика биосенсоров при разных значениях концентрации биологически активных веществ.
Погрешность, воспроизводимость измерения биосенсоров определяли методами математической статистики.
Селективность биосенсоров определяли путем измерения аналитического сигнала биосенсора от данного биологически активного вещества в присутствии других биологически активных веществ.
Стабильность при хранении биосенсоров определяли путем измерения отклика биосенсора через определенные промежутки времени при хранении при следующих параметрах окружающей среды: температура окружающей среды - от +5 ºС до +35 ºС; относительная влажность воздуха - до 75 % при 25 °С.
Результаты исследования и их обсуждение
В ходе предварительных исследований были сконструированы биосенсоры для определения биологически активных соединений, состоящие из кварцевой измерительной кюветы, носителя для селективных средств детекции биологически активных соединений - пленки Ленгмюра-Блоджетт на основе квазиодномерных комплексов с переносом заряда и электрохимического преобразователя, выполняющего роль устройства регистрации и обработки сигналов.
В настоящей работе ставилась задача установления таких функциональных и потребительских характеристик разработанных биосенсоров, как длительность определения, операционная стабильность (изменение аналитических характеристик сенсора при нахождении электрода в постоянном потоке раствора определенной концентрации); допустимая массовая доля мешающих примесей при работе биосенсора; температура окружающей среды; относительная влажность воздуха.
Важными характеристиками биосенсоров являются время отклика (длительность определения) и операционная стабильность - изменение аналитических характеристик биосенсора при нахождении электрода в постоянном потоке раствора определенной концентрации. Результаты определения этих характеристик для исследуемых биосенсоров представлены в табл. 1.
Таблица 1 Функциональные характеристики биосенсоров для определения биологически активных соединений
|
Биологически активное соединение |
Длительность определения, мин |
Операционная стабильность, сутки |
|
Левокарнитин |
1,0 |
60 |
|
Цианокобаламин |
2,5 |
180 |
|
Дигидротахистерол |
1,5 |
180 |
|
Пиридоксин |
1,0 |
120 |
|
Таурин |
5,0 |
60 |
|
Гидроксипролин |
3,0 |
120 |
|
Эстераза |
1,0 |
120 |
При эксплуатации биосенсоров важное значение имеют их потребительские характеристики: габаритные размеры, масса, энергопотребление и т.д. В настоящем исследовании все разработанные биосенсоры имеют габаритные размеры 7 см в каждом из трех измерений, массу 350 г. Для них обеспечивается возможность электрического питания от батарей или аккумуляторов автомобиля, характеризуются низким энергопотреблением и возможностью выполнения измерений в любом необходимом направлении.
Исследования показали, что разработанные биосенсоры для определения биологически активных соединений обеспечивают возможность проведения анализа при следующих параметрах внешних условий: массовая доля мешающих примесей - не выше 20 %; температура окружающей среды - от +5 ºС до +35 ºС; относительная влажность воздуха - до 75 % при 25 °С.
Эффективность биосенсора определяется его аналитическими характеристиками. Последние включают свойства аналитического сигнала (величина и время отклика) в ответ на добавление анализируемого вещества, обратимость системы после удаления аналита, стабильность датчика и многие другие. Параметры калибровочных зависимостей биосенсоров для определения биологически активных соединений представлены в табл. 2.
Линейный диапазон калибровочных зависимостей различался для разных биосенсоров. Минимальная нижняя граница определения характерна для дигидротахистерола и составляет 0,01 мМ, максимальная верхняя граница - для таурина и равна 10,00 мМ. Минимальная чувствительность определения, равная 20 мА/М·см2, характерна для дигидротахистерола, пиридоксина и эстеразы. Воспроизводимость сигнала исследуемых биосенсоров составляет от 2,0 до 2,5 %. Калибровочные кривые для изучаемых биосенсоров представлены на рис. 2.
Таблица 2 Параметры калибровочных зависимостей для определения биологически активных соединений
|
Биологически активное соединение |
Линейный диапазон детекции, мМ |
Чувствительность, мА/М·см2 |
Погрешность измерения концентрации аналита, % |
Воспроизводимость сигнала, % |
|
1 |
2 |
3 |
4 |
5 |
|
Левокарнитин |
0,05-5,00 |
25 |
2,0 |
2,0 |
|
Цианокобаламин |
0,05-5,00 |
30 |
2,0 |
2,5 |
|
Дигидротахистерол |
0,01-2,00 |
20 |
5,0 |
2,0 |
|
Пиридоксин |
0,02-2,00 |
20 |
2,5 |
2,0 |
|
Таурин |
0,05-10,00 |
25 |
2,5 |
2,0 |
|
Гидроксипролин |
0,04-4,00 |
25 |
5,0 |
2,5 |
|
Эстераза |
0,05-5,00 |
20 |
2,0 |
2,5 |
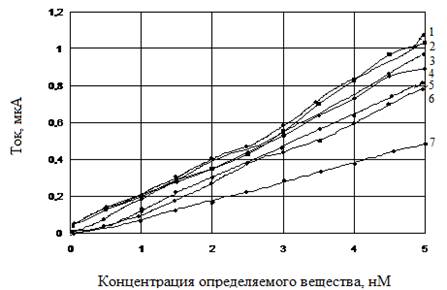
Рис. 2. Калибровочная кривая биосенсоров для определения биологически активных соединений: 1 - таурин, 2 - эстераза, 3 - гидроксипролин, 4 - цианокобаламин, 5 - левокарнитин, 6 - дигидротахистерол, 7 - пиридоксин
Результаты определения селективности биосенсоров представлены в табл. 3.
Результаты, представленные в табл. 3, свидетельствуют о высокой селективности разработанных биосенсоров, поскольку показания биосенсоров не зависят от присутствия в образце посторонних биологически активных веществ.
Таблица 3 Результаты определения селективности биосенсоров
|
Наименование соединения |
Исходное содержание биологически активного соединения (мМ) в анализируемом образце |
Содержание биологически активного соединения (мМ) в образце в присутствии трех других веществ в количестве 2,00 мМ |
|
1 |
2 |
3 |
|
Левокарнитин |
3,95±0,05 |
3,93±0,05 |
|
Цианокобаламин |
1,99±0,01 |
2,00±0,01 |
|
Дигидротахистерол |
1,00±0,01 |
0,99±0,01 |
|
Пиридоксин |
0,99±0,01 |
1,00±0,01 |
|
Турин |
4,95±0,05 |
5,00±0,05 |
|
Гидроксипролин |
2,00±0,01 |
1,99±0,01 |
|
Эстераза |
1,55±0,01 |
1,52±0,01 |
Изучение стабильности разработанных биосенсоров для определения биологически активных соединений проводили при изучении их первоначальной активности и активности после выдерживания в соответствующих буферных растворах при следующих параметрах окружающей среды: температура окружающей среды - от +5 ºС до +35 ºС; относительная влажность воздуха - до 75 % при 25 °С. Полученные результаты представлены на рис. 3.
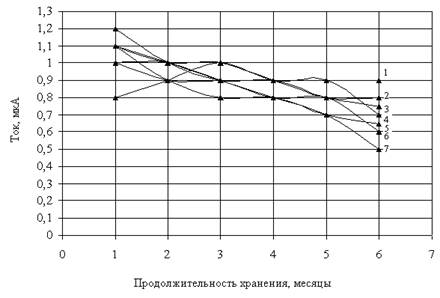
Рис. 3. Изменение сигнала биосенсоров для определения биологически активных соединений при хранении в соответствующих буферных растворах: 1 - таурин, 2 - эстераза, 3 - гидроксипролин, 4 - цианокобаламин, 5 - левокарнитин, 6 - дигидротахистерол, 7 - пиридоксин
Из рис. 3 следует, что стабильность всех исследуемых биосенсоров при определении биологически активных веществ является высокой даже по истечение 6 месяцев хранения. Максимальная стабильность характерна для биосенсора для определения эстеразы, а минимальная - для определения пиридоксина.
Таким образом, в работе изучены функциональные характеристики и потребительские свойства биосенсоров на основе пленок Ленгмюра-Блоджетт для определения биологически активных соединений: левокарнитина, цианокобаламина, дигидротахистерола, пиридоксина, таурина, гидроксипролина, эстеразы. Установлено, что длительность определения разработанными биосенсорами составляет от 1,0 до 3,0 мин, а операционная стабильность - от 60 до 180 суток.
Проведены испытания эффективности применения разрабатываемых биосенсоров при определении биологически активных веществ. Показано, что минимальным пределом определения биологически активных веществ разработанными биосенсорами является 0,01 мМ, максимальным - 10,00 мМ. Чувствительность разработанных биосенсоров составляет от 20 до 30 мА/М·см2, погрешность измерения концентрации аналита - от 2,0 до 5,0 %, воспроизводимость сигнала - от 2,0 до 2,5 %.
* Работа выполнена в рамках федеральной целевой программы «Исследования и разработки по приоритетным направлениям развития научно-технологического комплекса России на 2007-2013 годы» (государственный контракт №16.512.11.2220).
Сведения о рецензентах:
- Остроумов Л. А., д. т. н., профессор по кафедре «Технология молока и молочных продуктов» ФГБОУ ВПО «Кемеровский технологический институт пищевой промышленности», г. Кемерово.
- Просеков А. Ю., д. т. н., профессор, проректор по НИР ФГБОУ ВПО «Кемеровский технологический институт пищевой промышленности», г. Кемерово.



