Основным клиническим проявлением данного заболевания являются симптомы нарушения функции нижних мочевых путей, выраженность которых варьирует в широких пределах. Наибольшее беспокойство пациентам доставляют так называемые ирритативные расстройства мочеиспускания, обусловленные структурными и функциональными изменениями детрузора на фоне прогрессирующей инфравезикальной обструкции, и представленные учащенным мочеиспусканием, императивными позывами к нему, ноктурией и недержанием мочи. Большинство из этих симптомов не представляют непосредственной угрозы для жизни больных, однако могут оказывать значительное влияние на её качество, грубо нарушать структуру сна, профессиональную и социальную активность пациентов [2].
В настоящее время тактика ведения больных ДГПЖ претерпела существенные изменения благодаря активному развитию фармакотерапии, но наиболее радикальным и эффективным методом лечения по-прежнему остается хирургический. На сегодняшний день среди всех предложенных вариантов оперативного лечения ДГПЖ «золотым стандартом» считается ее трансуретральная резекция - ТУР ДГПЖ. У большинства пациентов операция со временем приводит к полной ликвидации или существенному уменьшению расстройств мочеиспускания, однако почти у половины больных дисфункция мочевого пузыря, несмотря на ликвидацию инфравезикальной обструкции, сохраняется в первые месяцы после операции, а у 10-20% больных ирритативные и обструктивные симптомы сохраняются даже через полгода после оперативного лечения [3].
Неудовлетворительные результаты оперативного лечения большинство авторов связывают с морфофункциональными изменениями мочевого пузыря, возникающими на фоне циркуляторной гипоксии детрузора [4; 5]. Исходя из этого, можно предположить, что использование гипербарической оксигенации (ГБО) в комплексном лечении больных, перенесших ТУР ДГПЖ, будет положительно влиять на гемодинамику детрузора, приводя тем самым к уменьшению выраженности симптомов нарушения функции нижних мочевых путей и улучшению качества жизни пациентов.
Цель исследования. Целью исследования является улучшение течения послеоперационного периода и качества жизни пациентов, перенесших ТУР ДГПЖ.
Материалы и методы. Основу исследования составили 82 больных, которым была выполнена ТУР ДГПЖ. Пациенты были разделены на две группы. В исследуемой группе (n-40) в послеоперационном периоде, после восстановления самостоятельного мочеиспускания, проводилась терапия альфа-адреноблокаторами в сочетании с гипербарической оксигеацией (10 сеансов с экспозицией 45 мин., под давлением 1,5 АТА, в камере БЛКС-301М); группу контроля (n-42) составили пациенты, получавшие только альфа-адреноблокаторы.
Оценка параметров мочеиспускания осуществлялась по данным модифицированного опросника IPSS и QoL непосредственно перед началом и после окончания курса терапии. На протяжении всего курса лечения пациенты вели дневник мочеиспускания, по которому вычислялось среднее количество дневных и ночных микций. По данным урофлоуметрии, проводимой на 4-е и 14-е сутки после восстановления самостоятельного мочеиспускания, вычисляли максимальную объемную скорость потока мочи (Qmax) и эффективный объем мочеиспускания. Одновременно с урофлоуметрией 29 пациентам исследуемой группы и 22 - контрольной выполнена цистоманометрия наполнения с использованием аппарата Duet Logic Medtronic.
У 26 больных исследуемой группы и 22 больных контрольной, проводилась ультразвуковая доплерография сосудов стенки мочевого пузыря трансректальным датчиком на аппарате Toshiba Xario SSA-660A. При этом изучались следующие показатели: систолическая скорость кровотока, диастолическая скорость кровотока и индекс резистентности. Указанные параметры оценивались дважды - непосредственно перед началом курса ГБО-терапии и после его завершения в исследуемой группе и до начала стандартной терапии послеоперационного периода и после ее окончания в контрольной группе.
Материалом для морфологического исследования послужили 10 результатов биопсии стенки мочевого пузыря, выполненной во время ТУР ДГПЖ, включавшей мышечный слой, а также аналогичные образцы ткани, полученные в результате цистоскопии с биопсией, проведенной у 5 пациентов по окончании курса ГБО и у 5 пациентов по окончании курса стандартной терапии. 23 пациентам исследуемой и 21 пациенту контрольной групп проведено обследование через 6 месяцев после оперативного лечения, включавшее в себя анкетирование по шкале IPSS, QoL, заполнение дневника мочеиспусканий в течение 3-х суток и урофлоуметрию.
Результаты. В исследуемой группе через 14 дней после восстановления самостоятельного мочеиспускания (после 10 сеансов ГБО) суммарный бал по шкале IPSS снизился с 16,35±1,24 до 10,39±0,76, в контрольной группе - с 17,24±1,12 до 13,56±0,91. Показатель QoL снизился в основной группе с 4,2±0,71 до 2,12±0,32, в контрольной - с 4,09±0,32 до 3,2±0,6. Qmax в основной группе выросла с 13,6±1,15 мл/с до 18,7±2,1 мл/с, и в контрольной группе - с 14,1±1,89 мл/с до 16,2±1,72 мл/с.
Эффективный объем мочеиспускания достоверно возрос с 122,36±8,2 мл до 179,26±10,1 мл в исследуемой группе и с 119,25±16,9 мл до 159,31±18,36 мл в контрольной. Снизилось число дневных (с 10,22±0,4 до 7,32±0,42 раза в исследуемой группе и с 9,83±0,12 до 8,8±0,91 в контрольной) и ночных мочеиспусканий (с 3,21±0,24 до 1,52±0,2 раза в исследуемой и с 3,5±0,6 до 2,1±0,8 в контрольной группе). Объем остаточной мочи снизился в среднем с 93,23±5,8 мл до 42,13±4,61 мл в исследуемой группе и с 86,8±53,52 мл до 19,23±4,21 мл в контрольной (рис. 1).
*После лечения без ГБО/после лечения с ГБО Р<0,05.
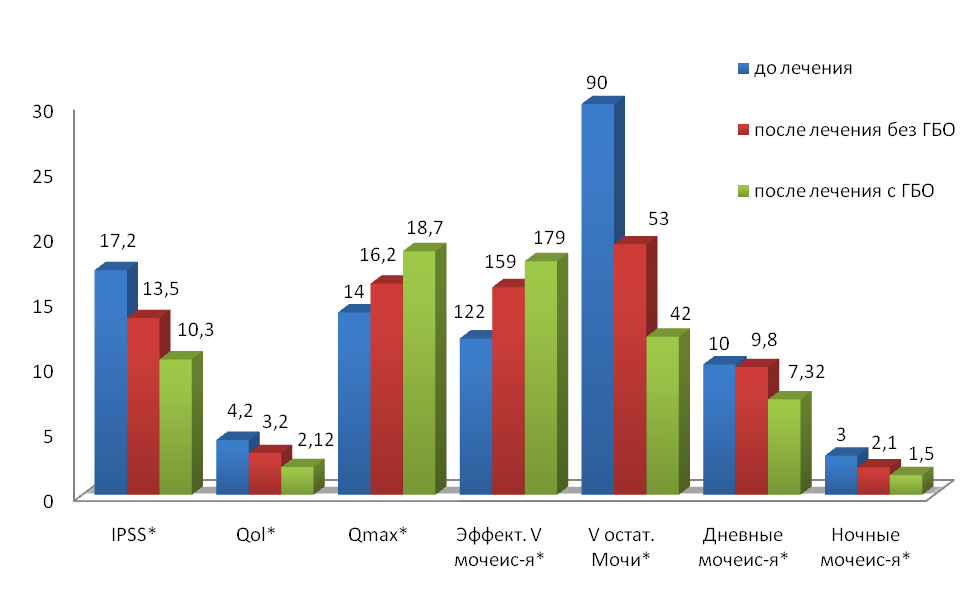
Рис. 1. Показатели функции нижних мочевых путей пациентов, перенесших ТУР ДГПЖ в контрольной и исследуемой группах до и после проведенного лечения.
Вышеуказанные показатели, оцененные через 6 месяцев после оперативного лечения, составили: суммарный бал по шкале IPSS 6,3±1,08 и 7,5±1,34, QoL - 1,5±0,27 и 2,2±0,5, Qmax 19,7±2,1 мл/с и 17,2±1,6 мл/с, эффективный объем мочеиспускания 201±8,46 мл и 178±14,3 мл, объем остаточной мочи 40,1±3,62 и 32,2±5,41 мл, частота дневных микций 6,1±0,82 и 7,3±0,71, ночных мочеиспусканий 0,7±0,26 и 1,1±0,48 в исследуемой и контрольной группе соответственно. Таким образом, в обеих группах отмечено дальнейшее улучшение показателей мочеиспускания, причем в исследуемой группе в большей степени (рис. 2).
*после лечения без ГБО/после лечения с ГБО Р<0,05
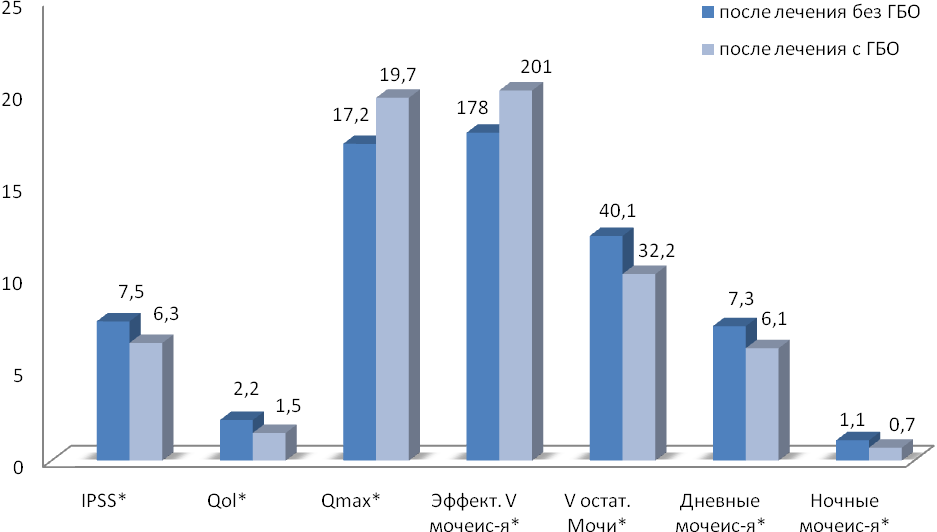
Рис. 2. Показатели функции нижних мочевых путей пациентов, перенесших ТУР ДГПЖ в контрольной и исследуемой группах через 6 месяцев после проведенного лечения.
По результатам доплерографии сосудов мочевого пузыря отмечено значимое увеличение кровотока в исследуемой группе на фоне проводимой терапии, в контрольной группе прирост аналогичных показателей был менее значимым (табл. 1).
Таблица 1 - Динамика показателей кровотока по данным доплерографии сосудов мочевого пузыря в исследуемой и контрольной группах
|
|
До лечения* |
После лечения** |
||
|
Исследуемая группа |
Контрольная группа |
Исследуемая группа |
Контрольная группа |
|
|
Систолическая скорость кровотока (см/с) |
10,26±2,12• |
11,35±1,89• |
8,12±1,74• * |
11,86±2,13• |
|
Диастолическая скорость кровотока (см/с) |
1,85±0,85• |
1,70±1,12• |
2,27±0,93 * |
1,90±0,78• |
|
Индекс резистентности |
0,82±0,02• |
0,85±0,03• |
0,72±0,03• * |
0,084±0,02• |
* до лечения исследуемая группа/контрольная группа P>0,05;
** после лечения исследуемая группа/контрольная группа P<0,05.
По результатам цистоманометрии в исследуемой группе показано достоверное увеличение объема мочевого пузыря при его наполнении как на момент первого позыва на мочеиспускания, так и при ургентном позыве. В группе контроля аналогичные показатели изменились в меньшей степени (табл. 2).
Таблица 2 - Динамика результатов цистоманометрии в исследуемой и контрольной группах
|
|
До лечения* |
После лечения** |
||
|
Исследуемая группа |
Контрольная группа |
Исследуемая группа |
Контрольная группа |
|
|
Объем мочевого пузыря в момент первого позыва (мл) |
115±7,2 |
121±11,2 |
144±6,3 |
132±5,5 |
|
Давление в мочевом пузыре в момент первого позыва (см вод. ст.) |
16±1,3 |
14±0,76 |
17±0,9 |
14±1,1 |
|
Объем мочевого пузыря в момент ургентного позыва (мл) |
202±17,6 |
198±12,4 |
254±21,1 |
224±12,8 |
|
Давление в мочевом пузыре в момент ургентного позыва (см вод. ст.) |
22±1,7 |
23±2,1 |
25,6±2.3 |
23,1±2,1 |
* до лечения исследуемая группа/контрольная группа P>0,05;
** после лечения исследуемая группа/контрольная группа P<0,05.
По результатам морфологического исследования у пациентов исследуемой и контрольной группы обнаруживались в целом однотипные изменения в виде нарушения кровообращения в стенке мочевого пузыря (выраженный склероз и гиалиноз артерий и артериол, гиперемия венозной сосудистой системы), атрофия, гипертонус миоцитов мышечной оболочки, склеротические изменения всех оболочек мочевого пузыря. После проведенного лечения в контрольной группе отмечались следующие изменения: уменьшение венозной гиперемии, расширение артериальной сети и улучшение гемомикроциркуляции.
У пациентов исследуемой группы после проведения сеансов ГБО признаки восстановления кровообращения в стенке мочевого пузыря были более выражены по сравнению с группой контроля, кроме того, уменьшался тонус миоцитов средней сосудистой оболочки и снижался уровень склероза стенки мочевого пузыря и артериальных сосудов.
Обсуждение. Гипоксия детрузора при доброкачественной гиперплазии предстательной железы может быть как следствием инфравезикальной обструкции [6], за счет развития относительной недостаточности кровообращения в гипертрофированной стенке мочевого пузыря и сдавления аденоматозными узлами нижнепузырных артерий, так и возникать в результате возрастного снижения кровоснабжения мочевого пузыря из-за атеросклеротического поражения артерий («сенильный детрузор») [4]. Гипоксия запускает сложный каскад реакций, который через холинергическую денервацию [7] детрузора ведет к развитию гиперактивности мочевого пузыря, что, в конечном счете, проявляется ирритативными симптомами.
В основе терапевтического воздействия ГБО лежит значительное увеличение кислородной емкости жидких сред организма (кровь, лимфа, тканевая жидкость и др.), составляющих до 70% массы тела. При этом они становятся мощными переносчиками кислорода к клеткам и создаются возможности для депонирования части кислорода в тканях. ГБО компенсирует практически любую форму кислородной недостаточности, и прежде всего гипоксию, существенно удлиняет радиус эффективной диффузии кислорода в ткани, обеспечивает метаболические потребности тканей, создает определенный резерв кислорода в организме. Кроме того, ГБО усиливает доставку кислорода не только в пораженные, но и в относительно интактные ткани или органы целостного организма, действует на все без исключения органы, ткани, клетки и субклеточные структуры, тем самым воздействуя на различные уровни адаптации организма, начиная с нейроэндокринного и кончая субклеточным [8].
Гипербарическая оксигенация обладает также противоспалительным действием - снимает отек, способствуя тем самым полноценной регенерации тканей [9].
Полученные результаты укладываются в представление о ведущей роли гипоксии в развитии ирритативных расстройств мочеиспускания и оправдывают применение гипербарической оксигенации в комплексе лечебных мероприятий у больных, перенесших ТУР ДГПЖ.
Следует отметить, однако, что ГБО, улучшая обмен веществ, не влияет на скорость удаления продуктов метаболизма из тканей, поэтому данный метод лучше использовать в сочетании с препаратами, улучшающими местное кровообращение. В данном случае комбинация ГБО и альфа-адреноблокаторов представляется наиболее целесообразной [5].
Заключение. Таким образом, включение гипербарической оксигенации в комплекс лечебных мероприятий после ТУР ДГПЖ позволяет существенно уменьшить выраженность расстройств мочеиспускания в ранние сроки после оперативного лечения. Кроме того, данный метод позволяет улучшить и отдаленный результат операции как в отношении ирритативной симптоматики, так и в отношении симптомов опорожнения мочевого пузыря. Все это диктует необходимость более разностороннего подхода к лечению расстройств мочеиспускания у пациентов, перенесших трансуретральную резекцию предстательной железы. При этом перспективным для решения остается вопрос об определении четких критериев отбора пациентов для того или иного направлении комплексного реабилитационного лечения после перенесенной операции.
Рецензенты
- Костюченко К.В., д.м.н., зам. главного врача ГБКУЗ МЧС ОАО «Автодизель», г. Ярославль.
- Гужков О.Н., д.м.н., зав. операционным отделением ГУЗ ЯО «Клиническая больница № 9», г. Ярославль.



