Гибернотерапия позволила улучшить эффективность ургентной терапии и достичь значительного удлинения времени сохранения обратимых изменений нервной системы при тотальной ишемии и нейротравме. Позднее благодаря работам Неговского В.А., Бакулева А.Н., Мешалкина Е.Н., Букова В.А. и мн. других крупных ученых методики управляемого понижения температуры тела стали успешно применяться в реаниматологии, кардио- и нейрохирургии, при черепно-мозговой травме [2]. Было установлено, что потребление кислорода мозгом при температуре тела +28 °С понижается на 50% и на 80% - при +25 °С [5]. Однако понижение температуры тела ниже +32 °С обуславливает кардиоваскулярную депрессию, развитие блокад, фибрилляцию и асистолию. Проградиентно нарастают электролитные нарушения и расстройства кислотно-основного состояния, подавление функции почек и печени. Увеличивается число гнойно-септических осложнений. Период увлечения гибернотерапией в западной медицине завершился в 70-х годах прошлого столетия в связи с большим числом тяжелых осложнений и побочных эффектов общей гипотермии.
В СССР управляемую гипотермию вполне успешно применяли в кардиохирургии и при черепно-мозговой травме до конца 80-х годов ХХ века [2]. Позднее единственным центром гипотермии оставался НИИ патологии кровообращения им. Е.Н. Мешалкина.
Первое десятилетие ХХI века справедливо можно назвать периодом ренессанса терапевтической гипотермии (ТГ), а причиной возвращения ТГ в клиническую практику является признание факта того, что до настоящего времени не созданы достаточно эффективные средства и методы нейропротекции.
Показано, что гипотермия мозга способствует торможению выброса глутамата, процессирования и взаимодействия сигнальных молекул, апоптоза, снижению оксидантного стресса, лежащих в основе эффектов эксайтотоксичности. Снижается внутричерепное давление (ВЧД), уменьшается объем повреждения аксонов, улучшается пиальная микроциркуляция [6-8]. Иначе говоря, понижение температуры мозга способно ограничить развитие всех основных патогенетических механизмов повреждения нейронов при ишемии, реперфузии и нейротравме.
В «Методических рекомендациях по проведению реанимационных мероприятий Европейского совета по реанимации» (пересмотр 2010 г.) подчеркнуто, что «...гипотермия обладает нейропротекторным действием и улучшает исходы после периода глобальной гипоксии-ишемии...». Метод общей ТГ определен в Рекомендательном протоколе по ведению больных с гипертензивными внутримозговыми гематомами (V Съезд нейрохирургов, 2009) как необходимый компонент лечения. Общая ТГ выделена в качестве важной составляющей сердечно-легочной реанимации в Рекомендациях Американской ассоциации кардиологов (American Heart Association - 2010).
Отечественные, Европейские и Американские Рекомендации подразумевают индукцию мягкой общей ТГ, то есть понижение базальной температуры тела пациентов в наименее опасных пределах и не ниже +32 °С.
Более 30 лет назад в СССР были разработаны и успешно применялись аппараты «Холод-2Ф» и «Флюидкраниотерм», позволяющие индуцировать локальную краниоцеребральную гипотермию (КЦГ) путем охлаждения поверхности волосистой части головы. Отечественный опыт применения КЦГ продемонстрировал высокую эффективность данной методики. Тем не менее большинство специалистов отдают предпочтения общей ТГ, и это связано с распространенным мнением о том, что понизить температуру в объеме головного мозга можно только при общей ТГ.
Известно, что при средней температуре около +37 °С головной мозг в норме термогетерогенен, а градиент температур между участками коры может достигать 1 °С [4]. В области травмы и асфиксии коры мозга температура нейронов повышается на 1,5 °С и выше, что усугубляет повреждение нейронов. Развитие отека и угнетение кровообращения в области поражения понижает эффективность теплоотведения с током крови. В этих условиях индукция гипотермии мозга охлажденной кровью может оказаться недостаточной. Прямые измерения температуры мозга и неинвазивная радиотермометрия при КЦГ показали снижение температуры коры при транскраниальном охлаждении. При индукции КЦГ ориентируются на температуру в наружном слуховом проходе, рассматривая её как достаточно точный коррелят температуры височных отделов коры.
Учитывая отсутствие осложнений, свойственных общей ТГ, нами было предпринято исследование КЦГ при церебральных катастрофах.
Материал и методы исследования. Исследования проведены на базе отделения острых нарушений мозгового кровообращения больницы № 1 УДП (Волынская б-ца). Для КЦГ использовали отечественный аппарат «АТГ-01» (рис. 1) при длительном поддержании температуры области скальпа на уровне +3±2 °С. Охлаждение головы осуществляли с помощью специальных шлемов. Мониторировали температуру в области теплоотведения, наружном слуховом проходе, регистрировали базальную температуру. Длительность процедуры КЦГ составила от 4 до 24 часов. КЦГ индуцировали 25 пациентам в острейшем периоде ишемического инсульта. Критерием включения являлся ишемический инсульт, подтвержденный методом нейровизуализации, сроком не более 72 часов.

Рис. 1. Аппарат терапевтической гипотермии в отделении острых нарушений мозгового кровообращения больницы № 1 УДП.
Средний возраст пациентов составил 70,6 лет. 11 пациентов с ишемическим инсультом в бассейне правой средней мозговой артерии, 9 пациентов - в бассейне левой средней мозговой артерии и 4 пациента с ишемическим инсультом в бассейне вертебро-базилярной артериальной системы.
Критерием исключения являлась брадикардия (ЧСС ниже 50 уд/мин). Проводили оценку неврологического дефицита по шкале NIHSS[1]. Все пациенты получали стандартную терапию. Оценивали параметры мозгового кровотока методом транскраниальной доплерографии (ТКД) на аппарате «Ангиодин-ПК». Рассчитывали уровень внутричерепного давления (ВЧД) по формуле (Klingelhofer J.).
Результаты. Все пациенты находились в сознании и удовлетворительно переносили процедуры КЦГ. Исходный уровень дефицита по NIHSS составил 11,3±0,26 балла.
КЦГ приводила к выраженному регрессу неврологического дефицита и снижению по NIHSS до 6,8±0,1 (p<0,01, 39,82%). Кроме того, анализировали результаты в зависимости от давности развития инсульта: до 48 часов (20 пациентов) и 48-72 часа (5 пациентов). В первой группе исходно NIHSS составил 11,1±0,12, уменьшившись после КЦГ до 5,8±0,98 балла (p<0,01, 47,7%), тогда как во второй группе динамика была недостоверной - от 11,7±1,4 в исходе до 10,3±2,75 после КЦГ (р>0,1, 12%, рис. 2).
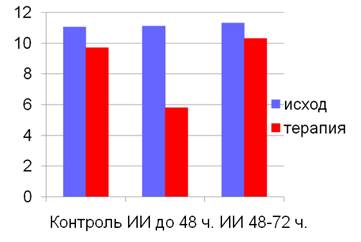
Рис. 2. Динамика изменений неврологического дефицита под влиянием КЦГ.
Методом ТКД были выявлены значительные изменения мозгового кровотока - увеличение пиковой систолической скорости на 69% (23,88±9,1 см/сек) и средней скорости кровотока на 59% (14,06±4,1 см/сек) в заинтересованном полушарии. Среднее снижение ВЧД составило 31%. Показатели системного артериального давления при КЦГ практически не изменялись.
В контрольную группу были включены 10 пациентов, не получавшие КЦГ, с областями локализации ишемического очага и объемом неврологического дефицита (11,4±0,41 балла по NIHSS) такими же, как и в основных группах. Изменения неврологического статуса и мозгового кровотока фиксировали при поступлении и через 24 часа. Статистически значимого изменения неврологического статуса и мозгового кровотока в контрольной группе отмечено не было. У пациентов с исходно нормальной базальной температурой температура в слуховом проходе спустя 4 часа от начала охлаждения понижалась до +35-33 °С, при 12-часовых процедурах - до +30 °С, удерживаясь на этом уровне. Процедуры более 12 часов обеспечивали развитие мягкой ОТГ (~ +36 °С) без мышечной дрожи. Средний градиент базальной температуры и температуры в слуховом проходе составлял 2,6 °С. У 12 пациентов развилась лихорадка с температурой тела +38-40 °С (аурикулярная выше на 0,5-1 °С). КЦГ позволяла купировать пиретические состояния и достичь обратного градиента температуры (аурикулярная температура ниже базальной на 2-3 °С).
Клинический пример. Пациент - мужчина, 55 лет. Диагноз: ишемический инсульт в бассейне правой средней мозговой артерии по кардиоэмболическому типу. Отёк головного мозга. Вторичный дислокационный синдром. Гипертоническая болезнь III ст., риск высокий. ИБС. Постоянная форма мерцательной аритмии, тахисистолический вариант. ТЭЛА. Тромбоз задних большеберцовых вен левой голени. Двусторонняя нижнедолевая пневмония. ИВЛ. Состояние при поступлении (первые сутки от дебюта) тяжелое, уровень сознания: оглушение. Неврологический дефицит: установка взора вправо, сглаженная левая носогубная складка, грубая дизартрия, язык девиирует влево, левосторонняя гемиплегия, патологические стопные знаки слева, NIHSS 22. Исходная базальная температура +39,2 °С, исходная температура в слуховом проходе +39,7 °С.
На фоне проводимого лечения, а также процедуры КЦГ отмечалось нарастание уровня бодрствования, мышечной силы в правых конечностях, уменьшение степени выраженности дизартрии, по NIHSS - 11 баллов. По данным доплерографии: улучшение кровотока в заинтересованном полушарии. На момент поступления кровоток в правой СМА не визуализируется, к 3-му часу процедуры отмечается появление минимального кровотока, через 8 часов пиковая систолическая скорость кровотока - 40 см/сек. Базальная температура после проведения КЦГ +37,2 °С, аурикулярная +34,1 °С.
У двух пациентов проводили неинвазивную радиотермометрию коры головного мозга с помощью специального радиотермометра РТМ-01. В области ишемического поражения мозга температура достигала +39,6 °С, при этом базальная температура оставалась на уровне субфебрильных значений. Средняя температура коры больших полушарий (18 точек измерения) составила +38,3±0,03 °С. КЦГ через 4 часа обеспечила снижение температуры коры мозга до +36,2±0,01 °С (Δt - 2,1 °С).
Обсуждение. Полученный материал даёт основания заключить, что КЦГ позволяет достичь позитивных клинических результатов у больных с ишемическим инсультом. Развивающийся регресс неврологического дефицита, по-видимому, является следствием уменьшения отека мозга, снижения ВЧД, что влечет за собой улучшение кровотока в магистральных сосудах заинтересованного полушария, косвенно свидетельствуя об улучшении кровоснабжения области «полутени». Данные изменения температуры в слуховом проходе и коры больших полушарий позволяют продемонстрировать успешную индукцию гипотермии мозга. Безусловно, представленные данные требуют дальнейшего уточнения. В первую очередь это касается выяснения возможностей понижения температуры различных отделов головного мозга при использовании КЦГ разной интенсивности и длительности. Кроме того, необходимо оценить особенности влияния КЦГ на церебральный кровоток и метаболизм, без чего невозможно доказательно обсуждать механизмы снижения ВЧД, степень и характер влияния методики на основные механизмы повреждения нейронов при ишемии.
Методика КЦГ выгодно отличается от известных методик воспроизведения общей гипотермии, не требует седации и дополнительной коррекции терморегуляции, очень проста в исполнении и не вызывает развития общей гипотермии ниже +35 °С. По указанным параметрам КЦГ вполне отвечает отечественным и зарубежным рекомендациям по использованию ТГ. КЦГ оказывается эффективной в коррекции пиретических состояний, которые существенно отягчают течение ишемического инсульта.
В наших исследованиях не отмечено каких-либо осложнений или побочных эффектов от применения КЦГ на протяжении всего периода госпитализации пациентов.
Рецензенты
- Радыш И.В., д.м.н., профессор кафедры нормальной физиологии РУДН, г. Москва.
- Демуров Е.А., д.м.н., профессор кафедры общей патологии и патологической физиологии РУДН, г. Москва.
[1] Шкала инсульта Национального института здоровья, National Institutes of Health Stroke Scale, Brott T., Adams H.P., 1989.



