Введение
Кизил мужской (Cornus mas L., сем. Кизиловые - Cornaceae) издавна известен как плодовое растение с ценными лекарственными свойствами. Листья кизила содержат: иридоиды (секологанин 0,1%), фенолкарбоновые кислоты, витамин С, дубильные вещества – до 17,6%, флавоноиды (рутин, кверцетин, кемпферол), проантоцианидины [4]. Ранее нами была разработана технология кизила листьев экстракта жидкого, представляющая собой противоточное многоступенчатое экстрагирование в батарее из шести диффузоров при соотношении фаз 1:2 с использованием в качестве экстрагента 70%-ного этилового спирта [5]. Настой из листьев кизила используется в народной медицине как антимикробное средство при желудочно-кишечных расстройствах и лечении различных ран, а также как мочегонное и противовоспалительное средство.
Целью данной работы является изучение острой токсичности, мочегонного, антимикробного действия кизила листьев экстракта жидкого.
Материал и методика. В качестве объекта исследования использовали жидкий экстракт листьев кизила 1:2 (экстрагент 70%-ный этиловый спирт, показатели качества экстракта: содержание флавоноидов, в пересчете на рутин, 0,52±0,01%; плотность экстракта 0,922 г/см3; сухой остаток - 8,02±0,28%; содержание спирта этилового в экстракте не менее 64%) [5].
Диуретическое действие [6] кизила листьев экстракта жидкого изучалось на белых крысах мужского пола линии Wistar массой 200-240 г. Животные содержались на обычном рационе в стандартных условиях вивария. В день, предшествующий эксперименту, крысы не получали пищу и воду. Использовались три группы крыс по 6 в каждой группе. Первая группа была контрольной и получала воду очищенную. Исследуемый экстракт и препарат сравнения (леспефрил) вводили перорально крысам второй и третьей групп соответственно. Вводимый объём составлял 1 мл. Затем производили водную нагрузку (из расчета 25 мл на 1 кг веса через желудочный зонд). После введения вещества животных помещали в клетки для изучения общего обмена и в течение 4 ч проводили учёт диуреза. Острую токсичность кизила экстракта жидкого определяли по методу Кербера [3]. Условия проведения опыта соответствовали рекомендациям Фармакологического комитета [6; 7]. Испытания проводили на интактных мышах обоего пола массой 19,0-21,0 г. Экстракт вводили животным непосредственно в желудок с помощью зонда с оливой на конце. Кизила листьев экстракт жидкий вводили в возрастающих дозах. В качестве контроля использовали спирт этиловый 64%-ный. Расчеты LD50 проводили по формуле: ![]() ; где LD100 - доза, вызывающая гибель всех животных, мл/кг; z - показатель разницы между количеством погибших животных при использовании двух соседних доз; d - интервал между каждыми двумя смежными дозами, мл/кг; m - число животных в каждой группе (m=6).
; где LD100 - доза, вызывающая гибель всех животных, мл/кг; z - показатель разницы между количеством погибших животных при использовании двух соседних доз; d - интервал между каждыми двумя смежными дозами, мл/кг; m - число животных в каждой группе (m=6).
Для определения острой токсичности самого комплекса биологически активных веществ (БАВ) кизила листьев экстракта жидкого, спирт этиловый из экстракта отгоняли под вакуумом и комплекс БАВ досушивали в вакуум-сушильном шкафу при температуре не выше 40 °С. В предварительном эксперименте на ограниченном количестве животных определяли ориентировочный диапазон доз, вызывающий гибель животных. Он находился в интервале от 5000 до 10000 мг/кг массы. В заключительном эксперименте нами были изучены дозы с шагом 1000 мг/кг. Белым мышам массой 18-20 г внутрь, через зонд, вводили по 0,5 мл водного раствора БАВ (1:10) повторно с интервалом в 3 часа. На каждую дозу брали по 6 животных. За животными наблюдали в течение 14 дней. Регистрировали их внешний вид, поведение и явления, при которых происходила их гибель.
В настоящее время промышленностью выпускается настойка зверобоя, которая применяется внутрь и наружно как антимикробное средство. Поэтому антимикробное действие кизила экстракта жидкого изучали в сравнении с настойкой зверобоя и спиртом этиловым 64%-ным. Для культивирования микроорганизмов использовали питательные среды (ПС), рекомендованные Государственной фармакопеей [2]. ПС № 1 – для Bacillus anthraxoides; № 2 – для Candida albicans, Aspergillus niger; № 3 – для бактерий семейства Enterobacteriaceae (Salmonella typhimurium, Shigella flexneri 266); № 8 - для Pseudomonas aeruginosa, Staphylococcus aureus, Bacillus subtilis L2.
Для выяснения активности исследуемые препараты (экстракт кизила жидкий, настойка зверобоя, спирт этиловый 64%-ный) разводили в фосфатном буферном растворе (ФБР) в соотношении 1:1, 1:5, 1:10. Определение антимикробной активности экстракта кизила мужского проводили методом диффузии в агар (способ «колодцев»). Метод основан на оценке угнетения роста тест-микроорганизма определёнными концентрациями испытуемого средства [2]. Для проверки антимикробной активности использовали 24-часовые тест-культуры, выращенные на соответствующих питательных средах, рекомендованных Государственной фармакопеей [2],: № 1 – для Bacillus anthraxoides; № 2 – для Candida albicans, Aspergillus niger; № 3 – для бактерий семейства Enterobacteriaceae (Salmonella typhimurium, Shigella flexneri 266); № 8 - для Pseudomonas aeruginosa и Staphylococcus aureus, Bacillus subtilis L2). Микробные культуры с питательных сред смывали фосфатным буферным раствором и готовили взвесь, содержащую 500 млн микробных тел в 1 мл по стандарту мутности. Разведение Aspergillus niger проводили в фосфатном буферном растворе с добавлением твина-80. На поверхность питательных сред в чашках Петри одинакового диаметра проводили посев сплошным газоном стандартных взвесей используемых тест-культур. Для этого 2 мл взвеси помещали в чашку Петри, взвесь равномерно распределяли по поверхности, а излишки взвеси полностью удаляли. Стерильным сверлом диаметром 6 мм делали 6 лунок («колодцев») на расстоянии 2,5 см от центра и на одинаковом расстоянии друг от друга. В три лунки через одну вносили 0,1 мл испытуемого вещества в соответствующем разведении, а в три оставшиеся лунки - растворитель в соответствующей концентрации (контроль). Под крышку чашки Петри помещали стерильный фильтр во избежание попадания конденсата на лунки. Все чашки Петри ставили в термостат строго горизонтально для получения круглых зон угнетения роста микрофлоры, инкубировали при температуре 35±2 °С в течение суток (Pseudomonas aeruginosa, Bacillus anthraxoides; Salmonella typhimurium, Shigella flexneri 266; Pseudomonas aeruginosa и Staphylococcus aureus, Bacillus subtilis L2) или в течение 4 суток (Candida albicans, Aspergillus niger) при температуре 30 ± 2 °С. После инкубации диаметр зон угнетения роста измеряли с помощью миллиметровой линейки. Оценка результатов проводилась по диаметру зон задержки роста вокруг «колодца», включая диаметр самого «колодца»: отсутствие зоны задержки роста - испытуемая культура не чувствительна к данной концентрации препарата; диаметр зоны задержки роста 10 мм - умеренная чувствительность культуры к данной концентрации препарата; диаметр зоны роста более 10 мм - высокая чувствительность испытуемой культуры к данной концентрации препарата.
Результаты и их обсуждение. Результаты определения диуретической активности экстракта листьев кизила жидкого были обработаны статистически при помощи программного пакета Microsoft Excel 2000 для независимых рядов с достоверностью р<0,05 и представлены в таблице 1 и на рисунке.
Таблица 1 - Влияние кизила листьев экстракта жидкого на диурез крыс М±m, р
|
Исследуемый объект |
Объём мочи /ед.веса/время, мл/кг/мин |
|||||
|
30´ |
45´ |
60´ |
120´ |
180´ |
240´ |
|
|
Контроль (вода очищенная) |
0,00±0,00 |
0,55±0,08 |
3,18±0,38 |
3,82±0,42 |
3,91±0,45 |
3,91±0,45 |
|
Леспефрил |
3,60±0,32* |
4,82±0,42* |
7,18±0,62* |
9,09±0,68* |
10,00±0,67* |
11,27±0,76* |
|
Кизила листьев экстракт жидкий |
0,00±0,00 |
2,27±0,22* |
6,14±0,44* |
8,73±0,62* |
8,73±0,62* |
9,10±0,83* |
Примечание: * - р<0,05 - достоверно относительно контроля
Результаты исследований, представленные в таблице 1, показывают, что через 30 минут диурез наблюдали только у животных, получавших леспефрил. К 60-й минуте объём мочи на фоне леспефрила и кизила листьев экстракта превышал контроль на 125% и 93% соответственно (рисунок 1). Через 120 минут результат изменился на 134% и 128% относительно контроля при применении леспефрила и изучаемого экстракта соответственно.
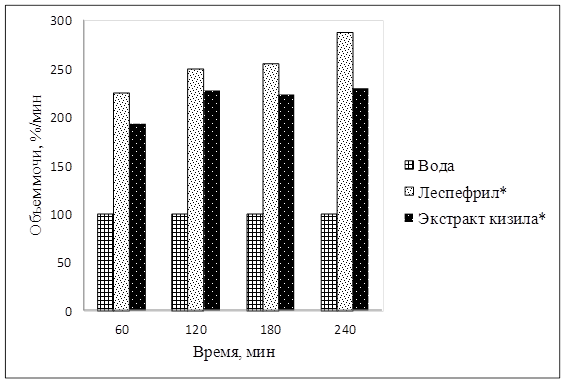
Рисунок 1 – Влияние кизила экстракта жидкого на диурез у крыс (* - р<0,05 относительно воды)
К окончанию опыта объём мочи, полученной от животных, которым вводили леспефрил, составил 11,27 ±0,76 мл, что на 188% превышало контрольные данные. На фоне экстракта из листьев кизила объём мочи составил 9,10±0,83 мл, что на 133% выше объёма мочи животных, которым вводили воду. Сравнительный анализ результатов применения кизила экстракта жидкого и леспефрила показал, что диурез на фоне леспефрила в среднем на 32% выше, чем при введении кизила листьев экстракта жидкого. Изменения количества мочи при применении кизила листьев экстракта жидкого в сравнении с результатом леспефрила носили недостоверный характер.
Результаты исследования острой токсичности спирта этилового 64%-ного и кизила листьев экстракта жидкого представлены в таблицах 2, 3.
Таблица 2 - Результаты исследования острой токсичности спирта этилового 64%-ного (m=6)
|
Дозы, мл/кг |
5 |
10 |
15 |
20 |
25 |
30 |
||||||
|
Выжило |
6 |
5 |
2 |
1 |
1 |
0 |
||||||
|
Погибло |
0 |
1 |
4 |
5 |
5 |
6 |
||||||
|
z |
|
1 |
3 |
1 |
0 |
1 |
|
|||||
|
d |
5 |
5 |
5 |
5 |
5 |
|
||||||
|
zd |
5 |
15 |
5 |
0 |
5 |
|
||||||
Для спирта этилового 64%-ного ![]()
Таблица 3 - Результаты исследования острой токсичности кизила листьев экстракта жидкого (m=6)
|
Дозы, мл/кг |
5 |
10 |
15 |
20 |
25 |
30 |
|||||
|
Выжило |
6 |
4 |
3 |
2 |
1 |
0 |
|||||
|
Погибло |
0 |
2 |
3 |
4 |
5 |
6 |
|||||
|
z |
|
2 |
1 |
1 |
1 |
1 |
|||||
|
d |
|
5 |
5 |
5 |
5 |
5 |
|||||
|
zd |
|
10 |
5 |
5 |
5 |
5 |
|||||
Для кизила листьев экстракта жидкого ![]()
Из результатов эксперимента, представленных в таблицах 2, 3, следует, что токсичность кизила экстракта жидкого связана с токсичностью 64%-ного спирта этилового. Результаты исследования острой токсичности комплекса БАВ кизила экстракта представлены в таблице 4.
Таблица 4 - Результаты исследования острой токсичности комплекса БАВ кизила экстракта (m=6)
|
Дозы, мг/кг |
5000 |
6000 |
7000 |
8000 |
9000 |
10000 |
||||||
|
Выжило |
6 |
5 |
4 |
3 |
2 |
0 |
||||||
|
Погибло |
0 |
1 |
2 |
3 |
5 |
6 |
||||||
|
z |
|
1 |
1 |
1 |
2 |
1 |
|
|||||
|
d |
|
1000 |
1000 |
1000 |
1000 |
1000 |
|
|||||
|
zd |
|
1000 |
1000 |
1000 |
2000 |
1000 |
|
|||||
Для комплекса БАВ кизила экстракта (высушенного) ![]()
Острая токсичность комплекса БАВ кизила листьев экстракта составила 9000 мг/кг массы животных. Комплекс БАВ кизила экстракта, при пероральном введении, относится к малоопасным веществам или веществам 4 класса токсичности [1] и является безопасным для человека. Безопасность кизила листьев экстракта жидкого будет зависеть от принятой дозы.
Результаты по изучению антимикробной активности кизила листьев экстракта жидкого (КЭ) и зверобоя настойки (ЗН) представлены в таблице 5.
Таблица 5 - Антимикробное действие кизила листьев экстракта жидкого и зверобоя настойки
|
Состав лунок |
Диаметр зоны задержки роста тест-культур микроорганизмов, мм (средние значения) |
||||||||||||||
|
1* |
2* |
3* |
4* |
5* |
6* |
7* |
8* |
9* |
10* |
11* |
12* |
13* |
14* |
15* |
|
|
Контроль 11 |
- |
- |
- |
- |
- |
- |
- |
- |
- |
- |
- |
- |
- |
- |
- |
|
ЗН |
14 |
12 |
12 |
11 |
15 |
12 |
19 |
15 |
15 |
10 |
12 |
13 |
8 |
7 |
7 |
|
КЭ |
20 |
20 |
20 |
22 |
22 |
18 |
24 |
20 |
20 |
18 |
18 |
18 |
20 |
21 |
22 |
|
Контроль 22 |
- |
- |
- |
- |
- |
- |
- |
- |
- |
- |
- |
- |
- |
- |
- |
|
ЗН + ФБР (1:1) |
12 |
9 |
9 |
10 |
11 |
10 |
17 |
13 |
12 |
8 |
11 |
11 |
5 |
6 |
6 |
|
КЭ + ФБР (1:1) |
15 |
15 |
15 |
16 |
17 |
13 |
20 |
17 |
17 |
12 |
14 |
15 |
15 |
16 |
17 |
|
Контроль 33 |
- |
- |
- |
- |
- |
- |
- |
- |
- |
- |
- |
- |
- |
- |
- |
|
ЗН + ФБР (1:5) |
9 |
7 |
7 |
8 |
9 |
8 |
13 |
11 |
9 |
6 |
9 |
9 |
4 |
4 |
3 |
|
КЭ + ФБР (1:5) |
11 |
12 |
11 |
12 |
13 |
11 |
16 |
12 |
13 |
10 |
11 |
13 |
11 |
12 |
14 |
|
Контроль 44 |
- |
- |
- |
- |
- |
- |
- |
- |
- |
- |
- |
- |
- |
- |
- |
|
ЗН+ ФБР (1:10) |
7 |
5 |
5 |
6 |
7 |
6 |
11 |
9 |
7 |
4 |
6 |
6 |
2 |
2 |
- |
|
КЭ +ФБР (1:10) |
11 |
12 |
11 |
12 |
13 |
11 |
16 |
12 |
13 |
10 |
11 |
13 |
11 |
12 |
14 |
Примечание: контроль 11 - спирт этиловый 64%-ный; контроль 22 - спирт этиловый 64% + ФБР (1:1); контроль 33 - спирт этиловый 70%-ный + ФБР (1:5); контроль 44 - спирт этиловый 64%-ный + ФБР (1:10); * -тест-культуры: 1) Staphylococcus aureus (209); 2) Staphylococcus aureus (Макаров); 3) Staphylococcus aureus (Type); 4) Staphylococcus epidermidis Wood-46; 5) Escherichia coli 675; 6) Escherichia coli 055;7) Escherichia paracoli; 8) Salmonella typhimurium; 9) Shigella flexneri 266; 10) Bacillus subtilis L2; 11) Bacillus anthraxoides - 96; 12) Bacillus anthraxoides -1; 13) Pseudomonas aeruginosa; 14) Candida albicans; 15) Aspergillus niger.
Результаты проведенных микробиологических исследований (таблица 5) показали, что кизила листьев экстракт жидкий в нативном виде, а также в разведениях (до 1:10) обладает высокой антимикробной активностью в отношении кокковой флоры, энтеробактерий и спорообразующих бактерий, грибов. При этом антимикробное действие изучаемого вещества зависит от концентрации: чем выше концентрация, тем выше антимикробная активность в отношении изучаемых микроорганизмов. Необходимо отметить, что кизила экстракт жидкий сильнее угнетает рост Escherichia paracoli, Staphylococcaceae, Pseudomonas aeruginosa, Candida albicans, Aspergillus niger. Сравнение антимикробной активности кизила экстракта жидкого и зверобоя настойки показало, что кизила экстракт жидкий обладает более выраженной антимикробной активностью, чем настойка зверобоя (в 1,2-4,7 раза).
Выводы. Выявлена антимикробная активность экстракта листьев кизила мужского в отношении энтеробактерий, бактерий рода Staphylococcaceae, Pseudomonas aeruginosa, Candida albicans, Aspergillus niger. Проведено сравнение антимикробной активности кизила листьев экстракта жидкого и настойки зверобоя и установлено, что кизила листьев экстракт обладает более выраженной антимикробной активностью, чем настойка зверобоя. Он может быть использован для лечения инфекционных заболеваний желудочно-кишечного тракта. Выявлено наличие мягкого диуретического эффекта у экстракта из листьев кизила в дозе 5 мл на 1 кг веса, что сопоставимо с действием леспефрила в той же дозе. Комплекс БАВ кизила экстракта, при пероральном введении, относится к малоопасным веществам или веществам 4 класса токсичности и является безопасным для человека.
Рецензенты:
Доркина Е.Г., доктор биологических наук, доцент, заведующая кафедрой биохимии и микробиологии, Пятигорский медико-фармацевтический институт, филиал ГБОУ ВПО «Волгоградский государственный медицинский университет», г. Пятигорск.
Василенко Ю.К., доктор медицинских наук, профессор, профессор кафедры биохимии и микробиологии, Пятигорский медико-фармацевтический институт, филиал ГБОУ ВПО «Волгоградский государственный медицинский университет», г. Пятигорск.



