Введение
Загрязнение воды является одной из острейших экологических проблем в мире. Более 90% сточных вод сбрасываются в открытые водоемы без предварительной очистки. В большей мере причиной тому являются сточные воды гальванических производств, содержащие целый ряд ионов металлов, пагубно воздействующих на здоровье людей и окружающую среду. Поэтому рациональное использование водных ресурсов и сохранение чистоты природных вод стало одной из актуальных проблем человечества.
В настоящее время существует большое количество способов очистки воды и водных растворов - механические, химические, электрические, физические, биологические, комбинированные и др. [1]. Например, для очистки воды от железа эффективно используется отстаивание, от меди, никеля, хрома (VI) широко применяют электрокоагуляцию, ионообменные технологии, биологическую очистку и т.д. В гальваническом производстве сточные воды содержат совокупность различных ионов металлов и недостаточно исследований по очистке воды от ионов металлов при концентрации каждого 0,5 мг/л и менее.
В данной статье представлены результаты экспериментальных исследований способов очистки воды от ионов металлов и их сравнительная оценка по степени очистки.
Методика исследований
При исследовании воду очищали от ионов следующими способами: отстаиванием, коагуляцией, электрохимическим и комбинированным.
Электрохимический способ переменным асимметричным током проводили электролизом с использованием пар нерастворимых разнородных электродов [2-4]. Электролизер выполнен из чередующихся электродов в виде пластин. Материал электродов: нержавеющая сталь 12Х18Н10Т, титановый сплав ОТ 4-0. Расстояние между электродами 12 мм. Объем заливаемой воды 1 л. В воде растворяли соли Fe(III), Ni(II), Cd(II), Cu(II) и Cr(VI) при концентрации каждого иона 0,5 мг/л. Переменный электрический ток пропускался через воду в течение 10 минут при силе тока 0,5 А и напряжении на клеммах электродов 4,1 В [5-7]. Ранее проведенные опыты показали, что максимальная степень очистки при минимальных энергозатратах достигается электрохимическим способом при этих параметрах.
Коагуляцию проводили с использованием хорошо растворимого в воде коагулянта – сернокислого железа FeSO4·7H2O. При введении в воду коагулянта происходило его растворение и электролитическая диссоциация с последующим образованием малорастворимого гидрата окиси железа (III), выпадающего в осадок в виде хлопьев и выступающего в качестве комплексообразователя. Соотношение начальных концентраций иона-комплексообразователя и удаляемого иона (СоFe2+/Coi) 2,5:1. Начальная концентрация иона-комплексообразователя 6,25 мг/л.
Отстаивание очищаемой воды проводилось в закрытых емкостях при температуре 20-25 °С и атмосферном давлении.
Комбинированный способ очистки заключался в электрохимическом воздействии, как указано выше, затем вводился коагулянт, и далее происходило отстаивание очищаемой воды.
Количественный анализ ионов, содержащихся в водном растворе после очистки, проводился на масс-спектрометре Agilent 7500 ICP -MS. Забор проб производился через 1 сутки и через 10 суток.
Степень очистки определялась по формуле, %:
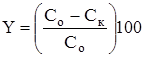 ,
,
где Со, Ск - начальная и конечная концентрации удаляемого иона металла, мг/л.
Удельные энергозатраты W определялись по формуле, (кВт·ч)/м3:
![]() ,
,
где I – сила тока, А;
U – напряжение на клеммах электродов, В;
![]() – время пропускания электрического тока, ч;
– время пропускания электрического тока, ч;
V – объем заливаемой воды, м3;
10-3 – переводной коэффициент из Вт в кВт.
Результаты исследований и их обсуждение
Результаты экспериментальных исследований влияния различных способов очистки воды на степень очистки при различном времени отстаивания представлены в таблицах 1, 2 и на рисунках 1, 2.
Таблица 1 - Результаты экспериментальных исследований влияния различных способов очистки воды на степень очистки при отстаивании воды 1 сутки
|
Ион металла |
Способ очистки |
|||
|
Отстаивание |
Коагуляция |
Электрохимический |
Комбинированный |
|
|
Степень очистки, % |
||||
|
Cd2+ |
4,3 |
14,16 |
12,07 |
46,98 |
|
Cu2+ |
16,45 |
76,91 |
34,25 |
86,17 |
|
Ni2+ |
1,98 |
6,75 |
3,31 |
28,51 |
|
Cr6+ |
2,72 |
68,13 |
7,17 |
79,86 |
|
Fe (общ.) |
31,73 |
85,05 |
13,47 |
90,7 |
Таблица 2 - Результаты экспериментальных исследований влияния различных способов очистки воды на степень очистки при отстаивании воды 10 суток
|
Ион металла |
Способ очистки |
|||
|
Отстаивание |
Коагуляция |
Электрохимический |
Комбинированный |
|
|
Степень очистки, % |
||||
|
Cd2+ |
9,19 |
23,97 |
30,91 |
73,1 |
|
Cu2+ |
88,83 |
96,05 |
87,17 |
99,14 |
|
Ni2+ |
9,59 |
12,17 |
9,33 |
37,37 |
|
Cr6+ |
7,17 |
90,7 |
19,31 |
91,41 |
|
Fe (общ.) |
87,67 |
98,59 |
90,83 |
99,71 |
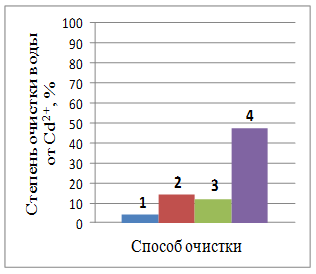
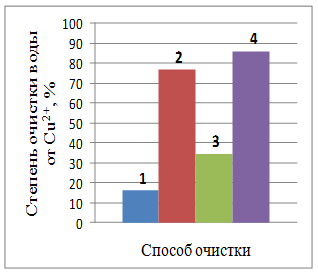
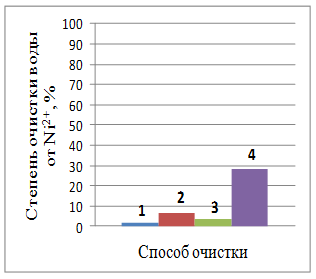
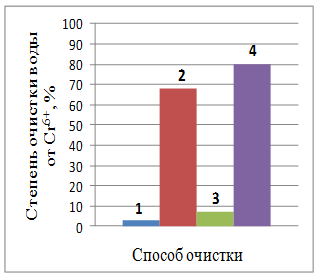
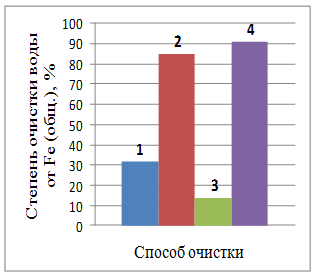
1 – отстаивание; 2 – коагуляция; 3 – электрохимический способ; 4 – комбинированный способ
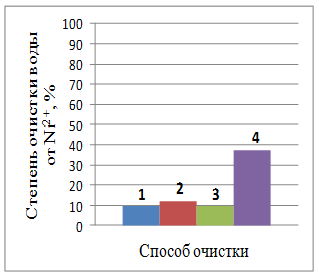
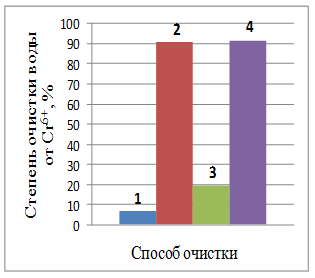
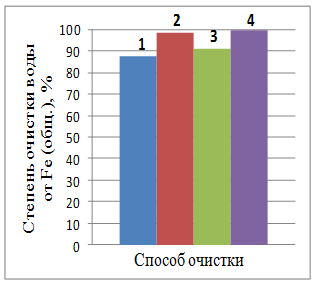
Рис. 1 – Степень очистки воды от ионов металлов при различных способах очистки (отстаивание воды 1 сутки)
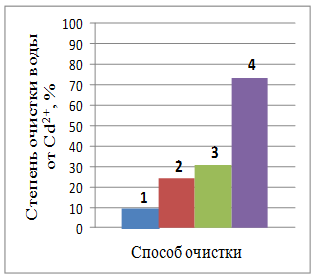
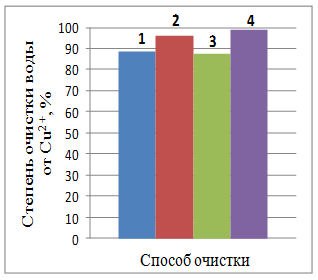
1 – отстаивание; 2 – коагуляция; 3 – электрохимический способ; 4 – комбинированный способ
Рис. 2 – Степень очистки воды от ионов металлов
при различных способах очистки (отстаивание воды 10 суток)
Из рис. 1 видно, что только отстаиванием в течение суток достичь высокой степени очистки практически невозможно (максимальная степень очистки воды при отстаивании от ионов железа YFe2+ = 31,73%, меди YCu2+ = 16,45%, кадмия YCd2+ = 4,3%, хрома YCr6+ = 2,72% и никеля YNi2+ = 1,98%).
Введение коагулянта позволяет значительно увеличить степень очистки воды от ионов хрома YCr6+ = 68,13%, меди YCu2+ = 76,91%, железа YFe2+ = 85,05% и незначительно от ионов кадмия YCd2+ = 14,16% и никеля YNi2+ = 1,98%.
Степень очистки при электрохимическом воздействии практически для всех ионов больше, чем при отстаивании, но меньше, чем при коагуляции (YCu2+ = 34,25%, YFe2+ = 13,47%, YCd2+ = 12,07%, YCr6+ = 7,17%, YNi2+ = 3,31%).
Комбинированный способ позволяет повысить степень очистки воды от всех присутствующих ионов (YFe2+ = 90,7%, YCu2+ = 86,17%, YCr6+ = 79,86%, YCd2+ = 46,98%, YNi2+ = 28,51%).
Отстаивание очищаемой воды в течение 10 суток (рис. 2) приводит к увеличению степени очистки. Наилучшие результаты по очистке воды комбинированным способом от ионов железа, меди и хрома (YFe2+ = 99,71%, YCu2+ = 99,14%, YCr6+ = 91,41%); от ионов кадмия и никеля степень очистки ниже (YCd2+ = 73,1%, YNi2+ = 37,37%).
Выводы
Экспериментальные исследования показали, что наибольшая степень очистки воды от всех рассматриваемых ионов металлов достигается комбинированным способом, заключающимся в пропускании через очищаемую воду переменного асимметричного тока с использованием нерастворимых электродов (нержавеющая сталь 12Х18Н10Т, титановый сплав ОТ 4-0), введении коагулянта - сернокислого железа FeSO4·7H2O в соотношении начальных концентраций иона-комплексообразователя и удаляемого иона 2,5:1 и отстаивании воды в течение 10 суток. При этом степень очистки воды равна: от ионов никеля 37,37%, кадмия – 73,1%, хрома – 91,41%, меди – 99,14% и железа – 99,71%. Удельные энергозатраты составляют W = 0,34 (кВт·ч)/м3. В то время как при очистке электрохимическим способом с применением нерастворимых электродов и переменного тока удельные энергозатраты составляют 1,5-2 (кВт·ч)/м3.
Рецензенты:
Петров Михаил Николаевич, д.т.н., профессор, зав. кафедрой «Электронная техника и телекоммуникации», Сибирский государственный аэрокосмический университет им. академика М.Ф. Решетнева (СибГАУ), г. Красноярск.
Смирнов Николай Анатольевич, д.т.н., профессор, зав. кафедрой «Теоретическая механика», Сибирский государственный аэрокосмический университет им. академика М.Ф. Решетнева (СибГАУ), г. Красноярск.



