Введение
На сегодняшний день иммунохроматографические тест-системы стали широко используемым средством детекции разнообразных аналитов, сфера их применения постоянно расширяется. Иммунохроматографический анализ основан на движении элюента вдоль мембраны (латеральная диффузия), которое приводит к образованию специфических иммунных комплексов на разных участках мембраны, визуализуемых как окрашенные полосы [1]. В качестве меток в данных системах используют ферменты, окрашенные латексы, но в подавляющем большинстве случаев – коллоидное золото [2, 3]. Исследуемый образец за счет капиллярных сил мигрирует вдоль тест-полоски. При наличии в пробе искомого вещества или иммунохимически близких соединений в момент прохождения образца через абсорбирующее устройство происходит взаимодействие антигена с антителами, меченными коллоидным золотом, сопровождающееся образованием комплекса антигена с антителом, который затем связывается в аналитической зоне.
Успех в создании высокочувствительной иммунохроматографической системы во многом зависит от состава мультимембранного композита и условий нанесения реагентов на мембраны тест-полоски. Несмотря на обилие существующих иммунохроматографических тестов, на сегодняшний день нет установленных рекомендаций по подбору условий, позволяющих достигать оптимальных аналитических характеристик.
Нами было исследовано влияние условий нанесения иммунореагентов на мембранные носители. Проведена оптимизация следующих параметров: 1) скорость нанесения; 2) объем нанесения; 3) pH буферных растворов, из которых проводится иммобилизация белков; 4) концентрация солей и детергентов, вносимых в рабочий буфер для нанесения; 5) концентрация наносимых белковых реагентов.
Материалы и методы
1. Реагенты
В работе использовали трис, Тритон Х-100, дигидрохлорид 3,3',5,5'-тетраметилбензидина, N-гидроксисукцинимидный эфир биотина, цитрат натрия, азид натрия, фетальную сыворотку КРС (“Sigma”, США), золотохлористоводородную кислоту (“Fluka”, Германия), диметилсульфоксид (ДМСО), Твин-20, БСА (“MP Biomedicals”, Великобритания). Все вспомогательные реагенты (соли, кислоты, щелочи, органические растворители) были аналитической или химической чистоты.
Растворы для получения коллоидного золота (КЗ) и его конъюгатов готовили на деионизированной воде (18.2 MΩ•cm при 25 ºС, система Simplicity (“Millipore”, США).
ЛПС Brucella abortus и моноклональные антитела против ЛПС производства Республиканского центра биотехнологии республики Казахстан.
Рабочие нитроцеллюлозные мембраны типов 10uCNPC-SS12, 90cnphnss40 и 150cnphnss41, и предобработанные мембраны под образец (TYPE-GBF-R7L), стекловолоконные крупнопористые мембраны для нанесения коллоидного конъюгата (CFCP203000) и адсорбирующие мембраны (CFSP223000) фирмы «MDI» (India). Также использовались рабочие нитроцеллюлозные мембраны фирмы Millipore.
2. Получение коллоидного золота (КЗ) цитратным методом [4]. К 97.5 мл деионизованной воды добавляли 1.0 мл 1 %-ного раствора HAuCl4, доводили до кипения и при перемешивании добавляли 1.5 мл 1 %-ного раствора цитрата натрия. Смесь кипятили 25 мин, затем охлаждали и хранили при 4–6 оС.
3. Просвечивающая электронная микроскопия. Препараты КЗ наносили на сеточки (300 меш., “Pelco International”, США), покрытые пленкой-подложкой из поливинилформаля, растворенного в хлороформе. Снимки получали на электронном микроскопе CX-100 (“Jeol”, Япония) при ускоряющем напряжении 80 кВ и увеличении 3.300.000. Фотографии в цифровой форме анализировали с помощью программы Image Tool.
4. Получение конъюгатов КЗ с антителами. Предварительную характеристику связывания антител с КЗ проводили согласно [5]. С этой целью к 0.1 мл растворов антител в воде (концентрацию варьировали от 5 до 250 мкг/мл) добавляли по 1.0 мл раствора КЗ (D520 = 1.0), перемешивали и инкубировали 10 мин при комнатной температуре. Затем в каждую пробу добавляли по 0.1 мл 10 %-ного NaCl, перемешивали и через 10 мин измеряли D580. Перед конъюгацией с КЗ антитела диализовали против 1000-кратного объема 10 мМ трис-HCl буфера, рН 8.5, в течение 2 ч при 4°C. К раствору КЗ (D520 = 1.0) добавляли 0.2 М К2СО3 до достижения рН 8.5 и вносили в раствор антител выбранной концентрации. Смесь инкубировали 30 мин при комнатной температуре и перемешивании, после чего вносили БСА до конечной концентрации 0.25 %. Частицы КЗ с иммобилизованными на них антителами отделяли от непровзаимодействовавших антител центрифугированием при 8000 g в течение 30 мин. После удаления супернатанта осадок ресуспендировали в фосфатно-солевом буфере (ФБС), рН 7,4, содержащем 0.25% БСА. При необходимости длительного хранения к полученному продукту добавляли азид натрия до конечной концентрации 0.02 %.
Результаты и обсуждение
В результате проведенных исследований выработан ряд рекомендаций по режимам иммобилизации реагентов на носителях:
Скорость нанесения должна находиться в пределах 5–20 мм/сек. Использование более высоких скоростей нанесения приведет к образованию неравномерного слоя нанесенного реагента, в то время как использование более низких скоростей может привести к неравномерной ширине образующейся полосы наносимого реагента.
Оптимальный объем наносимой пробы находится в диапазоне 0,1-0,2 мкл/мм. Стоит отметить, что данная величина напрямую обуславливает ширину аналитической и контрольных зон иммунохроматографической системы. Увеличение наносимого объема более 0,2 мкл/мл приводит к избыточному расходу реагента, неравномерному формированию зоны с иммобилизованным реагентом, а также к неравномерному или слабому окрашиванию зоны тест-полоски при взаимодействии с мечеными реагентами. При меньших объемах наносимых реагентов происходит прерывистое нанесение, т.к. ток жидкости (особенно при высоких скоростях нанесения) недостаточен для постоянного и равномерного выброса на мембрану.
pH буфера, из которого происходит нанесение, влияет на интенсивность, специфичность и воспроизводимость сигнала в контрольной и аналитических зонах тест-систем. Смещение в область крайних кислых или щелочных значений ведет к денатурации белковой составляющей наносимого реагента, что, в свою очередь, влечет за собой снижение активности последнего. В случае «сэндвич»-системы снижение реакционной способности антител ведет к неработоспособности аналитических наборов. Незначительная же денатурация белковой глобулы может оказать благоприятное влияние на эффективность иммобилизации. Исходя из этого, оптимальные значения pH для нанесения составляют 8–9. Данное значение обеспечивает необходимое распределение зарядов на белковой глобуле и активных групп нитроцеллюлозы рабочей мембраны для эффективного электростатического взаимодействия и высокого уровня иммобилизации целевого реагента (см. рис. 1).
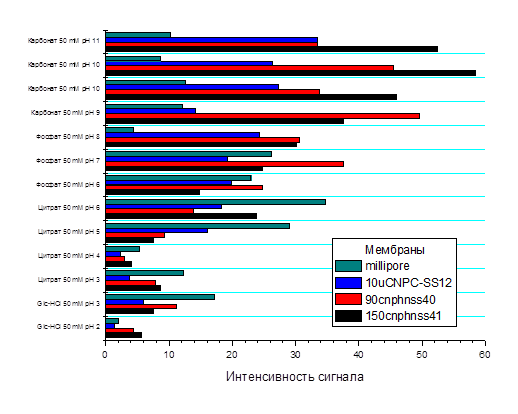
Рисунок 1. Интенсивность сигнала (яркости окраски) аналитической зоны при иммобилизации реагентов на мембране из буферов различного состава.
В состав рабочего буфера для нанесения могут быть включены различные компоненты. Проблемы могут возникнуть в результате химических взаимодействий, которые происходят в процессе испарения, когда концентрация солей становится очень высокой. Например, если используются растворы, в состав которых входят первичные амины, такие как трис или глицин, может происходить образование солевых соединений между кислыми аминокислотными остатками аминокислот белков (глутаминовой или аспарагиновой кислоты) и –NH3+ группы компонента буферного раствора, что, в свою очередь, приводит к снижению связывающей способности иммобилизуемого реагента. Помимо этого натрий в составе рабочего буфера предпочтительнее калия.
Возможно использование небольших количеств детергентов в составе рабочего буфера для обеспечения равномерности нанесения. Мембрана исходно выпускается с незначительным нанесенным количеством поверхностно активных веществ. В ходе формирования контрольной или аналитической зон при использовании свободного от детергентов рабочего буфера происходит размывание слоя ПАВ на поверхности нитроцеллюлозы, их концентрация около соответствующих зон снижается. В результате при прохождении фронта жидкости во время проведения анализа смачивание в данной области происходит медленнее, чем прилегающих районов необработанной мембраны. В результате фронт потока деформируется. В крайнем случае, поток обтекает переднюю линию нанесенного реагента с захватом пузырьков воздуха. Чтобы избежать этого, иногда эффективно добавить небольшое количество ПАВ (например, 0,05 % SDS или 0,005 % Тритон Х-100).
Тем не менее подобранные нами условия нанесения позволили избежать внесения дополнительных добавок и обеспечили равномерное формирование контрольной и аналитической зон.
Оптимальная концентрация для нанесения реагентов на рабочую нитроцеллюлозную мембрану находится в диапазоне 0,5-3 мг/мл (см. рис. 2). Внесение избыточного количества реагента приведет к увеличению несорбированных на поверхности молекул и, как следствие, к снижению аналитических характеристик производимой системы. Снижение же количества антител ниже указанного уровня в большинстве случаев недостаточно для эффективного специфического взаимодействия и формирования аналитической и контрольной зон высокой интенсивности и, как следствие, снижает чувствительность данной иммунохроматографической системы.
|
|
|||||
|
0 |
0,2 |
0,4 |
0,8 |
1,6 |
3,2 |
|
мкл/мм |
|||||
Рисунок 2. Зависимость интенсивности сигнала от количества вносимого конъюгата специфических антител с коллоидным золотом
Нанесение конъюгатов коллоидных маркеров на мембраны под конъюгат производят в соответствии с нижеприведенными требованиями.
Концентрация коллоидного маркера должна находиться в диапазоне 1–10 оптических единиц для обеспечения интенсивности аналитического сигнала на достаточном уровне. В качестве рабочего раствора используется буфер с рядом стабилизирующих добавок. Для этой цели в разрабатываемой тест-системе использовался бычий сывороточный альбумин, сочетающий высокую эффективность стабилизации коллоидных препаратов и низкую стоимость реагента. Помимо этого вносился раствор азида натрия в качестве консерванта.
Нанесение реагентов на стеклянную мембрану под конъюгат необходимо проводить при скорости движения каретки 5–20 мм в секунду и интенсивности потока 0,5–1,5 мкл на мм мембраны. Оптимальное значение составляет около 8 мкл/мм, что обеспечивает равномерную пропитку мембраны и отсутствие избытка реагента.
Все растворы, наносимые на мембраны, могут быть приготовлены заранее, при этом храниться они должны при 4 °С. После нанесения готовые мембраны хранят при комнатной температуре в течение как минимум 7–8 часов до полного высыхания и сборки мультикомпозита. Не допускается хранение готовых мембран с нанесенными реагентами при отрицательных температурах, а также нагревание, даже кратковременное, до температур выше 35 С.
Выводы
На примере тест-системы для определения ЛПС Brucella abortus определены оптимальные режимы иммобилизации реагентов на иммунохроматографические мембраны. Поскольку иммобилизуемыми реагентами являются антитела класса IgG – наиболее часто используемый компонент иммунохроматографических тестов, приведенные рекомендации носят общий характер и могут быть использованы в оптимизации тест-систем для определения широкого круга антигенов.
Работа проводилась при финансовой поддержке Министерства образования и науки Российской Федерации (Федеральная целевая программа «Исследования и разработки по приоритетным направлениям развития научно-технологического комплекса России на 2007–2013 годы», государственный контракт от 12 марта 2012 г. № 11.519.11.2046).
Рецензенты:
Сахаров Иван Юрьевич, доктор химических наук, старший научный сотрудник кафедры химической энзимологии Химического факультета Московского государственного университета им. М. В. Ломоносова, г. Москва.
Венгеров Юрий Юзефович, профессор, доктор биологических наук, ведущий научный сотрудник Института биохимии им. А. Н. Баха Российской академии наук, г. Москва.



