УДК 616.132.2-092.9
ОСОБЕННОСТИ СТРУКТУРНЫХ ИЗМЕНЕНИЙ ГОЛОВНОГО МОЗГА ПРИ МОДЕЛИРОВАНИИ АЛИМЕНТАРНОГО ДЕФИЦИТА МАГНИЯ
Смирнов А. В., Снигур Г. Л., Шмидт М. В., Гуров Д. Ю., Евсюков О. Ю.,
Медников Д. С., Спасов А. А., Харитонова М. В.
ГБОУ ВПО «Волгоградский государственный медицинский университет» Минздрава России Волгоград, Россия (400131, Волгоград, пл. Павших Борцов, 1), e-mail: [email protected]
В статье представлены результаты качественного и количественного изучения структурных преобразований различных отделов головного мозга крыс при моделировании алиментарного дефицита магния. Отмечено, что изменения экспрессии белков TRPM7, TRPM6, а также индуцибельной и эндотелиальной нитрооксидсинтазы в нейронах и нейропиле гипоталамуса, гиппокампа, коры полушарий большого мозга в условиях дефицита магния 8 и 12 недель свидетельствуют о преобладании процессов альтерации над процессами компенсаторно-приспособительного характера. Атрофические изменения нейросекреторных клеток крупноклеточных ядер гипоталамуса сочетаются с признаками их обратимого повреждения, установленными при дефиците магния 8 и 12 недель на разных уровнях патоморфологического исследования, развивающимися на фоне преобразования капилляров и нарушений кровообращения.
Ключевые слова: магний, дефицит, головной мозг, структура, изменения, моделирование.
FEATURES OF STRUCTURAL CHANGES THE BRAIN IN MODELING
ALIMENTARY MAGNESIUM DEFICIENCY
Smirnov A. V., Snigur G. L., Shmidt M. V., Gurov D. Y., Evsyukov O. Y., Mednikov D. S., Spasov A. A., Kharitonova M. V.
Volgograd State Medical University, Volgograd, Russia (400131, Volgograd, sq. Fallen Fighters, 1), e-mail: [email protected]
In this article it was presented the results qualitative and quantitative study of the structural changes in various parts of the rat’s brain in the modeling of nutritional magnesium deficiency. It was noted that the changes expression of proteins TRPM7, TRPM6, the inducible and endothelial nitric oxide synthase in neurons and neuropil of the hypothalamus, hippocampus, cerebral cortex with magnesium deficiency 8 and 12 weeks showed the predominance an alteration to adaptive changes. Atrophic changes in the neurosecretory cells of the magnocellular nuclei of the hypothalamus combined with signs of reversible damage in deficiency of magnesium at 8 and 12 weeks at different levels of pathological studies, developing against the background to alterative changes in brain’s capillaries and blood circulation disorders.
Key words: magnesium, deficiency, brain, structure, changes, modeling.
Введение
В настоящее время активно изучается роль дефицита магния в процессах повреждения и регенерации нейронов, механизмах нейропластичности и связанных с ними процессах обучения и памяти [5], синтеза и секреции нейропептидов головного мозга [2], модуляции рецепторной активности нейронов и их микроокружения [4, 8, 9]. Однако многие аспекты структурных изменений головного мозга при дефиците магния остаются мало изученными.
Цель исследования – охарактеризовать особенности патоморфологических изменений в различных отделах головного мозга крыс в условиях алиментарного дефицита магния.
Материал и методы исследования
В работе использовали 30 половозрелых нелинейных белых крыс-самцов массой 220– 260г. Животные были разделены на 3 группы: 1 группа – контрольные животные (n=10); 2 группа – животные, находящиеся на магний-дефицитной диете в течение 8 недель (n=10); 3 группа – животные, находящиеся на магний-дефицитной диете в течение 12 недель (n=10). Животные содержались в условиях вивария, согласно правилам лабораторной практики при проведении доклинических исследований в РФ (ГОСТ З 51000.3-96 и 51000.4-96). Интактные животные (1 группа) получали полноценную магний-сбалансированную диету, содержащую 0,84г MgO (0,5г элементарного магния) на 1 кг диеты и отстоянную воду (содержание магния 20 мг/л). В другой группе дефицит магния моделировался с помощью специальной диеты, которая включала: 20 % казеина, 70 % крахмала, 0,3 % DL-метионина, 0,2 % холина битартрата, 5 % кукурузного масла, 1 % поливитаминной смеси, 3,5 % полиминеральной смеси, не содержащей магния, аналогичной по составу полиминеральной смеси AIN-76 (Biomedical, США). Скорость и глубину развития гипомагнезиемии контролировали, определяя концентрацию магния в плазме и эритроцитах крови спектрофотометрическим методом по цветной реакции с титановым желтым (Sigma, США) с измерением на спектрофотометре «СФ-26» (ЛОМО, Россия) в кювете с длиной оптического пути 1 см при длине волны 550 нм. При снижении концентрации магния ниже 1,4 ммоль/л в эритроцитах и ниже 0,7 ммоль/л в плазме считалось, что у животных развилась гипомагнезиемия средней тяжести, свидетельствующая об адекватности используемой экспериментальной модели [3]. После декапитации животных образцы головного мозга фиксировали в нейтральном забуференном 10 % формалине с дальнейшим обезвоживанием в батарее спиртов и изготовлением парафиновых срезов толщиной 5 мкм. Для проведения иммуногистохимического исследования использовались антитела к белкам TRPM7, TRPM6, эндотелиальной и индуцибельной нитрооксидсинтазе, кислому глиальному астроцитарному белку. Антигенная демаскировка проводилась высокотемпературным способом с использованием фосфатного буфера (pH=9,0). Для визуализации использовалась полимерная система EnVision (Dako, Дания), в качестве хромогена – 3,3-диаминобензидин (Dako, Дания). Электронно-микроскопическое исследование проводили по стандартному для трансмиссионной электронной микроскопии протоколу. На фронтальных срезах головного мозга и мозжечка с помощью программы «Видеотест-Морфо-4» (Россия) определяли среднюю площадь перикарионов нейронов, среднюю площадь ядер нейронов, среднюю площадь цитоплазмы перикарионов нейронов. При оценке достоверности полученных данных использовали t критерий Стьюдента для нормальных распределений.
Результаты исследования и их обсуждение
При моделировании алиментарного дефицита магния на 8–12 неделе в головном мозгу наиболее выраженные структурные изменения в виде увеличения удельного количества гиперхромных нейронов наблюдались в крупноклеточных ядрах гипоталамуса, CA1 и CA3 полях гиппокампа, моторной коре полушарий большого мозга, ретикулярной формации ствола головного мозга, грушевидных нейронах коры полушарий мозжечка.
В группах 2 и 3 при иммуногистохимическом исследовании с использованием антител к белку TRPM6 отмечалась более выраженная (степень 3 по полуколичественной шкале Allred D.C., 1998) по сравнению с контролем диффузная экспрессия в виде относительно равномерного глыбчатого накопления иммунореактивного материала в цитоплазме перикарионов и ядерных оболочках большинства нейронов указанных отделов головного мозга, в то время как в глиальных клетках экспрессия была минимальна или отсутствовала (степень 0–1). Эндотелий капилляров в группах 2 и 3 имел слабо выраженную (степень 1) экспрессию изучаемых антигенов в цитоплазме, в контрольной группе имела место иммунонегативная реакция. Усиление TRPM6-иммунопозитивной реакции в большинстве нейронов в опытных группах отражает, по нашему мнению, адаптивные реакции при изменении магниевого гомеостаза, направленные на усиление трансцеллюлярного переноса ионов магния. Данное предположение согласуется с данными о клаудин-16-ассоциированном трансцеллюлярном транспорте ионов магния через каналы TRPM6 в дистальных почечных канальцах [7].
При иммуногистохимическом методе с использованием антител к TRPM7 в опытных группах (2 и 3) отмечалось умеренное и выраженное (степени 2–3) мозаичное иммунопозитивное окрашивание цитоплазмы перикарионов и отростков нейронов отмеченных отделов головного мозга; при этом встречалось не менее 30 % нейроцитов с иммунонегативной реакцией. Ядра и ядрышки большинства нейроцитов были слабо иммунопозитивными или негативными. Глиальные клетки этих областей были слабо иммунопозитивны. Эндотелиоциты капилляров имели слабо выраженную экспрессию (степень 1) изучаемых антигенов в цитоплазме. Усиление цитоплазматической экспрессии белка TRPM7 в нейронах при моделируемой магниевой недостаточности может являться специфическим маркером повреждения высокоспециализированных в функциональном отношении клеток при нарушении магниевого гомеостаза, что подтверждает результаты похожих исследований, указывающих на ключевую роль активации TRPM7 при аноксической дегенерации нейронов [4]. По мнению других исследователей [9], изменение функциональной активности TRPM7 может отражать нарушения процессов холинергической нейротрансмиссии в нейронах головного мозга, что в условиях дефицита магния, по нашему мнению, сопровождается нарушением процессов синаптической пластичности.
При иммуногистохимическом исследовании с использованием антител к эндотелиальной нитрооксидсинтазе (e-NOS) в опытных группах отмечалось преобладание нейронов, глиоцитов и эндотелиоцитов капилляров отмеченных отделов головного мозга с иммунонегативной или слабо иммунопозитивной (степень 0–1) цитоплазматической экспрессией белка по сравнению с контролем (степень 2). При иммуногистохимическом исследовании с использованием антител к индуцибельной нитрооксидсинтазе (i-NOS) в опытных группах отмечалось увеличение удельного количества нейронов и эндотелиоцитов капилляров отмеченных отделов головного мозга с усиленной иммунопозитивной реакцией цитоплазмы (степень 2), в отличие от контроля, где преобладали иммунонегативные клетки (степень 0). Разнонаправленные преобразования иммуноэкспрессии e-NOS и i-NOS в нейронах и эндотелиоцитах согласуются с концепцией о развитии в условиях дефицита магния эндотелиальной дисфункции, а также данными о повреждении нейроцитов, обусловленном снижением продукции оксида азота (NO), важнейшего модулятора синаптической пластичности [6], реакциями оксидативного стресса, связанными с активацией i-NOS [2].
При иммуногистохимическом исследовании первичной и вторичной моторной коры полушарий большого мозга, крупноклеточных ядер гипоталамуса, гиппокампа, среднего мозга с использованием антител к GFAP в опытных группах отмечалось усиленное по сравнению с контролем иммунопозитивное окрашивание цитоплазмы астроцитов, при этом встречались в большом количестве по сравнению с контролем периваскулярно расположенные фибриллярные астроциты с выраженным усилением экспрессии GFAP (степень 2–3). Усиление астроглиальной реакции в отмеченных отделах головного мозга сочеталось с обнаруженным нами увеличением удельной площади нейропиля, что отражает процессы репаративной регенерации в головном мозгу при моделируемом дефиците магния.
При электронно-микроскопическом исследовании паравентрикулярного и супраоптического ядер гипоталамуса у животных с моделируемым дефицитом магния встречались два типа нейронов: «светлые», которые характеризовались низкой электронной плотностью цитоплазмы, конденсацией гранул рибонуклеопротеинов рибосомного типа на ядерной мембране, в окружности которой отмечалось скопление митохондрий с разрежением матрикса, лизосом; «темные», для которых была характерна выраженная осмиофилия цитоплазмы, снижение количества и размеров внутриклеточных органелл, с признаками их повреждения (вакуолизация, лизис крист митохондрий, деформация ядер и очаги разрушения ядерной оболочки) (рис. 1).
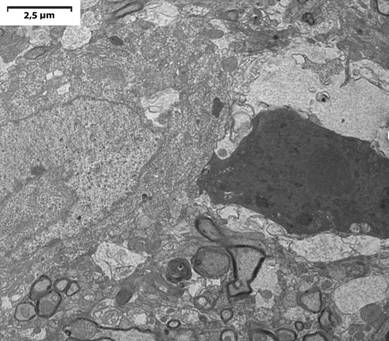
Рис. 1. «Светлые» и «темные» нейроны в паравентрикулярном ядре гипоталамуса при дефиците магния 8 недель. Ув. ×6000
Наблюдалось относительное уменьшение количества аксо-дендритических синапсов в непосредственной близости от перикарионов нейронов. Эти синапсы имели асимметричный тип по Грею, с нечетко выраженной синаптической щелью, участками слияния пре- и постсинаптической мембран, неравномерным накоплением синаптических пузырьков с умеренным и слабо выраженным электронно-плотным содержимым. В нейропиле отмечалось относительное увеличение числа аксо-соматических синапсов, представленных синапсами асимметричного типа по Грею, содержащих множество мембранных везикул с содержимым умеренной и высокой электронной плотности диаметром около 80–100 нм в пресинаптических и постсинаптической частях. Изменения синаптического аппарата при моделировании дефицита магния отражают, по нашему мнению, преобразование синаптической пластичности [8]. В некоторых отделах нейропиля при дефиците магния отмечался выраженный периаксональный отек, разрушение мембран отростков нейронов с накоплением лизосом и фаголизосом. Увеличение количества вакуолей с содержимым высокой электронной плотности в нейросекреторных клетках гипоталамуса при дефиците магния может свидетельствовать о включении механизмов аутофагии, которые, как известно, могут быть фактором, способствующим выживанию нейронов даже при инициированной программе гибели, например, апоптозе [1].
В проведенном нами исследовании у всех животных с моделируемым дефицитом магния в головном мозгу отмечались явления внутриклеточного и перицеллюлярного отека, в ряде случаев, имел место и периваскулярный отек. Подобные изменения могут быть связаны с нарушением водно-электролитного баланса, обусловленным дисфункцией вазопрессинергических нейронов гипоталамуса.
При морфометрическом анализе изменений (табл. 1) в головном мозгу обнаружено уменьшение площади цитоплазмы перикарионов крупных нейросекреторных клеток паравентрикулярных ядер гипоталамуса на 12,3 % (р<0,05) к 8 неделе моделирования дефицита магния и на 14,8 % (р<0,05) к 12 неделе эксперимента, уменьшение площади перикарионов пирамидных нейронов CA1 и CA3 полей гиппокампа на 16,1 % и 14,4 % (р<0,05) соответственно во 2 группе и на 16,8 % и 15,2 % (р<0,05) соответственно в 3 группе, что свидетельствует о развитии процессов атрофического характера при моделировании алиментарного дефицита магния. Увеличение по сравнению с контролем площади перикарионов нейронов мелкоклеточной части паравентрикулярных ядер гипоталамуса на 11,7% (р<0,05) при 8 недельном дефиците магния и на 12,1 % (р<0,05) при 12-недельном дефиците магния, в сочетании с данными светооптического и ультраструктурного исследования свидетельствует о преобладании процессов повреждения при дефиците магния, с прогрессивной динамикой к 12 неделе эксперимента.
Таблица 1
Изменение некоторых морфометрических параметров головного мозга при алиментарном дефиците магния (М±m)
|
1 группа (контрольные животные) |
2 группа (дефицит магния 8 недель) |
3 группа (дефицит магния 12 недель) |
|
|
Средняя площадь перикарионов крупных нейронов паравентрикулярных ядер гипоталамуса, мкм2 |
221,1 ± 5,7 |
193,9 ± 4,6* |
188,3 ± 4,3* |
|
Средняя площадь перикарионов мелких нейронов паравентрикулярных ядер гипоталамуса, мкм2 |
117,2 ± 3,1 |
130,9 ± 4,2* |
131,3 ± 4,9* |
|
Средняя площадь перикарионов пирамидных нейронов СА1, мкм2 |
103,1 ± 3,7 |
86,5 ± 3,1* |
85,7 ± 3,2* |
|
Средняя площадь перикарионов пирамидных нейронов СА3, мкм2 |
109,2 ± 3,8 |
93,4 ± 3,2* |
92,6 ± 3,6* |
Обозначения: * – достоверное отличие в сравнении с группой 1 при р<0,05; M – средняя величина; m – стандартная ошибка средней величины; СА1, СА3 – поля гиппокампа.
Выводы
При моделировании алиментарного дефицита магния в течение 8 и 12 недель в головном мозгу преобладают процессы повреждения нейронов в крупноклеточных ядрах гипоталамуса, в пирамидном слое CA1 и CA3 полей гиппокампа, первичной и вторичной моторной коре полушарий большого мозга, ретикулярной формации ствола головного мозга, коре полушарий мозжечка. В условиях моделируемого дефицита магния усиление экспрессии белка TRPM7 и индуцибельной нитрооксидсинтазы в цитоплазме перикарионов и отростков нейронов гипоталамуса, гиппокампа, коры полушарий конечного мозга и полушарий мозжечка свидетельствует о повреждении энергетического аппарата клеток и проявлении реакций оксидативного стресса. Диффузное усиление цитоплазматической и ядерной экспрессии белка TRPM6 в нейронах в сочетании со сниженной экспрессией эндотелиальной нитрооксидсинтазы отражает комбинацию альтеративных и компенсаторно-приспособительных процессов. Обратимое повреждение нейронов гипоталамуса, установленное на светооптическом уровне в динамике экспериментального моделирования дефицита магния (8–12 недель), а также при ультраструктурном исследовании, характеризуется признаками дегенерации нейросекреторных клеток, структурной перестройкой синаптического аппарата, и сопровождается компенсаторными процессами в виде атрофии нейронов, гиперхроматоза цитоплазмы их перикарионов, отражая патоморфологические механизмы нейропластичности.
Рецензенты:
Ермилов Виктор Владимирович, доктор медицинских наук, профессор кафедры судебной медицины ВолгГМУ, г. Волгоград.
Григорьева Наталья Владимировна, доктор медицинских наук, профессор кафедры патологической анатомии ВолгГМУ, г. Волгоград.



