Э. И. Гальперин определяет печеночную недостаточность как несоответствие между потребностями организма и возможностями печени в удовлетворении этих потребностей [5]. Кутепов Д. Е. (2004) вносит уточнение в общее понятие и термин ОППН обозначает декомпенсацию функции печени, которая проявляется возникновением желтухи, коагулопатии и печеночной энцефалопатии (ПЭ), нередко переходящей в коматозное состояние [7].
В резекционной хирургии цирротически измененной печени развитие ОППН, как правило, связывают с несоответствием потребностей организма и возможностями остающейся после резекции части печени, функциональная способность которой исходно резко снижена [8, 9]. Именно это несоответствие ограничивает показания к радикальным операциям и, особенно, к резекциям печени в объеме гемигепатэктомии и более. Поскольку потребность в трансплантации печени значительно превышает возможности её проведения, перед хирургами остро встает проблема расширения показаний к резекциям печени на фоне цирроза. Одним из путей решения этой проблемы является интра- и послеоперационная защита печеночной ткани с целью профилактики развития тяжелой прогрессирующей ОППН.
Цель работы. Расширение показаний к радикальным операциям и улучшение результатов хирургического лечения больных с очаговыми поражениями печени, ассоциированными с циррозом.
Материал и методы. В клинике госпитальной хирургии ГБОУ ВПО Кировской ГМА Минсоцздравразвития на базе 1 ХО Кировской областной клинической больницы в период с 1994 по 2011 годы наблюдался 91 пациент с очаговыми заболеваниями печени, ассоциированными с циррозом: женщин - 39 (42,8 %), мужчин - 52 (57,14 %) в возрасте от 11 до 83 лет. Средний возраст больных составил 57,6±17,7лет.
Всего радикально оперированы 33 пациента (36,26 %). С целью профилактики и лечения, а также снижения тяжести проявлений ОППН разработан алгоритм интраоперационной и послеоперационной терапии, основанный на внутрипортальном введении гепатопротекторов и мембраностабилизаторов в максимальных терапевтических дозах.
Двадцать пять пациентов оперированы без использования разработанного алгоритма (контрольная группа), восьми больным во время и после операции проводилась внутрипортальная инфузия гепатопротекторов (исследуемая группа). Обе группы сопоставимы между собой.
Очаговые поражения в исследуемых группах были представлены следующими нозологическими формами: доброкачественные образования - 6 больных (18,2 %), злокачественные опухоли - 27 (81,8 %), в том числе: первичный рак - 26 (78,8 %), метастатическое поражение - 1 (3,03 %). Резекции печени в объеме гемигепатэктомии и более выполнены у 12 (36,3 %) пациентов (исследуемая группа - 2, контрольная - 10): правосторонняя гемигепатэктомия у - 8, расширенная правосторонняя гемигепатэктомия - у 3, левосторонняя гемигепатэктомия - у 1. Экономные резекции печени были выполнены у 21 (63,6 %) больного (исследуемая группа - 6, контрольная - 15): трисегментэктомия (5,6,7S) у - 9, кавальная левосторонняя лобэктомия у - 7, сегментэктомии и атипичные резекции у - 5. Цирроз класса Апо Child-Pugh являлся фоновым процессом у 25 (75,7 %) пациентов, класса В - у 8 (24,2 %). Резекции печени больным с циррозом класса С по Сhild-Pugh не выполняли, так как считаем эту стадию абсолютным противопоказанием к операции.
Производили изучение исходного функционального статуса печени, пораженной диффузным процессом и динамику изменений клинико-лабораторных показателей в послеоперационном периоде. Обработка данных производилась общепринятыми статистическими методами. При оценке результатов использовался критерий Х2 и точный критерий Фишера. Уровень статической значимости устанавливался прир<0,05.
В таблице 1 представлен исходный функциональный статус печени и диаметр воротной вены.
Производящими факторами и основными маркерами развития послеоперационной печеночной недостаточности являлись показатели холестаза и печеночно-клеточная недостаточность (белоксинтетическая функция). Так как печеночная недостаточность после резекции печени развивается вследствие недостаточного объема остающейся паренхимы печени, индикаторы синдрома цитолиза (АСТ, АЛТ) не расценивали в качестве проявлений послеоперационной печеночной недостаточности.
Таблица 1. Исходный функциональный статус печени в исследуемых группах
|
Показатели |
Значение |
|
|
Контрольная группа (n=23) |
Исследуемая группа(n=8) |
|
|
АсТ (Ед/л.) (N<42) АлТ (Ед/л.) (N<42) |
110,31±35,2* 130,2±41,2* |
98,23±32,1* 92,36±34,7* |
|
ЩФ (Ед/л.) (N<306) ГГТП (Ед/л.) (N<61) |
430,45 ± 62,2*; 80,6 ± 43,2* |
436,34±57,3*; 81,2 ± 41,3* |
|
Альбумин (г/л.) (N=35-53) |
38,57±21,1* |
39,61±18,9* |
|
Тромбоциты (х109/л) (N=180-320) |
212,23±43,1* |
198,1±23,6* |
|
Биллирубин (мкмоль/л.) (N<20,5) |
26,4±8,9* |
28,2±7,9* |
|
Протромбиновый индекс (%) (N=80-120) |
78,24±28,9* |
77,17±31,1* |
|
Диаметр воротной вены по УЗИ (мм) (N<14мм) |
19,2±3,6* |
18,4±4,6* |
*- p>0,05.
Пациентам исследуемой группы (n = 8) после мобилизации печени и определения окончательного объема удаляемой и остающейся части паренхимы производили бужирование и катетеризацию пупочной вены подключичным катетером обычного диаметра (СН 10-1,0мм) для внутрипортальной инфузии. До начала и по ходу разделения паренхимы печени производили введение изотонического раствора глюкозы и 1,5 % раствора реамберина со скоростью не более 2,5-3,0 мл/мин через инфузомат. После окончания интраоперационной инфузии катетер выводился на переднюю брюшную стенку и фиксировался к коже обычным способом для последующей послеоперационной внутрипортальной терапии по следующей схеме: гептрал - 400 мг на 200,0 мл 0,9 % раствора NaCl и дексаметазон 4 мг. Терапия проводилась 1 раз в сутки, медиана времени введения - 110 минут, длительность лечения 5-6 суток (среднее время «работы» катетера). По окончании лечения катетер удаляли.
Для оценки тяжести ОППН пользовались классификацией печеночной недостаточности, предложенной Гальпериным Э. И. (1978). Степень тяжести гепатопатии оценивали согласно критериям Шиманко Ш. И. и Лужникова Е. А. (1974).
Степень тяжести послеоперационной печеночной энцефалопатии оценивалась в соответствии с критериями Брайтон (1992) [7]. В послеоперационном периоде все пациенты консультированы неврологом на 1-е, 5-е и 14-е сутки. Для определения процесса восстановления когнитивных функций использовали тест связи чисел, разработанный Соnn HO (1977) [7]. Дополнительно перед инфузией измерялось внутрипортальное давление аппаратом Вальдмана через катетеризированную пупочную вену.
Результаты. Оценку эффективности применения внутрипортальной инфузии гепатопротекторов проводили по следующим показателям: 1. Динамика улучшения белок - синтетической функции печени. 2. Динамика уменьшения уровня холестаза. 3. Динамика уменьшения тяжести печеночной энцефалопатии.
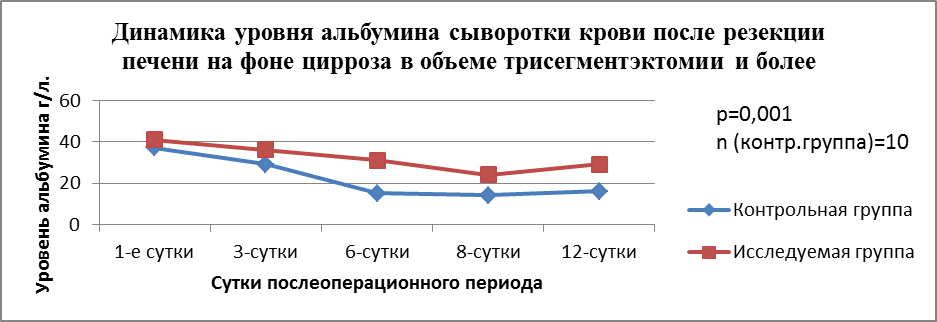
Ниже приведена динамика изменений синдромахолестаза (ЩФ) и печеночно-клеточной недостаточности (уровень альбумина сыворотки крови) у пациентов, оперированных по поводу первичного рака в объеме трисегментэктомии и более на фоне цирроза класса А по Child-Pugh. Контрольная группа (n=10), исследуемая (n=7). Результаты приведены в диаграммах 1 и 2.
Диаграмма 1
Динамика изменения уровня щелочной фосфатазы (ЩФ) в сыворотке крови оперированных больных представлена в диаграмме 2.
Диаграмма 2
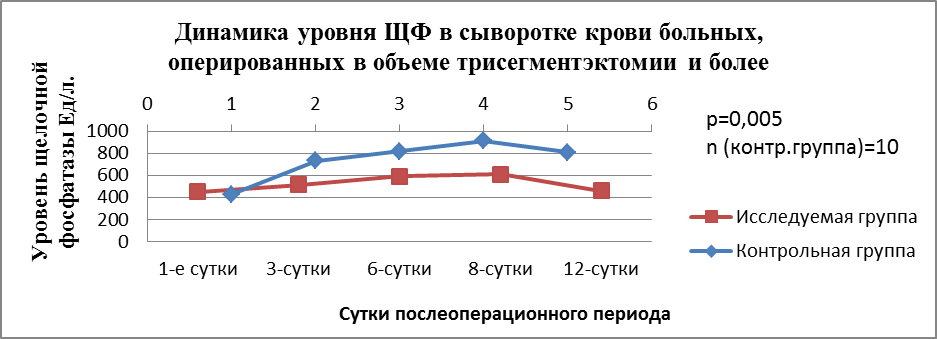
Представленные диаграммы демонстрируют более плавное и менее выраженное снижение уровня альбумина крови в исследуемой группе, а также меньшее повышение уровня ЩФ сыворотки крови в исследуемой группе по сравнению с контрольной.
При исследовании степени тяжести послеоперационной печеночной недостаточности оценивались клинико-лабораторные показатели гепатопатии в группах больных после резекции печени различного объема. В контрольной группе (n=25) печеночная недостаточность средней степени тяжести выявлена у 11 (44 %) больных после малых (сегмент- и бисегментэктомии) и атипичных резекций, с более гладким течением при наличии крупноузлового цирроза. В исследуемой группе печеночная недостаточность после малых резекций не зафиксирована, даже при наличии мелкоузлового цирроза. При выполнении трисегментэктомий и гемигепатэктомий в контрольной группе у всех больных наблюдалась печеночная недостаточность тяжелой степени, сопровождавшаяся печеночной энцефалопатией (ПЭ) 1-2 стадии по Брайтон, из них у 6 (24 %) пациентов отмечено постепенное прогрессирование печеночной недостаточности до крайне тяжелой, с присоединением почечной недостаточности, сердечно-сосудистых нарушений, прекомой и комой. В исследуемой группе у 4 (57,14 %) больных зафиксирована печеночная недостаточность тяжелой степени, сопровождавшаяся у 3(75 %) больных ПЭ 1-2стадии.
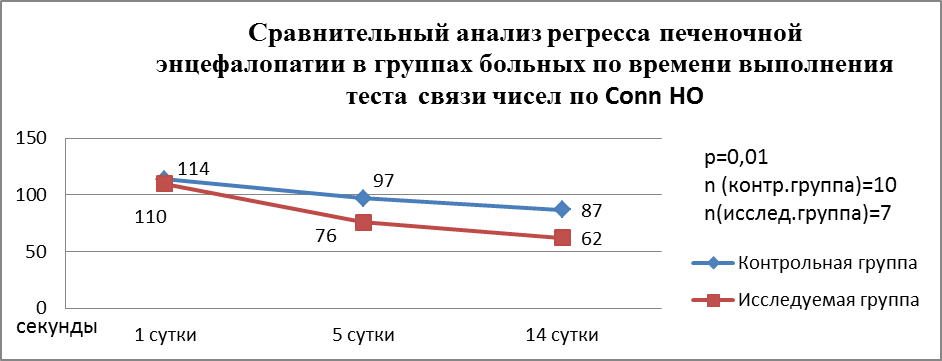
Внутрипортальнаяинфузия привела к снижению тяжести печеночной энцефалопатии в исследуемой группе и улучшению когнитивных функций головного мозга больных по сравнению с пациентами контрольной группы.
В диаграмме № 3 представлена динамика регресса печеночной энцефалопатии в группах больных по времени выполнения теста связи чисел по Соnn HO после трисегментэктомии и более на фоне цирроза класса А по Child-Pugh.
Диаграмма 3
При изучении динамики изменения портального давления в исследуемых группах достоверных различий выявлено не было. Исходное давление, измеренное до начала резекции, равнялось в среднем 292,66 ± 79,77 мм вод. ст., 1-е сутки после резекции - 365,058± 60,2 мм вод. ст. При сопутствующем крупноузловом «мягком» циррозе с меньшим количеством фиброзной ткани к 5-м суткам послеоперационного периода отмечалось постепенное снижение внутрипортального давления до уровня 304,28 ± 36,16 мм вод. ст. При наличии мелкогоузлового «плотного» цирроза снижение портального давления было незначительным и уровень его составил в среднем 345,68 ± 58,15 мм вод. ст. (p< 0,05).
Осложнения в послеоперационном периоде отмечены в исследуемой группе у 5 (62,5 %) больных, в контрольной группе у 18 (72%). В исследуемой группе они представлены: тяжелая печеночная недостаточность - 4 (50 %), реактивный плеврит - 3 (37,5 %), нагноение послеоперационной раны - 1 (12,5 %), в контрольной группе тяжелая печеночная недостаточность - 14 (56 %), реактивный плеврит - 15 (60 %), стойкие желчные свищи - 3 (12 %), пневмония - 4 (16 %), нагноение послеоперационной раны - 3 (12 %). Причиной летальных исходов в обеих группах являлась прогрессирующая печеночная недостаточность. В контрольной группе умерло 6 (24 %) пациентов, в исследуемой группе умер 1 (12,5 %) пациент.
Обсуждение. Общеизвестно, что при цирротической транформации печени общий объем ее портального сосудистого русла уменьшается из-за сморщивания и облитерации мелких разветвлений воротной вены, сокращения сети синусоидов, а также повышения внутрипортального давления после резекции печени. Вводимые в системный кровоток лекарственные средства идут в обход облитерированной капиллярной сети печени через отдельные сформированные портосистемные анастомозы. В итоге объем проходящих через печень лекарственных сред значительно сокращается, и они в неизменном виде выделяются почками. Методы регионарной внутрипортальнойтерапии позволяют подводить лекарственные средства высокой концентрации непосредственно к очагу повреждения и значительно повысить эффективность проводимого лечения. Целенаправленная доставка лекарственных веществ к сосудисто-паренхиматозному аппарату печени принципиально возможна лишь при использовании портального русла [6]. Этим и обусловлен выбор именно внутрипортальной инфузии перед обычным внутривенным введением.
При анализе послеоперационного периода у пациентов после резекции компрометированной печени можно отметить следующие особенности его течения: стопроцентное развитие послеоперационной печеночной недостаточности разной степени тяжести с четкой прямой корреляционной зависимостью от объема резекции, тяжесть данного осложнения более выражена при злокачественном поражении, так как удаляется не только очаг (функционально неактивный), но и функционирующая часть печени. Принципы радикализма требуют удаления паренхимы печени, отступая минимум 2 см от очага.
Ассоциация очагового поражения с мелкоочаговым циррозом («плотный» цирроз с выраженным фиброзом) является абсолютным противопоказанием к обширным резекциям печени, не продлевающим продолжительность жизни и значительно увеличивающим летальность. Пациентам этой группы показаны сегментарные резекции печени, либо химическая абляция (введение в очаг 95 % спирта). Перспективным вмешательством можно считать радиочастотную абляцию.
В послеоперационном периоде отмечено постепенное нарастание показателей холестаза и печеночно-клеточной недостаточности с максимумом на 8-9 сутки. В дальнейшем отмечается либо утяжеление состояния, либо постепенное восстановление функций печени. При изучении динамики портального давления отмечается выраженное его повышение в 1- е сутки после операции. Степень портальной гипертензии (ПГ) постепенно снижается к 5-м суткам при сопутствующем крупноузловом циррозе. При ассоциации с «плотным» мелкоузловым циррозом портальная гипертензия сохраняется на высоком уровне в течение всего периода наблюдения.
Внутрипортальное введение гепатопротекторов и мембраностабилизаторов достоверно снижает биохимические показатели основных проявлений печеночной недостаточности - синдромов холестаза и печеночно-клеточной недостаточности, а также приводит к более быстрому восстановлению когнитивных функций головного мозга пациентов, тем самым уменьшая тяжесть проявлений печеночной энцефалопатии.
Таким образом, использование внутрипортальной гепатопротективной и мембраностабилизирующей терапии приводит к уменьшению частоты печеночной недостаточности после малых резекций (на 44 %). Частота развития тяжелой ОППН после гемирезекций печени снижена на 42,8 %. Удалось снизить летальность с 24 % до 12,5 %.
Выводы. Исходя из вышеизложенного, можно сделать следующие выводы:
- Послеоперационная печеночная недостаточность является неизбежным специфическим осложнением резекции компрометированной цирротическим процессом печени.
- Профилактику печеночной недостаточности целесообразно начинать с предоперационного отбора пациентов на оперативное вмешательство и продолжать в интраоперационном и послеоперационном периодах.
- Интраоперационная и послеоперационная гепатопротективная внутрипортальная терапия снижает тяжесть основных клинико-биохимических синдромов печеночной недостаточности, уменьшает частоту её возникновения при малых резекциях и степень тяжести при гемирезекциях, пораженной циррозом печени.
Рецензенты:
- Капутин Борис Борисович, д.м.н., профессор, зав. кафедрой госпитальной хирургии ГБОУ ВПО Ижевская государственная медицинская академия Минсоцздравразвития России, г. Ижевск.
- Журавлев Валентин Андреевич, д.м.н., профессор, зав. кафедрой хирургии с курсом травматологии и ортопедии ИПО ГБОУ ВПО Кировская ГМА Минсоцздравразвития России, г. Киров.
Библиографическая ссылка
Бахтин В.А., Янченко В.А., Кучеров А.А., Кучеров А.А. ПРОФИЛАКТИКА И ЛЕЧЕНИЕ ОСТРОЙ ПОСЛЕОПЕРАЦИОННОЙ ПЕЧЕНОЧНОЙ НЕДОСТАТОЧНОСТИ ПРИ РЕЗЕКЦИИ ЦИРРОТИЧЕСКИ ИЗМЕНЕННОЙ ПЕЧЕНИ // Современные проблемы науки и образования. – 2012. – № 3. ;URL: https://science-education.ru/ru/article/view?id=6353 (дата обращения: 27.04.2024).



