Хилоторакс – это скопление хилезной жидкости в плевральной полости как результат травмы или закупорки грудного протока, правого лимфатического протока или их ветвей. Основная функция хилуса иммунологическая и транспортная, один литр содержит 30 г белка, 30 г жиров, электролиты, жирорастворимые витамины, микроэлементы и жирные кислоты [1]. Большой объем лимфоистечения способен привести к тяжелым расстройствам питания, нарушениям функций иммунной системы и дыхательной недостаточности.
Традиционно лечение хилоторакса начинают с консервативных мероприятий и малоинвазивных хирургических процедур, таких как торакоцентез и дренирование плевральной полости, контроль уровня электролитов и белка в крови, частичное или полное парентеральное питание, а также диета с низким содержанием жиров для уменьшения образования хилуса [2]. Данных методов лечения придерживаются в течение 14 дней, а эффективность составляет примерно 50% [3]. Химический плевродез, направленный на облитерацию плевральной полости, является весьма эффективным способом борьбы с рецидивирующим плевральным выпотом и пневмотораксом. К данной процедуре прибегают при безуспешности вышеописанных способов лечения.
Цель исследования
Провести анализ лечения пациентки с послеоперационным хилотораксом, осложненным коронавирусной инфекцией 2019 года (COVID-19). Оценить возможность применения химического плевродеза на ранних стадиях лимфоистечения в плевральную полость, а также эффективность и безопасность йодповидона в качестве плевросклерозанта. Оценить перспективу научного исследования данной проблемы с последующим внедрением индукции плевродеза в тактику ведения пациентов с хилотораксом на самых ранних стадиях.
Материал и методы исследования
Под нашим наблюдением находилась пациентка Л. 65 лет, которая поступила в отделение торакальной хирургии Национального госпиталя Министерства здравоохранения Киргизской Республики 07.10.2020 с жалобами на одышку при физической нагрузке, общую слабость, головокружение, периодическое повышение температуры тела.
Из анамнеза: 22.09.2020 была оперирована в Бишкекском национальном исследовательском центре травматологии и ортопедии по поводу застарелого перелома L1 позвонка, была произведена торакотомия слева по X м/р, передний корпородез со стабилизацией кейдж-домкратом Th12-L1. Выписана на 8-е сутки после операции. С 03.10.2020 стала отмечать ухудшение состояния, появилась одышка при физической нагрузке, общая слабость, повышение температуры тела. Обратилась в частный медицинский центр, было проведено УЗИ, на котором обнаружена жидкость в плевральной полости слева. Произведена пункция плевральной полости слева, удалено 1200 мл жидкости, по виду напоминающей млечный сок. Через 2 дня вновь удалено 1200 мл аналогичной жидкости. Диагноз послеоперационного хилоторакса сомнений не вызывал, и пациентка была направлена в профильное отделение. Учитывая эпидемиологическую ситуацию, перед поступлением пациентка в обязательном порядке сдала ИФА на антитела к коронавирусу SARS-CoV-2: lgG-КП=0,17 (отрицательный) и lgM-КП=0,24 (отрицательный).
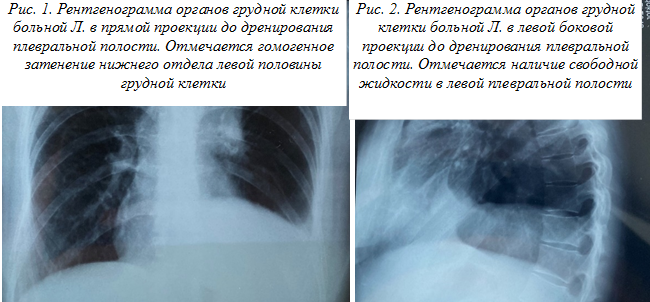
При поступлении в отделение торакальной хирургии общее состояние средней степени тяжести. Температура тела 38 °С. При перкуссии: выявлено притупление легочного звука в нижних отделах левой половины грудной клетки. При аускультации: дыхание в нижних отделах левого гемиторакса резко ослаблено. Тоны сердца ясные и ритмичные. Артериальное давление (АД) 90/60 мм рт. ст. Пульс удовлетворительного наполнения, 92 уд./мин. Со стороны органов брюшной полости, при физикальном обследовании, каких-либо изменений не выявлено. Живот участвует в акте дыхания. При пальпации мягкий, безболезненный. Общий анализ крови от 07.10.2020: эритроциты 3,7х1012/л, hb 110 г/л, лейкоциты 9,8х1012/л: э 1%, п/я 7%, с/я 60%, л 26%, м 6%, СОЭ 25 мм/ч. Биохимические анализы крови от 07.10.2020: общий белок 58 г/л, альбумин, 28 г/л; АСТ 23 ЕД/л, АЛТ 20 ЕД/л; креатинин 87 мкмоль/л, глюкоза крови 5,5 ммоль/л. 07.10.2020 произведена R-графия органов грудной клетки (ОГК) в прямой (рис. 1) и левой боковой (рис. 2) проекциях, а также УЗИ, на которых обнаружено наличие свободной жидкости в левой плевральной полости, без каких-либо инфильтративных или очаговых теней.
В день поступления пациентке произведено дренирование плевральной полости слева в VII м/р по задне-подмышечной линии, получено 500 мл жидкости молочного характера. Назначена диета с низким содержанием жиров, антибактериальная, плазмозамещающая, восполняющая водно-электролитный баланс и обезболивающая терапии. Анализ плевральной жидкости: цвет - белый; прозрачность - мутная, реакция Ривольта положительная +++, белок - 26,4 г/л, лейкоцитов большое количество, эритроцитов 25-29 в поле зрения. На основании клинического обследования и анамнеза установлен диагноз: Послеоперационный хилоторакс слева. Состояние после операции по поводу компрессионного перелома позвоночника на уровне L1.
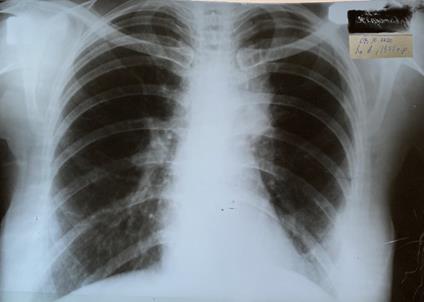  |
На контрольных R-граммах ОГК в прямой (рис. 3) и левой боковой проекциях от 08.10.2020 левое легкое полностью расправлено, в нижних отделах слева отмечается понижение прозрачности за счет гиповентиляции. В нижнем легочном поясе справа отмечается локальное изменение, усиление легочного рисунка за счёт периваскулярного компонента. Очаговых и инфильтративных теней нет. Корни легких неструктурные. Синус справа свободен. Тень сердца без особенностей. Аорта уплотнена.
08.10.2020 вместо традиционной выжидательной тактики было решено произвести индукцию плевродеза слева. Стоит отметить, что с момента дренирования до проведения рентгенографии ОГК прошло примерно 20 часов, при этом количество выделившегося хилуса составило 350 мл.
С целью обезболивания, предварительно, было введено 50 мл 1% раствора лидокаина с экспозицией 20 минут через дренажную трубку. В качестве плевросклерозанта был выбран йодповидон, так как в нашей практике он зарекомендовал себя как эффективный, безопасный и доступный агент. До процедуры температура тела больной составляла 36,5 °С, пульс 79 ударов в минуту, АД 110/70 мм рт. ст. Экспозиция йодповидона составила 2 часа, при этом пациентка осуществляла активные дыхательные движения и меняла положение тела для лучшего контакта с плевральной поверхностью. После процедуры пациенткой было отмечено однократное повышение температуры тела до 37,1 °С, болевые ощущения были оценены на 3 из 10 по визуально-аналоговой шкале, пульс составил 85 ударов в минуту, АД 110/70 мм рт. ст. В период с 9 по 11 октября 2020 отделяемое по дренажной трубке составило 250, 200 и 50 мл соответственно, характер жидкости оставался прежним.
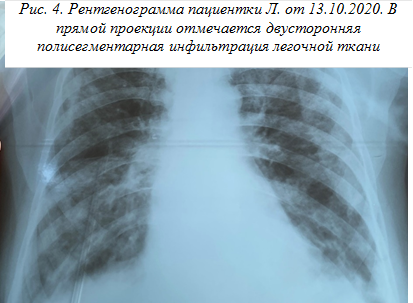 |
11.10.2020 состояние больной стало прогрессивно ухудшаться, появилась одышка в покое, усиливающаяся при малейшем движении, ЧД 32 уд./мин. в покое, пульс 104 уд./мин., АД 90/60 мм рт. ст., температура тела повысилась до 38,2 °С. В связи с этим пациентка была переведена в отделение интенсивной терапии с клиникой острого респираторного дистресс-синдрома (ОРДС), SpO2 без кислородной поддержки составила 45%. Общий анализ крови от 11.10.2020: эритроциты 3,5х1012/л, hb 108 г/л, лейкоциты 10,0х1012/л: э 0%, п/я 4%, с/я 44%, л 22%, м 30%, СОЭ 30 мм/ч. Биохимические анализы крови от 07.10.2020: общий белок 67 г/л, альбумин, 38 г/л; АСТ 39 ЕД/л, АЛТ 30 ЕД/л; креатинин 66 мкмоль/л, глюкоза крови 6,1 ммоль/л. На рентгенограммах ОГК от 11.10.2020 и 13.10.2020 (рис. 4) имелась выраженная двусторонняя полисегментарная инфильтрация легочных полей, причем с отрицательной рентгенологической динамикой, свободной жидкости в плевральных полостях не было, легкие были полностью расправлены. 13.10.2020 произведена полимеразно-цепная реакция на SARS-CoV-2, которая 14.10.2020 дала положительный результат, и больная была переведена в карантинно-казарменный стационар для пациентов с коронавирусной инфекцией 2019 года. Дренажная трубка из плевральной полости была удалена только после полного прекращения экссудации 14.10.2020.
Находилась на лечении в карантинно-казарменном стационаре 17 дней, в течение которых получала соответствующее лечение согласно клиническому руководству, утвержденному Министерством здравоохранения Киргизской Республики. 14 дней пациентка провела в отделении интенсивной терапии. Неоднократно производился рентгенологический контроль органов грудной клетки и ультразвуковой контроль синусов плевры, при этом жидкости в плевральных полостях не было обнаружено. Была выписана в относительно удовлетворительном состоянии на амбулаторное наблюдение. Контрольные осмотры были назначены через 1, 3 и 6 месяцев. Первые два обращения показали отсутствие рецидива хилоторакса.
Результаты исследования и их обсуждение
Послеоперационное истечение хилезной жидкости в плевральную полость является опасным осложнением хирургических вмешательств на органах грудной клетки, частота данного осложнения составляет от 0,5% до 2,3% [4; 5]. Хотя частота низкая, травматический хилоторакс способен привести к тяжелым проблемам иммунной системы, пневмониям, а также к летальному исходу в 30% случаев [6].
Причины хилоторакса подразделяются на три категории: нетравматический, травматический и идиопатический. В историческом аспекте нетравматические причины хилоторакса составляли две трети всех случаев. Последние данные литературы свидетельствуют о преобладании травматических причин, а именно об осложнениях при операциях на органах грудной клетки [7-9].
Несмотря на отсутствие четких клинических рекомендаций по ведению пациентов с хилотораксом, в литературных данных особую роль придают консервативным методам лечения. В основном пациента переводят на частичное или полное парентеральное питание, диету с низким содержанием жиров, что требует длительного нахождения больного в специализированном стационаре, а также применения дорогостоящих препаратов для инфузии, переливания альбумина, процедур терапевтического торакоцентеза и дренирования плевральной полости [3; 10].
Постановка дренажной трубки в плевральную полость позволяет легкому расправиться, что улучшает его дыхательные функции, но, с другой стороны, ведет к увеличению риска инфекции, а также к неконтролируемой потере белков, жиров и электролитов. Соответственно, чтобы снизить риск развития осложнений, длительность нахождения дренажа не должна превышать 14 дней. В этот период пациент должен находиться на специальной диете или получать питание парентеральным путем [2; 10]. К хирургическим методам лечения прибегают при безуспешности консервативных мероприятий или в случае ежесуточной потери лимфатической жидкости более одного литра [3]. К хирургическим способам лечения относятся перевязка грудного протока, ушивание его дефекта, плеврэктомия, плевровенозное или плевроперитонеальное шунтирование [3]. С развитием интервенционной хирургии свою нишу в лечении хилоторакса получила эндоваскулярная эмболизация грудного протока [11].
Химический плевродез – это процедура, направленная на искусственное асептическое воспаление листков плевры, путем введения плевросклерозанта, с последующей облитерацией плевральной полости. Данный метод лечения с успехом применяется для лечения пациентов с рефрактерными плевральными выпотами, а наиболее распространенными препаратами являются тальк, тетрациклин, блеомицин и гипертонический раствор глюкозы (3). Основными требованиями, предъявляемыми к химическим агентам, являются безопасность, эффективность и доступность. В данном отношении, в практике врача торакального профиля нашего региона, широкое применение получил способ индукции плевродеза комбинацией 10% раствора йодповидона и 40% р-ра глюкозы, являясь весьма эффективным методом в борьбе с плевральными выпотами различной этиологии [12].
Еженедельный отчет Всемирной организации здравоохранения (ВОЗ) от 25 мая 2021 года приводит следующие данные: коронавирусная инфекция 2019 года (COVID-19) уже поразила 166,4 миллиона людей по всему миру, что привело к смерти 3,4 миллиона человек [13]. Результаты научных исследований в Ухане показали высокую смертность (52%) среди пациентов с инфекцией COVID-19, осложненной ОРДС, причем смертность достоверно увеличивалась у пожилых людей с сопутствующими заболеваниями [14]. По-прежнему не существует противовирусного препарата с доказанной эффективностью, поэтому важную роль в профилактике и борьбе с инфекцией играет состояние собственной иммунной системы, а также сбалансированное питание для поддержания иммунитета [15].
В описанном случае химический плевродез был применен на следующий день после дренирования плевральной полости. Единственным условием было рентгенологически подтвержденное полное расправление легкого. Анализируя анамнез и течение заболевания, решили, что тенденции к самостоятельному закрытию дефекта в грудном протоке нет. В связи с этим авторами было принята отличная от традиционной тактика ведения больной. Проведение радикальной операции по перевязке грудного протока, несомненно, являющейся основным методом лечения, не представлялось возможным ввиду тяжелого состояния пациентки. Говоря постфактум, послеоперационный период повторной торакотомии однозначно усугубил бы течение двусторонней пневмонии. Избранная тактика позволила больной продолжить полноценное питание per os, что, несомненно, сыграло положительную роль в борьбе с коронавирусной инфекцией.
Выводы
1. Индукция плевродеза, на ранних стадиях течения хилоторакса, возможна и оправданна, так как исключает необходимость в переводе на парентеральное питание и как результат способствует более быстрому восстановлению и сопротивлению инфекционным заболеваниям.
2. Учитывая пандемию COVID-19, любое проявление острого респираторного заболевания должно расцениваться как подозрительный случай с проведением всех необходимых мероприятий для раннего выявления или исключения вирусного заболевания.
3. Применение йодповидона в качестве плевросклерозантов является эффективным, доступным и безопасным методом в лечении больных с хилотораксом.
4. Удаление дренажной трубки из плевральной полости, после химического плевродеза, возможно после снижения экссудации менее 150 мл.
5. Возможно применение химического плевродеза в качестве альтернативного способа лечения хилореи при невозможности перевязки грудного протока, в том числе и торакоскопическим методом.
6. Данный клинический случай является основанием для начала научного исследования данной проблемы с последующим обновлением тактики лечения пациентов с хилотораксом.



